2019年ASCO年會上,研究者公布了一項關於非小細胞肺癌(NSCLC)的臨床研究,該研究旨在評估HS-110+O葯聯合治療經檢查點抑製劑(CPI)治療失敗的晚期NSCLC患者的療效和安全性。
Viagenpumatucel-L (HS-110)是一種異基因細胞免疫療法。HS110-102「Durga」試驗是一項探索性的多隊列研究,評估HS-110聯合抗PD1單克隆抗體治療晚期NSCLC的療效。本次試驗提供了B隊列前20名患者的中期數據。
臨床數據
試驗共入組20名之前接受過至少4個月的檢查點抑製劑(CPI)治療後出現疾病進展的NSCLC患者。所有患者每周接受一次HS-110,每兩周接受一次O葯。本次試驗主要觀察終點是客觀反應率(ORR)。
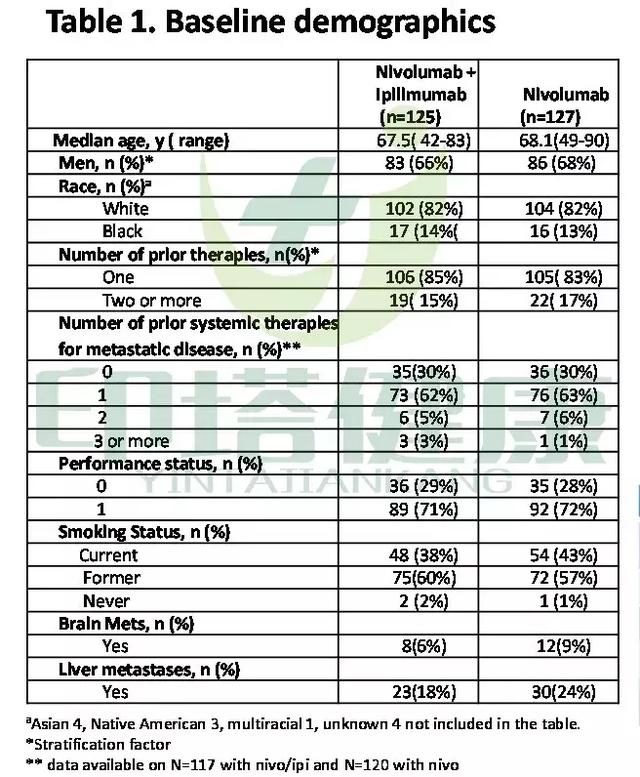
入組患者的人群特徵為:中位年齡65歲,70%為女性,75%為白人。50%ECOG評分為1,10%EGFR或ALK突變陽性。85%的患者為腺癌,15%的患者為鱗癌。85%的患者以前或現在吸煙,15%的患者從不吸煙。15%的患者之前接受過一種治療方案,45%的患者之前接受過兩種治療方案,40%的患者之前接受過三種或以上治療方案。
35%的患者PD-L1表達<1%,40%的患者PD-L1表達≥1%,25%的患者PD-L1表達情況無法評估。35%的患者CD8+腫瘤浸潤淋巴細胞(CD8+TIL)表達≤10%,30%的患者CD8+TIL表達>10%,35%的患者CD8+TIL表達無法評估。患者接受CPI治療的中位時間為10.2個月,患者停止CPI至開始HS-110+O葯治療的中位間隔時間為1.7個月。

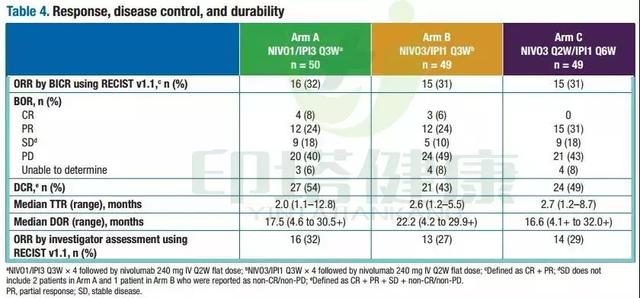
試驗結果表明,所有患者的ORR為15%,PR為15%。40%的患者疾病穩定,疾病緩解率(DCR)為55%。在35%的患者中觀察到腫瘤縮小。

患者的中位OS為NR(not reached 沒有達到)。65%患者存活,中位隨訪時間為5個月。

所有患者中,注射部位有反應(n=12)的患者和注射部位無反應(n=8)的患者的中位PFS為NR VS 1.8個月。

所有患者中,注射部位有反應(n=12)的患者和注射部位無反應(n=8)的患者的中位OS為NR VS 5個月。

不良反應
最常見的不良反應有:疲勞(55%)、咳嗽(35%)、呼吸困難(35%)、貧血(20%)、腹瀉(20%)、低血鈣症(20%)、體重減輕(20%)、頭暈(20%)、頭痛(20%)、皮膚瘙癢(20%)。

小結
1、HS-110聯合O葯耐受性較好;
2、HS-110聯合O葯在CD8+TIL低表達(≤10%)和PD-L1陰性腫瘤(<1%)中具有臨床活性;
3、皮膚注射部位反應的發生(任何級別)與無進展生存期和總生存期的改善有關。
【重要提示】本公號【全球好葯資訊】所有文章信息僅供參考,具體治療謹遵醫囑!