11月26日上午,治療轉移性結直腸癌的靶向藥物愛優特(愛優特為產品名稱,也稱呋喹替尼膠囊)在上海同濟大學附屬東方醫院開出了第一張處方。根據禮來公司給予第一財經記者的反饋,本周國內主要醫院和有需求的患者陸續可以拿到這款新葯了。目前第一階段主要還需患者自費。
「許多結直腸癌患者在二線治療失敗後,體能狀況都較好,生存慾望也很強烈。但由於國內目前三線的治療方案有限,留給患者的選擇餘地不多。」同濟大學附屬東方醫院腫瘤醫學部主任李進表示,「呋喹替尼經FRESCO研究結果證實,能顯著延長患者總生存期至9.3個月,有望成為晚期結直腸癌三線治療的標準治療方案。」

在中國,結直腸癌發病率、死亡率在全部惡性腫瘤中均位居第5位。其中,每年新發病例 37.6 萬,死亡病例 19.1 萬。據悉,近一半患者首診即為晚期或由於手術後複發轉移進入晚期疾病狀態,無治癒機會,他們大多以延長生存及提高生活品質為治療目標。
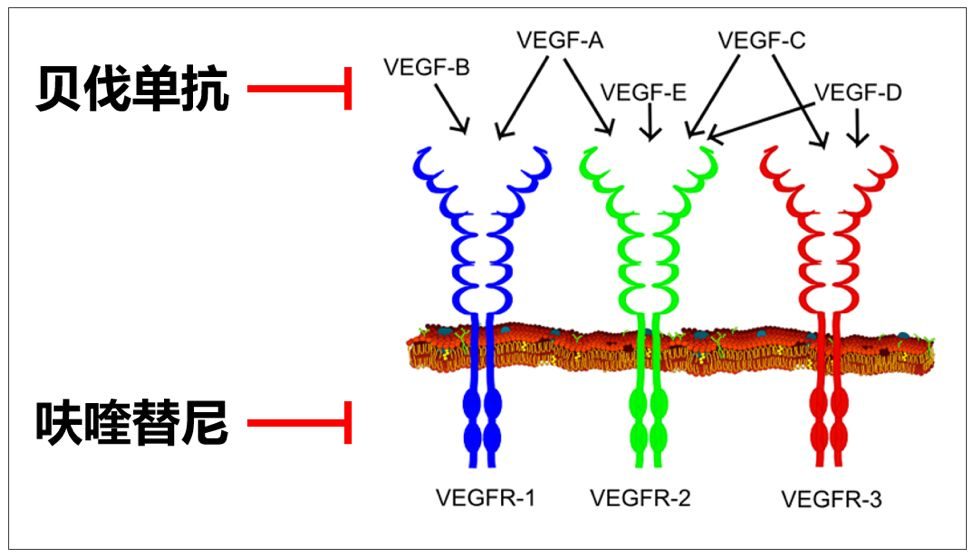
根據介紹,呋喹替尼是一個喹唑啉類小分子血管生成抑製劑,主要作用靶點是VEGFR激酶家族(VEGFR1、2和3)。通過抑製血管內皮細胞表面的VEGFR磷酸化及下遊信號轉導,抑製血管內皮細胞的增殖、遷移和管腔形成,從而抑製腫瘤新生血管的形成,最終發揮腫瘤生長抑製效應。
李進對第一財經記者表示,根據初步研究臨床結果提示,愛優特對二線化療甚至三線化療失敗的病人在疾病控制上在60%以上,也就是說100個病人裡面有超過60個病人可以從藥物應用當中獲益。
這一首個在國內發現、研發並獲批治療結直腸癌的抗腫瘤新葯是由記黃埔醫藥(上海)有限公司(下稱「和記黃埔醫藥」)自主研發。在2013年10月,和記黃埔醫藥與美國禮來公司達成了一項對呋喹替尼在中國市場範圍內進行授權、共同開發和商業化的協定。按照協定約定,和記黃埔醫藥負責呋喹替尼的開發,由此產生的費用由雙方共同承擔。
值得注意的是,呋喹替尼膠囊的快速獲批,得益於國家藥品上市許可人制度(MAH)的積極推進。2015年11月,中國開始試行上市許可人制度(MAH),2016年7月上海市食品藥品監督管理局開始全力推進MAH制度改革試點落地。2016年10月,呋喹替尼膠囊進入上海市食品藥品監督管理局MAH制度試點品種名單。
實際上,呋喹替尼從2006年立項到2018年9月被批準上市,歷經整整12年,耗資15億元。其也是和記黃埔醫藥成立16年以來首個獲批的新葯。
一直以來,我國醫藥產業長期以仿製葯為主,缺乏自主知識產權的創新葯。MAH制度是國際普遍實行的藥品管理制度,藥品批準文號和生產許可脫離,允許試點的藥品研發機構和科研人員取得藥品的批準文號,並且對藥品品質承擔相應的責任。開展藥品上市許可持有人制度試點工作,對於鼓勵藥品創新、提升藥品品質具有重要意義,讓研髮型的葯企可以把主要精力和資源都投入到新葯研發上。
和記黃埔醫藥科技有限公司執行董事及首席執行官賀雋指出,推行MAH,最大的益處是避免當前醫藥企業廣泛存在的重複投資建設現象,推動製藥產業結構調整和資源優化配置,促進創新藥物的生產和轉化,也大大加速了新葯上市的時間,相當於為呋喹替尼這類創新葯的上市開闢了「綠色通道」,為患者帶來更多益處。
他向記者強調,此次上市的呋喹替尼最大的特點是一個非常「乾淨」,即是靶點選擇性非常高,除了設定的靶點VEGFR以外,對其他靶點的抑製十分低,通過對VEGFR的抑製,可以抑製腫瘤的生長以及血液輸送,這對抑製腫瘤生長很重要。因為呋喹替尼具有高選擇性的和非常「乾淨」的靶點抑製,它的最大的潛力是和其他藥物聯合治療。
「我們現在已經在考察呋喹替尼和免疫療法和化學療法都有非常大的可能性和這些療法進行組合,未來我們也會在這些方面組合療法方面進行探索。」賀雋說。