肺癌佔癌症相關死亡率中的首位[1]。全球每年有超過130萬的患者死於肺癌,80%以上的病人為非小細胞肺癌[2],至少51%的肺癌患者被診斷為轉移性肺癌。儘管過去幾年中非小細胞肺癌(NSCLC)靶向治療有著明顯的進步,但晚期NSCLC的化療治療仍然至關重要。多項研究[3-8]顯示含有表皮生長因子受體(Epidermal Growth Factor Receptor, EGFR)激活突變的晚期肺腺癌患者應用EGFR酪氨酸激酶抑製劑(Tyrosine kinase inhibitors, TKIs)療效優於化療,這部分肺癌患者的中位生存時間可以達到3.5年[9],有效地改善預後。NCCN指南推薦:EGFR突變陽性晚期肺癌患者的首選TKIs治療,沒有EGFR突變的患者則採取以化療為主的綜合治療。EGFR活性突變存在與否決定了晚期肺癌治療的選擇,由於EGFR突變人群在高加索人群中佔9-21%[10,12],亞裔人群中佔40%左右[13,14],說明EGFR無突變(野生型)肺癌仍然佔有大多數,因此,化療在晚期肺癌治療的地位不可或缺。本文綜述了EGFR野生型晚期NSCLC的化療進展。
晚期EGFR野生型肺癌一線治療
自上世紀90年代中期以來,NSCLC的一線治療獲得了很大的進步。一些新葯含鉑方案(如泰素、多西他賽和吉西他濱聯合順鉑或卡鉑)已廣泛用於晚期NSCLC的治療。多項Ⅲ期隨機臨床試驗、重要的協作組研究及薈萃分析(ECOG1594)[15-18]均顯示,以鉑類藥物為基礎的化療優於最好的支持治療,能夠明顯延長患者生存期,減輕癥狀,改善生活品質。但各新葯與鉑類聯合的兩藥方案在一線治療晚期NSCLC的療效相同,各方案間的主要區別在於毒性特徵、給葯的方便性和治療費用的不同。晚期NSCLC一線治療的總體緩解率為20%~50%,中位進展時間4~6個月,中位生存期為8~10個月,1年生存率為30%~35%,2年生存率約為10%~15%[15-18]。這些結果提示,單純化療的療效似乎已經到達了「平台期」,無論藥物的種類、給葯的方式、劑量的強度和療程的調整,都難以進一步提高療效和改善預後。ECOG4599臨床研究[19]給晚期NSCLC患者帶來了新的希望。這個研究是將878例晚期NSCLC患者隨機分到PC組(444例,接受紫杉醇:200mg/m2+卡鉑:AUC=6;q3w方案化療6周期)和PCB組(434例,在上述相同化療基礎上加用貝伐單抗15mg/kg,q3w)直至病情進展。結果顯示,中位隨訪9.4個月,PC組、PCB組的有效率分別為10%、27%,無疾病進展分別為4.5個月、6.4個月,中位生存期分別為10.2個月、12.5個月,貝伐單抗的加入顯著提高了患者的臨床緩解率,延長了患者的生存期。這項研究具有劃時代意義,揭開了肺癌靶向一線治療時代的序幕。在歐洲進行的AVAIL研究[20]成為ECOG 4599的補充性研究,入組標準與ECOG 4599研究類似。AVAIL研究評價了不同劑量貝伐單抗聯合吉西他濱+順鉑(GP)方案治療ⅢB/Ⅳ期初治或複發的非鱗狀上皮細胞NSCLC患者的效果。結果顯示,與安慰劑組相比,安慰劑組、低劑量貝伐單抗組、高劑量貝伐單抗組的治療有效率分別為20%、34%(P<0.0001)、30%(P=0.0017);無疾病進展時間安慰劑組為6.2個月,低劑量貝伐單抗組為6.8個月(P=0.0003,HR=0.75,95% CI 0.64~0.87),高劑量貝伐單抗組為6.6個月(P=0.0456,HR=0.85,95% CI 0.73~1.00);中位生存時間分別為安慰劑組13.1個月,低劑量貝伐單抗組為13.6 個月(HR=0.92,95%CI 0.77~1.10),高劑量貝伐單抗組為13.4個月(HR=1.02,95%CI 0.85~1.22)。研究結果顯示GP方案中加入貝伐單抗一線治療晚期非鱗狀上皮細胞NSCLC未改善總生存,作者分析其原因可能是後續治療(化療、TKIs、外科治療和其他乾預措施)干擾了生存期。在兩項研究中發現,老年患者、鱗癌患者、有咯血或腦轉移者使用該葯有較高的風險。
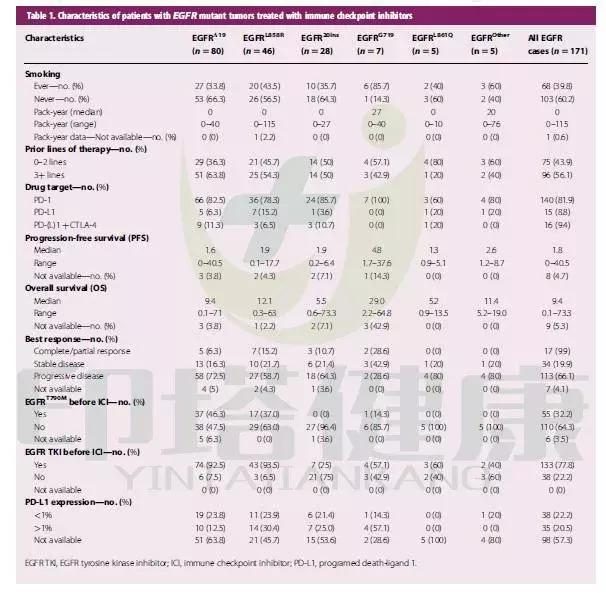
隨著IPASS研究[3]結果的公布,NSCLC的一線治療選擇在短短數年內,獲得了巨大的變化。研究證實[21,22],腺癌、不吸煙、女性和亞裔等群體是TKIs一線治療的優勢人群。IPASS研究[3,23]是在不吸煙的亞裔腺癌患者群體中進行的臨床試驗。結果顯示,在EGFR野生型肺癌中,紫杉醇+卡鉑(PC)方案化療優於吉非替尼治療,兩組有效率分別為23.5%和1.1%( P=0.0013),PFS分別為5.5月和1.6月(P<0.0001),中位生存時間分別12.7月與11.2月(p=0.309)。雖然EGFR野生型肺癌採取化療與靶向治療最後的中位生存時間在統計學上沒有差異,但絕對值相差1.5個月,也充分說明對於EGFR野生型晚期肺癌的治療應該選擇化療。採用相似設計的FIRST-SIGNAL研究[4]得出的結論與IPASS基本一致。隨後在EGFR突變人群中進行的6項研究[3-8],進一步證實了EGFR的突變狀態是決定EGFR-TKI一線療效的關鍵因素,已經寫入NCCN指南,這些結果無疑是NSCLC領域新的裡程碑。在未經選擇人群中進行的研究[3,4,24]分層分析中發現,EGFR無突變的患者,化療可以明顯延長無疾病進展時間,因此,對於EGFR野生型NSCLC患者仍是首選化療(見表1)。由於EGFR野生型肺癌仍然佔有大多數,化療在晚期肺癌治療的地位不可或缺。

對EGFR野生型NSCLC患者應用哪個化療方案更好的問題,沒有隨機研究可以回答這個問題。韓國的一項回顧性研究[25]對217例一線接受含鉑雙藥方案治療的進展期NSCLC患者檢測了EGFR突變情況,比較分析了紫杉類鉑二聯與吉西他濱鉑二聯療效與EGFR狀態的相關性。結果發現,EGFR野生型的患者中,兩個方案在反應率和無進展生存期上均無顯著性差異。因此對化療敏感性生物學標誌的研究尤為重要,也是大家不斷探索的方向。
化療方案選擇的生物標誌物
應用DNA修復酶作為選擇一線化療方案的生物標誌物的研究領域極其活躍。早期研究結果顯示,無論IHC或RT-PCR檢測的ERCC1低表達被認為是有益於選擇鉑類化合物的生物標誌物,RRM1低表達有利於選擇吉西他濱的生物標記物。由於ERCC1酶可以除去鉑類誘導的DNA加合物,故低ERCC1水準和鉑類敏感性相關[26]。RRM1是吉西他濱的重要靶位點的核苷酸還原酶的亞部門,低RRM1水準和吉西他濱敏感性相關。最近發表的在轉移性NSCLC中進行的III期TASTE試驗中[27],採用AQUA自動化免疫組化技術檢測ERCC1和RRM1表達,病人以2:1比例隨機分配到試驗組與對照組。試驗組根據RRM1和ERCC1的表達水準將患者分為4組,即(I)若RRM1和ERCC1是低表達,給予吉西他濱/卡鉑;(II)若RRM1高表達而ERCC1低表達,給予多西紫杉醇/卡鉑;(III)若RRM1低表達而ERCC1高表達,給予吉西他濱/多西紫杉醇;(IV)若二者均高表達,給予多西紫杉醇/長春瑞濱。對照組給予吉西他濱/卡鉑。PFS為主要觀察終點。結果發現在ERCC1和RRM1均低表達組中,對照組的吉西他濱+卡鉑方案療效優於多西他賽+卡鉑方案(5.0個月vs 8.1個月),與預期結果相反。客觀有效率及OS在各組間無顯著性差異。儘管作者認為在腫瘤中的化療分子檢測是可行的,AQUA方法的缺陷使得結果呈假陰性。ERCC1、RRM1兩個分子mRNA和蛋白表達水準無相關性。
胸甘酸合酶(TS),是一種重要的DNA修復酶和細胞生長的酶,亦是培美曲塞首要的靶向之一。培美曲塞有具有組織學特異性優點,鱗癌TS表達水準高於腺癌,TS過表達的肺癌對培美曲塞敏感性低[28]。在體外研究顯示,TS表達狀態與培美曲塞的敏感性相關[29]。
2013年ASCO會議上,來自西班牙的Moran代表西班牙肺癌協作組(SLCG)報告了另一分子標誌物導向的化療臨床試驗BREC[30]。研究組基於BRCA1和RAP80表達水準被分為3組:第1組,RAP80低表達,BRCA1任何水準表達,吉西他濱/順鉑化療;第2組,RAP80中/高表達,BRCA1低/中表達,多西他賽/順鉑化療;第3組,RAP80中/高表達,BRCA1高表達,多西他賽單葯化療。對照組採用多西他賽+順鉑治療,主要終點指標為PFS期。結果出人意料,PFS在試驗組的多西他賽組2.5個月,吉西他濱+順鉑組5.43個月,多西他賽順鉑組5.49個月,而未經分子標誌物選擇的多西他賽+順鉑對照組為5.49個月。可見試驗組不僅沒有取得主要終點的優勢,反而處於劣勢(P=0.003)。由於中期分析結果為陰性,本研究被提前終止。
目前分子標誌物檢測及指導化療方案的結果不如人意,與分子標誌物檢測方法、樣本處理不夠標準化、mRNA和蛋白檢測的異質性等問題尚未弄清楚相關。預測因子的研究向有利於將化療轉變為靶向化療的方向發展。
晚期EGFR野生型肺癌二線治療
厄洛替尼和多西他賽均為非選擇的晚期NSCLC二線標準治療藥物,所有的研究結果及指南中都未強調對接受二線及以上EGFR靶向藥物治療的NSCLC患者進行基因檢測的必要性。野生型NSCLC患者和非野生型NSCLC患者在二線治療時都可以使用吉非替尼或厄洛替尼,但作為靶向藥物的EGFR TKI,沒有靶點也能發揮作用嗎?日本學者在DELTA研究[31]中直接比較二線厄洛替尼和多西他賽治療晚期非小細胞肺癌的療效。結果顯示,不考慮EGFR突變狀態時,兩組中位PFS和OS無差別;對於EGFR野生型者,厄洛替尼和多西他賽的PFS為1.3 vs 2.9個月(Log-Rank P=0.013,HR=1.44,95%CI:1.08~1.92),但兩組OS無差別。該研究回答了EGFR野生型晚期NSCLC化療優於靶向治療的問題。2013年WCLC會議上我國學者報告了對於一項Ⅱ期多中心、隨機對照研究[32],比較了EGFR野生型晚期NSCLC二線吉非替尼和培美曲塞的療效。共入組157例患者,吉非替尼組81例,培美曲塞組76例,主要終點指標PFS 1.6 vs 4.8個月,HR=0.51(95%CI:0.36~0.73,P<0.0001)。雖然該研究的OS數據尚不成熟,但初步數據表明,EGFR野生型晚期NSCLC二線治療培美曲塞優於吉非替尼。因此,二線治療EGFR-TKI的作用需重新定位,佔多數的EGFR野生型患者,二線治療應以化療為首選,而不適合使用EGFR-TKI。
綜上所述,化療仍然是EGFR野生型晚期NSCLC患者一線、二線首選的治療方式,化療在無EGFR突變的NSCLC治療中的作用不可動搖,主要是含鉑類的藥物,包括紫杉醇、多西紫杉醇、吉西他濱、培美曲塞、長春瑞濱等,但目前仍沒有一線藥物明確的選擇,亦無相應的生物標誌物指導化療方案的選擇,這是今後努力的方向。但也應看到,目前針對EGFR突變的臨床研究設計中,僅根據EGFR突變狀態對晚期NSCLC患者進行分類研究,沒有排除EGFR野生型中含有的其他驅動基因突變對研究結果的影響,因此有必要進一步深入研究,細化10個肺癌驅動基因治療策略,包括與化療相結合的時序;對55%未檢測到驅動基因的晚期肺癌患者仍然要選擇以化療為主的綜合治療。化療在目前仍然是晚期肺癌治療的基石。