不想錯過界哥的推送?


哪些肺癌患者能從輔助化療中獲益?哪些肺癌患者最容易出現轉移?肺癌患者中的基因突變情況如何?
文丨Sharon
肺癌的發病率、死亡率居高不下,其研究進展日新月異,熟悉其治療發展趨勢,是臨床醫師和基礎研究人員的必備技能。每年的11月為全球肺癌關注月,11月17日是國際肺癌日,關於肺癌的最新進展有哪些?我們一起來了解下!
01
哪些肺癌患者術後輔助化療有益?腫瘤突變負荷或可預測
輔助化療目前被認為是切除術後Ⅱ~Ⅲ期非小細胞肺癌(NSCLC)患者的標準治療,5年生存獲益約為5%。然而對於哪些患者最有可能從輔助化療中獲益,目前臨床上尚無有用的預後和(或)預測生物標誌物。
近日,美國華盛頓大學醫學院Siddhartha Devarakonda等報告的LACE-Bio-II研究發現,較高的非同義腫瘤突變負荷(TMB)是切除術後NSCLC患者良好預後的強有力的預測因子,並可能用於識別不太可能從輔助化療中獲益的患者。研究顯示,在切除術後NSCLC患者中,較高的非同義TMB(>8個/Mb)提示良好預後,患者總生存(OS)率、無病生存率和肺癌特異性生存率(LCSS)均更佳;非同義TMB較低(≤4個/Mb)則反之,此類患者更有可能從輔助化療中獲益,接受輔助化療後的LCSS顯著提高(圖1)。


研究還發現,DNA損傷修復通路基因突變、腫瘤浸潤性淋巴細胞、TP53亞型改變和瘤內異質性均無預後或預測意義。
雖然研究顯示一些單基因可能具有預後或預測價值,但由於較高的偽發現率,單基因突變的影響較難確定。
該研究納入908例未匹配的、福爾馬林固定、石蠟包埋處理的肺癌組織標本,選取了1538個目標基因進行測序。通過嚴格的篩查標準以排除種系突變和因福爾馬林固定所導致的人為突變。
運用Cox模型分層分析患者的無病生存率、OS率和LCSS,並根據治療方式、年齡、性別、一般情況評分、組織學分型、手術方式和分期進行校正。在納入標本中共發現1515個基因存在非同義突變。
02
中央型肺腺癌更易早期轉移且生存更差
器官轉移是肺腺癌不良預後的重要影響因素,然而原發腫瘤位置對轉移部位和順序的影響尚未闡明。奧地利維也納醫科大學Thomas Klikovits等進行的一項多中心、大型隊列研究發現, 中央型肺腺癌更容易發生早期轉移,並導致生存期縮短[2]。該研究表明,在制定診斷策略和治療決策時或應考慮原發肺腺癌位置。
研究顯示,研究期間最常見的轉移部位為肺(33%)、骨(28%)、腦(25%)、腎上腺(13%)、胸膜(13%)、肝(12%)和皮膚(3%)。另外有19例(1.5%)患者發生心包轉移,29例(2.6%)發生其他罕見部位轉移(脾、腎、腹膜)。
其中,肺(P<0.001)、胸膜(P<0.001)和腎上腺(P<0.001)轉移通常較早發生,腦轉移(P=0.002)較晚發生。
對哪些轉移更容易同時發生的分析發現,腦轉移常常伴隨著骨轉移和肺轉移,骨轉移常常伴隨著肺轉移。而且,骨轉移伴隨腎上腺和肝轉移,腎上腺轉移伴隨皮膚轉移,以及胸膜轉移伴隨心包轉移的發生高於預期。
此外,與周圍型腫瘤相比,中央型原發肺腺癌更傾向於早期轉移(OR 1.43;P=0.02)。中央型腫瘤患者更多發生骨轉移(OR 1.86;P=0.017),而周圍型腫瘤更容易發生肺轉移(OR 1.35;P=0.015)。值得注意的是,下肺葉原發腫瘤患者更多發生胸膜轉移(OR 1.97;P=0.001)。
在單變數(HR 2.075;P=0.001)和多變數(HR=1.558;P<0.001)分析中,與周圍型腫瘤相比,中央型原發肺腺癌均與中位OS縮短相關(10.2個月 vs. 22個月),且獨立於腫瘤分期和T因子(圖2)。
原發肺腺癌位於上肺葉 vs. 下肺葉,或者左肺 vs. 右肺對OS無顯著影響,而腫瘤分期和T因子是不良預後的重要預測因素。在肺腺癌診斷時已出現器官轉移的622例(55%)患者中,出現2處轉移者較1處轉移者OS縮短的風險顯著升高(13.4個月 vs. 3.7個月;HR 1.339),3處轉移者也較2處轉移者OS縮短的風險顯著升高(9.4個月 vs. 9.4個月;HR 1.917),但出現4處(4.3個月)和5處(3.8個月)轉移者與2處轉移者的OS無顯著差異。


該研究共納入2001-2014年在5家中心接受診治的1126例肺腺癌白人患者。診斷時有435例(38%)患者存在單器官轉移,187例(16%)存在多器官轉移。隨訪期間,另有243例(22%)患者發生轉移,即「晚期轉移」。690例(61%)患者為周圍型原發腫瘤,434例(39%)為中央型原發腫瘤。
03
吳一龍教授:半數EGFR陽性晚期NSCLC患者存在T790M耐葯突變
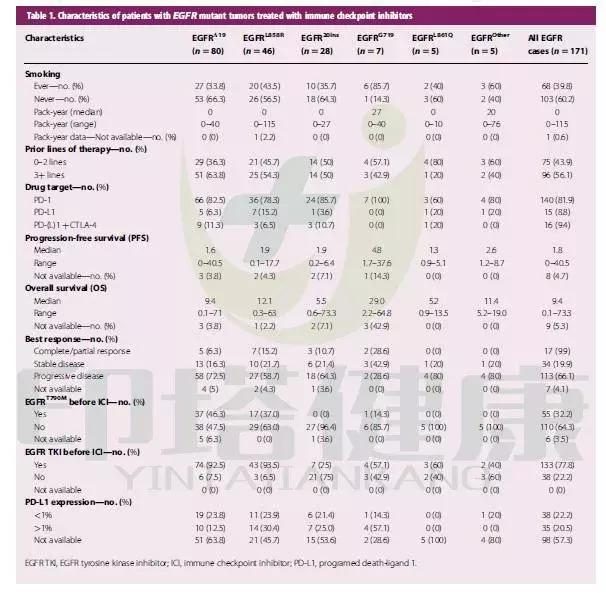
表皮生長因子受體(EGFR)酪氨酸激酶抑製劑(TKI)是晚期EGFR突變陽性NSCLC患者的一線治療。ex19del和L858R是最常見的EGFR突變類型,約佔90%,存在這兩種突變的患者往往對EGFR-TKI治療敏感。而EGFR T790M突變的存在會導致EGFR-TKI一線治療發生耐葯。
廣東省人民醫院吳一龍教授等對AURA3研究進行的一項回顧性分析發現,在EGFR-TKI治療後進展的EGFR突變陽性晚期NSCLC患者中,約一半存在T790M突變。而且,相對於L858R突變,T790耐葯突變更多存在於ex19del突變的患者中。該結果提示了基於激活突變的耐葯機制的差異性[3]。研究顯示,在820例具有有效EGFR突變檢測結果數據的患者中,分別有58%、35%和55%的患者存在ex19del、L858R和T790M突變。
T790M突變率不受種族影響。在亞洲和非亞洲人群中T790M(53% vs. 58%)和ex19del(56% vs. 63%)突變的檢出率均相似。與之相反,L858R突變率在亞洲人群中相比非亞洲人群中更高(39% vs. 28%;P=0.0017)。與存在L858R突變者相比,ex19del突變者中T790M突變的患者比例更高(64% vs. 47%)。同樣,T790M突變率也不受之前使用的EGFR-TKI類型影響(圖3)。


圖3 ex19del、L858R和T790M突變率不受種族影響
此外,有28例(3%)罕見EGFR突變患者同時存在T790M突變,包括G719X(2%)、ex20ins(1%)和S768I(<1%)。
該研究結果與既往報告的該人群中的T790M檢出率一致。
AURU3是一項隨機III期研究,在EGFR-TKI一線治療後進展的EGFR T790M陽性晚期NSCLC患者中,比較了奧斯替尼治療相比鉑類加培美曲塞的臨床獲益。
參考文獻
[1]Devarakonda S, Rotolo F, Tsao MS, et al. Tumor Mutation Burden as a Biomarker in Resected Non–Small-Cell Lung Cancer. J Clin Oncol. 2018 Aug 14:JCO2018781963. doi: 10.1200/JCO.2018.78.1963.
[2]Klikovits T, Lohinai Z, Fabian K, Gyulai M, Szilasi M, Varga J, Baranya E, Pipek O, Csabai I, Szallasi Z, T?mar J, Hoda MA, Laszlo V, Hegedus B, Renyi-Vamos F, Klepetko W, Ostoros G, Dome B, Moldvay J, New insights into the impact of primary lung adenocarcinoma location on metastatic sites and sequence: a multicenter cohort study, Lung Cancer (2018), https://doi.org/10.1016/j.lungcan.2018.11.004
[3]John T, Akamatsu H, Delmonte A, Su W-Chou, Lee JS, Chang G-Chen, Huang X, Jenkins S, Wu Y-Long, EGFR mutation analysis for prospective patient selection in AURA3 phase III trial of osimertinib versus platinum-pemetrexed in patients with EGFR T790M-positive advanced non-small-cell lung cancer, Lung Cancer (2018), https://doi.org/10.1016/j.lungcan.2018.10.027