近日,在中國臨床腫瘤學會(CSCO)指南大會上,結合最新肝癌研究進展,CSCO臨床腫瘤學研究基金會理事長、解放軍東部戰區總醫院全軍腫瘤中心主任秦叔逵教授就《CSCO原發性肝癌診療指南》(以下簡稱「《指南》」)的系統治療進行了要點解讀。
遵循「更細、更快、更新」的特色
《指南》亮點薈萃
1.1.充分考慮中國「肝癌大國」的實際國情和臨床實踐,強調依據中國證據和專家推薦。
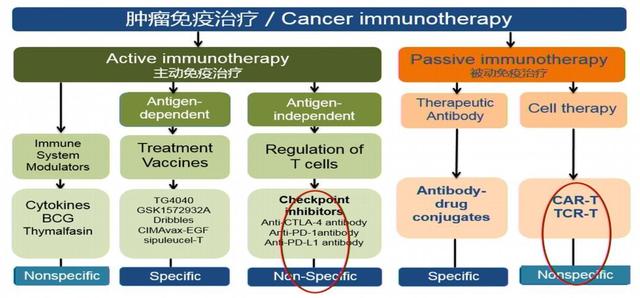
1.2.全球首個證實為肝癌患者帶來生存獲益的PD-1抑製劑——納武利尤單抗,以及帕博利珠單抗已作為肝癌二線推薦,被納入2018版指南。現隨著PD-1抑製劑在肝癌領域的多個臨床試驗的推進,免疫話題仍作為此次《指南》解讀的重點進行了深入探討。
1.3. 「多模式、多學科、多藥物」:免疫治療的一線推進離不開中國數據,免疫聯合方案也將進一步提升肝癌治療的療效及生存期,成為未來中國肝癌診療不可或缺的重要部分。
/鎖定肝癌「異質」特性
訂製《指南》立足國情/
2019年1月,國家癌症中心發布的中國惡性腫瘤流行情況數據顯示,中國原發性肝癌新發病例37萬,約佔全球44%;死亡病例32.6萬,約佔全球42%[1,2]。其中,肝細胞癌(HCC)患者佔所有肝癌患者的85%-90%[3],是最常見的消化系統惡性腫瘤。就既往HCC發病與死亡率數據判斷,中國目前依然處於全球肝細胞癌「高危地區」的首位 [1]。
總體而言,中國HCC在流行病學特徵、分子生物學行為、臨床表現和分期、治療方法以及預後轉歸等方面都具有高度異質性。
對此,《指南》特彆強調根據中國國情來指導臨床實踐,採用大量中國人群研究數據,把握特點有的放矢,而非完全照搬國外經驗。同時,遵循證據級別和專家推薦級別對各種治療進行不同推薦,制定過程中亦充分考慮藥效經濟學。
/免疫治療開啟肝癌征程
無懼「中國特色」難題/
在中國,約85%的HCC患者在確診時已處於疾病晚期,喪失了手術的時機,總體五年生存率僅為10%[4]。針對晚期肝癌患者的治療正面臨三大難題:第一,晚期患者雖經靶向治療得到緩解,但生存期較短,改善預後效果有限,如何突破?第二,中期患者經過化療和TACE介入治療後,如何使療效進一步提高?第三,早期患者手術治療後,如何預防腫瘤複發?
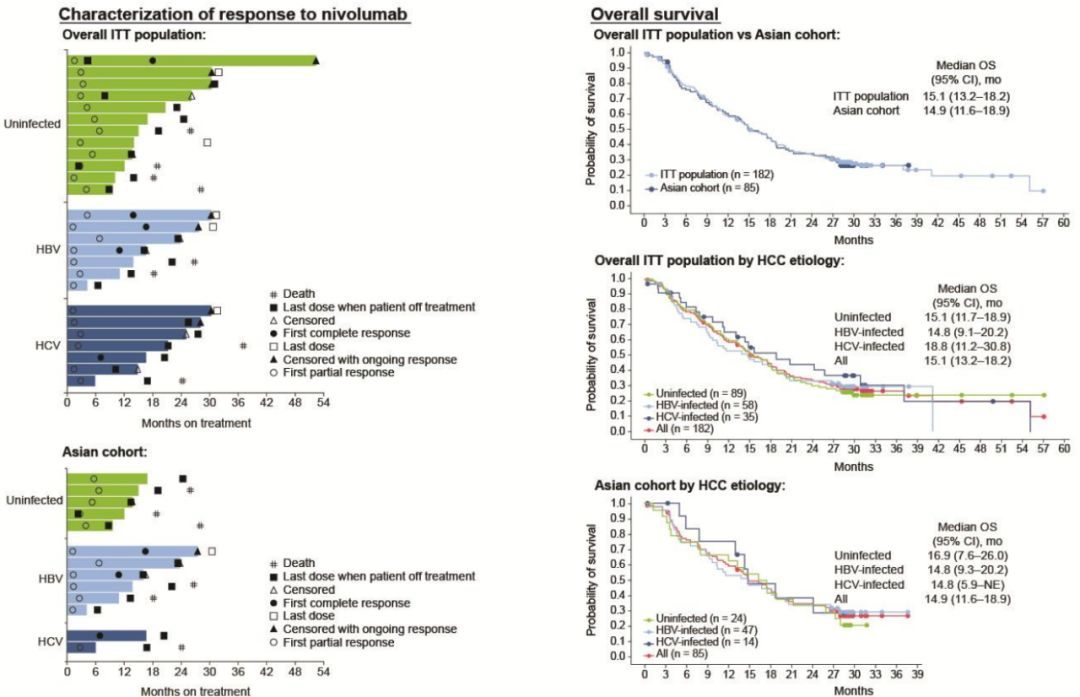
而一項名為CheckMate 040研究的關鍵性結果,為中國肝癌治療僵局帶來了轉機。CheckMate 040是一項單臂治療晚期肝細胞癌的I/II期劑量遞增及擴展臨床試驗。入組人群包含未接受過索拉非尼治療的一線初治患者,及以往進行過索拉非尼治療的二線經治患者,且不排除慢性病毒性肝炎患者。研究結果表明,納武利尤單抗在晚期肝癌中療效優異、安全性良好,且東西方人群療效一致 [5,6]:
一線中位總生存期(mOS)高達28.6個月,客觀緩解率(ORR)為20%左右;二線mOS分別為15個月(劑量遞增組)與15.6個月(劑量拓展組),ORR為15%左右[5]。
總體安全性與免疫治療用於其它瘤種數據相似,沒有新的安全性問題出現,3-4級不良反應較少,且可防可控[5]。
入組患者中,包括中國人群在內的亞洲患者佔比近50%,結果顯示亞洲患者與總人群的兩年生存率分別為34.5%和33.6%,治療反應和生存率均相當[6]。
亞洲人群不同病因的患者均能獲益,HBV與HCV感染患者mOS均為14.8月,且HBV患者的兩年生存率同樣能達到34%[6]。
作為肝癌領域免疫腫瘤治療的里程碑式關鍵研究,CheckMate 040為「中國特色」難題進行了解答。致病因素層面上,中國肝癌患者HBV病毒感染比例非常高,免疫治療能為亞洲人群與HBV患者帶來無異於其他病因肝癌患者的獲益,且數據證明,在進行有效的抗B肝病毒的治療下,PD-1抑製劑並不會加強B肝病毒的感染;療效層面上,相比靶向藥物3.3%-7%之間的ORR [7,8,9,10],PD-1抑製劑所達到的15%-20%有效率[5],意義重大。
基於此研究在內的多項研究結果,PD-1抑製劑已被國內外各大指南(如NCCN、ESMO、EASL及CSCO指南等)作為晚期肝癌的二線治療推薦。在最新的歐洲腫瘤內科學會(ESMO)肝細胞癌(HCC)的診斷、治療和隨訪指南中,納武利尤單抗還被推薦為唯一用於HCC一線治療的PD-1抑製劑。
/致敬肝癌患者生命之春
免疫治療未來猶可期/
免疫檢查點抑製劑已經在晚期肝癌患者身上顯示了有前景的臨床療效,CheckMate 040研究結果讓我們看到了PD-1抑製劑延展至肝癌一線治療的潛力和機遇。隨著更多一線臨床試驗的穩步推進,免疫治療有望向一線用藥全線進軍。
與此同時,多項正在進行的臨床試驗顯示免疫治療與介入、化療、靶向治療的聯合必將進一步提升肝癌治療的療效,未來肝癌治療的主流趨勢將是多種治療手段的聯合,免疫治療也將會是其中重要的部分。
此外,正如《指南》所強調,在臨床實踐中,醫務工作者要充分考慮患者的家庭條件,經濟狀況以及治療意願,做到真正的「以患者為中心,開展MDT多學科團隊模式為載體」的全程管理。為滿足不同的醫療需求,在整個醫療實踐過程中,應讓患者積極參與,了解不同治療手段特點,醫患共同制定最「適合」、最具「性價比」的個體化治療決策。
*目前,尚未有免疫腫瘤治療藥物在中國大陸獲批肝癌適應症
[參考文獻]
1. Global Cancer Statistics 2018: GLOBOCAN Estimates ofIncidence and Mortality Worldwide for 36 Cancers in 185 Countries [J]. CA: ACancer Journal for Clinicians, 2018;68:394-424.
2. 2015年中國惡性腫瘤流行情況分析[J].Chin J Oncol, 2019;41(1): 19-28
3. 中華人民共和國國家衛生和計劃生育委員會,原發性肝癌診療規範(2017年版)
4. Zhu, Q., Li N.,Zeng X. et al. Hepatocellular carcinoma in a large medical center of China overa 10-year period: evolving therapeutic option and improving survival.Oncotarget. 2015 Feb; 6(6): 4440-4450.
5. El-Khoueiry, A.B.,Sangro, B., Yau, T. et al. nivolumab in patients with advanced hepatocellularcarcinoma (CheckMate 040): an open-label, non-comparative, phase 1/2 doseescalation and expansion trial[J]. Lancet, 2017. Jun 24;389(10088):2492-2502.
6. Hsu C., et al.nivolumab in advanced hepatocellular carcinoma (aHCC): Asian Cohort Analysisfrom the CheckMate 040 study. Poster presented at 2018 CSCO. 2018 Sep.
7. Kudo, M.,Finn, R.S., Qin, S. et, al. Lenvatinib versus sorafenib in first-line treatmentof patients with unresectable hepatocellular carcinoma: a randomised phase 3non-inferiority trial. Lancet. 2018 Mar; 391(10126): 1163-1173.
8. Chen, A.L.,Kang, Y.K., Chen, Z. et al. Efficacy and safety of sorafenib in patients in theAsia-Pacific region with advanced hepatocellular carcinoma: a phase IIIrandomised, double-blind, placebo-controlled trial. Lancet Oncol. 2009Jan;10(1):25-34.
9. Bruix, J.,Qin, S., Merle, P. et al. Regorafenib for patients with hepatocellularcarcinoma who progressed on sorafenib treatment (RESORCE): a randomised,double-blind, placebo-controlled, phase 3 trial. Lancet. 2016Dec:389(10064):56-66.
10. 秦叔逵,HCC免疫治療實踐的若乾重要問題,CSCO第三屆全國腫瘤免疫高峰論壇現場講話,2019年4月.
本文轉載自其他網站,不代表健康界觀點和立場。如有內容和圖片的著作權異議,請及時聯繫我們(郵箱:[email protected])