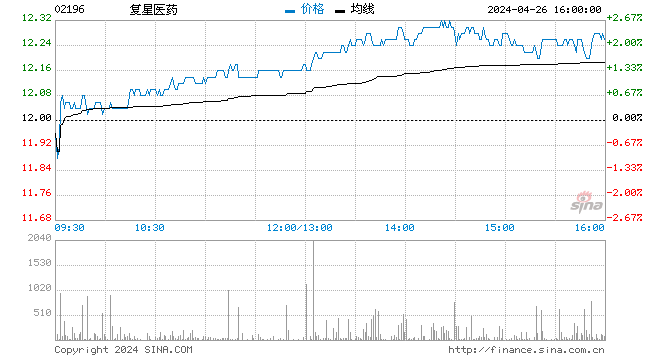
複星公告承認曾被美食品藥品監督管理局警告 昨天股價大幅下跌
針對網絡反映舉報重慶醫藥工業研究院有限責任公司的情況,國家藥品監督管理局已責成重慶市食品藥品監督管理局開展徹查,盡快查清核實。如發現違法違規行為,依法嚴肅查處。調查結果及時向社會公開。國家藥監局已派出督查組,對調查工作進行督查。
遭遇前員工舉報企業旗下全資子公司控股的孫公司存在“原料藥工藝造假”行為後,上市公司複星醫藥昨天緊急作出回應,稱根據相關公司自查,其現有產品均根據已批準的工藝進行生產,在生產過程中對於生產工藝的調整也均經相關藥監部門批準或備案。不過複星醫藥在公告中也承認,美國食品藥品監督管理局(FDA)2016 年5月對該孫公司一工廠進行檢查時,針對其 QC 實驗室原料藥檢查中所發現的實驗室數據規範性不足出具過警告信並提出整改要求。
受到這一舉報事件的影響,複星醫藥昨天大幅低開,盤中甚至曾觸及跌停,但隨後有所反彈,最終全天下跌6.89%,成交量大幅放大兩倍多,換手率達到4.44%。
“因藥物數據造假被FDA警示”
近日,重慶市食品藥品監管局公開信箱收到有關“重慶醫藥工業研究院製藥公司嚴重違反藥品管理法”的舉報信件,其中所涉及的“重慶醫工院”即為複星醫藥旗下全資子公司上海複星醫藥產業發展有限公司控股的重慶醫工院。該舉報信稱重慶醫工院存在“原料藥工藝造假”行為。舉報人同時提到,在2016年5月美國FDA現場檢查後,重慶醫工院收到了警告信!2017年11月美國FDA再次現場檢查,又出現了嚴重違反藥品管理法規的情況,得到了美國FDA給予的最差評價結果(OVI)”,舉報人還提供了相關警告信的原文。
重慶醫工院主要從事仿製藥生產等業務
公開資料顯示,重慶醫工院是複星醫藥控股孫公司,主要從事仿製藥原料藥和中間體的研發、生產和銷售。重慶醫工院(合並口徑)去年實現營業收入7780萬元,對應複星醫藥集團2017年度營業收入的0.42%,淨利潤虧損3461萬元。重慶醫工院主要客戶為歐美及中國的製劑企業,其中境外銷售收入佔比約26%。
對此,複星醫藥昨天在公告中承認了重慶醫工院在2016 年 5 月接受FDA檢查時,一工廠存在 QC 實驗室原料藥的實驗室數據規範性不足,被FDA出具警告信並被提出整改要求。據悉,該事件複星醫藥此前已經予以公告,但具體資訊披露得不像舉報信這樣詳細,因此當時在外界產生的影響也遠不像此次舉報信這麽大。
飛行檢查尚無結論
根據複星醫藥披露,重慶食藥監局在接到舉報信後已經開展相關調查,並已於8月23日對重慶醫工院進行了飛行檢查,飛行檢查的結果尚待結論性意見。複星醫藥董事長陳啟宇也回應稱,公司高度重視本次舉報事件,目前集團總部已派員到企業現場對生產管理進行嚴格檢查,核實情況。 重慶市食品藥品監管局也表示已啟動對被投訴舉報企業的相關調查工作,已派出檢查組進駐企業,如發現存在違法違規生產行為,將依法進行查處。
文/本報記者 張欽
責任編輯:依然