▎葯明康德/報導
近日,默沙東(MSD)宣布FDA已經批準其重磅免疫療法Keytruda上市,治療縱膈大B細胞淋巴瘤(PMBCL,一種非霍奇金淋巴瘤)。值得一提的是,這是首個治療這一疾病的抗PD-1療法,也是Keytruda在惡性血液癌症領域的第二個適應症。


PMBCL是一種侵襲性瀰漫性大B細胞淋巴瘤,佔所有非霍奇金淋巴瘤的約2%至4%,這種疾病主要影響青年人,女性患者比例約為男性患者的1.7-2倍。
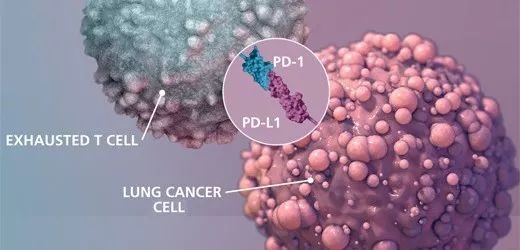
Keytruda是一種已被批準用於多種癌症的免疫療法,可治療黑色素瘤、非小細胞肺癌、以及頭頸部鱗狀細胞癌等。它可以選擇性阻斷PD-1與其配體PD-L1和PD-L2結合,激活淋巴T細胞殺死癌細胞。默沙東正在對Keytruda進行750項不同的臨床試驗。
此次PMBCL適應症的獲批,是基於多中心、開放標籤、單臂臨床研究KEYNOTE-170的試驗數據。患者每三周接受一次200 mg固定劑量的Keytruda單葯治療,直至病情進展或毒性變得不可接受。主要終點是總體緩解率(ORR),關鍵次要終點包括緩解持續時間(DOR)、藥物安全性和耐受性。


試驗結果顯示,Keytruda治療組的ORR為45%(24例,95% CI:32-60),完全緩解率(CRR)為11%,部分緩解率(PRR)為34%。在24例參加隨訪的患者中,中位DOR尚未達到(範圍:1.1-19.2+月),實現客觀緩解(完全或部分)的中位時間為2.8個月(範圍:2.1-8.5月)。
Dana-Farber癌症研究所血液腫瘤治療中心的醫學腫瘤學家Philippe Armand博士表示: 「複發性或難治性PMBCL通常是一種難治的疾病,而且許多患者都是年輕人。Keytruda的臨床試驗治療,產生了有意義的緩解率,一些患者能達到完全緩解。因此該批準為疾病發生進展,或歷經多次治療仍不幸複發的PMBCL患者提供了另一種治療選擇。」


▲默沙東研究試驗室腫瘤臨床研究副總裁Jonathan Cheng博士(圖片來源:默沙東官網)
默沙東研究試驗室腫瘤臨床研究副總裁Jonathan Cheng博士說:「默沙東的抗PD-1療法Keytruda此次獲得的難治性或複發性PMBCL適應症批準,將給這種罕見疾病患者提供重要的治療新選擇,這體現了默沙東一貫的對血液癌症患者的承諾,並標誌著Keytruda在血液惡性腫瘤中的第二個適應症。」
我們期待Keytruda能為廣大的癌症患者帶來更多好消息!
參考資料:
[1] FDA Approves Merck』s KEYTRUDA? (pembrolizumab) for Treatment of Refractory or Relapsed Primary Mediastinal Large B-Cell Lymphoma (PMBCL)
[2] FDA Accepts Supplemental Biologics License Application (sBLA), Assigns Priority Review to Merck』s KEYTRUDA? (pembrolizumab) for Treatment of Relapsed or Refractory Primary Mediastinal Large B-Cell Lymphoma (PMBCL)
[3] 默沙東官網
[4] Primary Mediastinal Large B-cell Lymphoma

 播放GIF
播放GIF
TAG: |