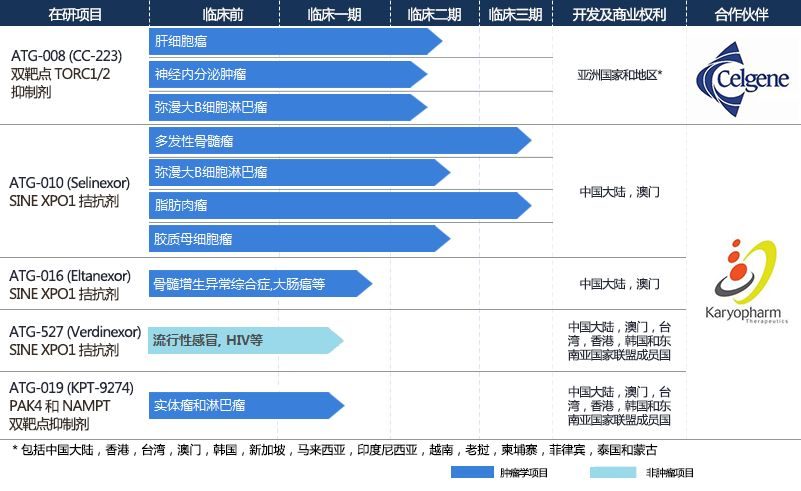
近日,美國Karyopharm Therapeutics公司宣布,美國FDA已經授予了Selinexor(KPT-330)治療難治性多發性骨髓瘤的優先審查資格。
Selinexor是一種XOP1抑製劑。該新葯申請的依據是臨床IIb期STORM試驗的結果,該試驗檢測了Selinexor+地塞米松的組合治療難治性多發性骨髓瘤患者的效果。2018年血液腫瘤學會(SOHO)年會上發布的最新數據顯示,難治性多發性骨髓瘤患者對這種治療方案的總體反應率為26.2%,中位總生存期為8.6個月。
西奈山Tisch癌症研究所的多發性骨髓瘤項目主任和醫學教授Sundar Jagannath在SOHO發表了STORM試驗的研究結果。他解釋說,所有對治療有反應的患者都明顯獲益,中位總生存期為15.6個月。而之前的病歷記錄顯示,難治性多發性骨髓瘤患者人群的中位總生存期僅3.6個月。
根據《處方葯申報者付費法案(PDUFA)》,FDA將在2019年4月6日之前就該項新葯申請做出決定。
「作為一項潛在的新療法,Selinexor應用了新的機制,臨床表現也很驚艷,我們認為口服selinexor獲批後將成為患有難治性骨髓瘤患者的重要治療選項,」Karyopharm的創始人、總裁兼首席科學官Sharon Shacham博士在一份聲明中說。「FDA接受此新葯申請審查並授予優先審查資格是Selinexor項目重要的裡程碑,這也反映了該患者群體中有強烈的未滿足的需求。我們期待在審查過程中與FDA合作。」
來源:

 播放GIF
播放GIF
愛諾美康直播
10月14日(周日)晚20:00,與您相約
進入方式:1.掃描二維碼,進入直播間
2.點擊閱讀原文,進入直播間


專註腫瘤與重大疾病
不片面為了尋求合作而與醫院簽署轉診患者數量條款,堅持結合醫院優勢,從患者病情角度推薦更好的醫院和專家
不接受短期逐利資本投資,避免被資本綁架
-
不利用合作關係、綠色通道誤導患者,不誇大出國看病難度;個性化分析出國利弊,不給患者虛擬的希望
不介入醫院收費,患者直享醫院收費10-45%折扣,不利用美國保險漏洞漁利
業內創立了三段式收費(簽約時30%,預約醫生、簽證通過後40%, 出國後30%),信守翻譯錯誤全額退款的機構。
出國看病整體解決方案提供商
貴賓熱線:400-900-1233
官方網址 : www.auromcs.com
深圳公司:深圳福田區福中三路1006號諾德金融中心30E