本文系生物谷原創編譯,歡迎分享,轉載須授權!
腫瘤免疫治療巨頭默沙東(Merck & Co)近日宣布,PD-1免疫療法Keytruda(pembrolizumab,帕博利珠單抗)已獲中國藥品監督管理局(CNDA)批準,用於前一種療法治療失敗的不可切除性或轉移性黑色素瘤成人患者的治療。審查方面,Keytruda之前已被CNDA授予優先審評資格,從申報上市到獲得批準隻用了5個月時間。

此次批準,使Keytruda成為中國市場獲批治療晚期黑色素瘤的首個也是唯一一個抗PD-1療法,同時也是繼百時美施貴寶Opdivo之後在中國市場獲批的第二款抗PD-1療法,後者於今年6月中旬獲批,用於二線治療非小細胞肺癌(NSCLC),具體為EGFR陰性、ALK陰性、既往接受含鉑化療後病情進展或不可耐受的局部晚期或轉移性NSCLC成人患者。
此次Keytruda在中國獲批,是基於一項Ib期臨床研究KEYNOTE-151的總緩解率(ORR)數據。該研究在103例先前接受過系統療法治療後病情進展的局部晚期或轉移性黑色素瘤的中國成人患者中開展,評估了Keytruda單葯療法的療效和安全性。
KEYNOTE-151研究的首席研究員、中國臨床腫瘤學會(CSCO)惡性黑色素瘤專家委員會主任委員、中國黑色素瘤協會會長、北京大學腫瘤醫院副院長郭軍教授指出,在過去幾十年裡,我們對抗惡性黑色素瘤的選擇非常有限。使用傳統治療方案,患者的長期生存獲益非常低。惡性黑色素瘤是對免疫療法反應最敏感的腫瘤之一;在國外, 以帕博利珠單抗為代表的 PD-1抑製劑早已成為了惡性黑色素瘤的標準治療手段。如今帕博利珠單抗在中國獲批,意味著晚期惡性黑色素瘤患者終於有了與世界接軌的治療方案, 也將推動中國晚期惡性黑色素瘤的治療格局的改變,這在人類對抗惡性黑色素瘤歷史上具有裡程碑式意義!
默沙東中國總裁羅萬裡(Joseph Romanelli)表示,我們由衷讚賞中國政府大力推進創新藥物引入中國和加速新葯審評審批的力度,帕博利珠單抗的成功研發,體現了默沙東在腫瘤免疫治療領域的專註與投入,以及對患者的堅定承諾。從干擾素到PD-1抑製劑,默沙東始終以創新為驅動,為患者帶來全新治療方案。我們將繼續與政府、醫療機構、專家和醫護人員展開合作,擴展帕博利珠單抗在中國的其他適應症,同時快速擴大其可及性,讓更多中國腫瘤患者受益於前沿的免疫治療。
黑色素瘤(melanoma)是一種來源於黑色素細胞的惡性腫瘤,是最致命的皮膚癌類型之一,特徵為色素生成細胞不受控制的生長。在中國,黑色素瘤是中國發病率增長最快的惡性腫瘤之一,每年以3%-5%的速度增長,已成為嚴重危及中國居民健康的重要疾病。黑色素瘤惡化程度較快,極易出現遠處轉移,因此,一旦進入腫瘤晚期,既往治療手段療效相對較差,患者的預後及生活品質受到很大影響。研究數據顯示,一旦發生腫瘤轉移,黑色素瘤患者的5年生存率僅為4.6%。
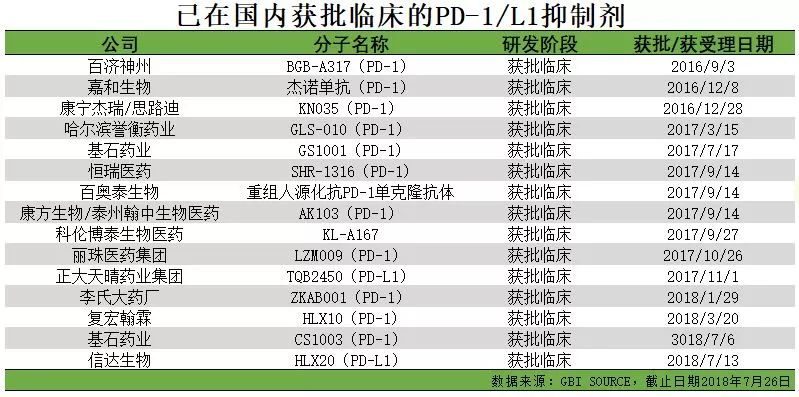
PD-(L)1市場格局:百濟神州tislelizumab或成首個本土研發、全球上市的第7個PD-(L)1免疫療法
目前,全球已有5款PD-(L)1免疫療法上市,除了Keytruda和Opdivo之外,還包括羅氏的Tecentriq、阿斯利康的Imfinzi、默克/輝瑞的Bavencio。其中,Keytruda是該領域的領頭羊,在美國市場,該葯已獲批多種類型癌症的治療,包括:黑色素瘤、肺癌、頭頸部癌、經典霍奇金淋巴瘤、原發性縱膈大B細胞淋巴瘤、尿路上皮癌、微衛星高不穩定(MSI-H)癌症、胃癌、宮頸癌。此前,醫藥市場調研機構EvaluatePharma發布報告預測,Keytruda在2024年將成為全球最暢銷的腫瘤學藥物,銷售額將高達126.86億美元,百時美施貴寶的Opdivo屆時的銷售額也將高達112.47億美元。
今年4月,由賽諾菲和再生元合作研製的cemiplimab獲美國FDA受理,預計將成為上市的第6款PD-(L)1療法。
就在上周,百濟神州的PD-1療法tislelizumab治療霍奇金淋巴瘤關鍵性臨床研究獲得成功,預計將在今年晚些時候在中國申報上市;同時,百濟神州與合作夥伴新基宣布,將於2019年上半年向美國FDA提交tislelizumab治療華氏巨球蛋白血症的上市申請。業界預測,tislelizumab或將成為首個由中國本土研發、全球上市的第7個PD-(L)1免疫療法。
原文出處:
KEYTRUDA? (pembrolizumab) is the First Anti-PD-1 Therapy Approved in China for Advanced Melanoma