女性乳腺是由皮膚、纖維組織、乳腺腺體和脂肪組成的,乳腺癌是發生在乳腺腺上皮組織的惡性腫瘤。乳腺癌中99%發生在女性,男性僅佔1%。據中國腫瘤登記年報顯示:女性乳腺癌年齡別發病率0~24歲年齡段處較低水準,25歲後逐漸上升,50~54歲組達到高峰,55歲以後逐漸下降。
乳腺癌的病因目前尚未完全清楚,研究發現乳腺癌的發病存在一定的規律性,具有乳腺癌高危因素的女性容易患乳腺癌。所謂高危因素是指與乳腺癌發病有關的各種危險因素,而大多數乳腺癌患者都具有的危險因素就稱為乳腺癌的高危因素。
雖然我國乳腺癌的發病率趨勢並不樂觀,但事實上,乳腺癌患者的癌後生存率還是相對不錯的。乳腺癌患者好好治療,帶癌生存也是不影響生活的,而且完全治癒的案例也不少。


HER-2陽性晚期乳腺癌患者的福音:
注射用重組抗HER-2(表皮生長因子受體2)人源化單克隆抗體(簡稱GB221)是由嘉和生物葯業有限公司開發的,針對HER-2(表皮生長因子受體2)受體的乳腺癌分子靶向治療藥物。臨床前研究證實,GB221與已上市同類藥物赫賽汀在蛋白結構、理化特性和凍融穩定性方面具有相似性,具有明顯的體內外抗腫瘤作用,安全性良好。
全國多家大型醫院正在開展一項注射用重組抗HER-2(表皮生長因子受體2)人源化單克隆抗體的國際III期臨床研究,如您是HER-2(人類表皮生長因子受體2)陽性晚期乳腺癌的患者,您有可能適合參與本次臨床研究。
本研究已經獲得國家食品藥品監督管理局批準(批件號:2013L01513),計劃招募大約412例HER-2(人類表皮生長因子受體2)陽性晚期乳腺癌的患者參與此項研究。


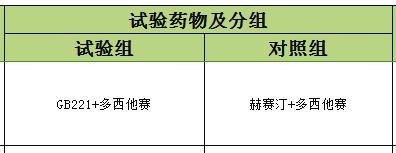
參加本研究,有機會獲得A、B方案治療
A:注射用重組抗HER-2(表皮生長因子受體2)人源化單克隆抗體(簡稱GB221)聯合多西他賽。GB221是針對HER-2(表皮生長因子受體2)受體的乳腺癌分子靶向治療藥物,臨床前研究證實,GB221與已上市同類藥物赫賽汀在蛋白結構、理化特性和凍融穩定性方面具有相似性,具有明顯的體內外抗腫瘤作用,安全性良好。 多西他賽是治療晚期乳腺癌的經典化療藥物;
B:赫賽汀聯合多西他賽
註:參加本研究,獲得A方案或者B方案的治療概率各50%
主要參加條件:
1. 年齡滿18周歲的女性患者;
2. 經病理學或組織學診斷為晚期乳腺癌,且至少有一個可測量的靶病灶,CT掃描(電腦斷層掃描)≥10 毫米;
3. HER-2(人類表皮生長因子受體2)陽性;
4. 目前不適合手術/放療;
5. 既往未接受過針對晚期乳腺癌的全身性治療;
6. 紫杉類藥物治療停止已至少6個月;
提示:以上為主要參加標準,最終入組情況以項目醫生為準。
醫生將根據您的具體情況,進一步確認是否符合本研究的篩選條件。經過檢查等確認符合所有指標者,將接受以上A方案或B方案治療及治療後的安全性隨訪。該研究將為您免費提供研究藥物(GB221/赫賽汀和多西他賽),並免除研究中規定的檢查費。
以下為正在開展的中心列表:
浙江省腫瘤醫院
海南省人民醫院
安徽省腫瘤醫院
徐州市中心醫院
安徽省立醫院
瀋陽軍區總醫院
北京大學腫瘤醫院
四川大學華西醫院
武漢市中心醫院
北京大學首鋼醫院
復旦大學附屬腫瘤醫院
汕頭大學醫學院附屬腫瘤醫院
廣西壯族自治區人民醫院
哈爾濱醫科大學附屬腫瘤醫院
點擊下方【了解更多】進入報名頁