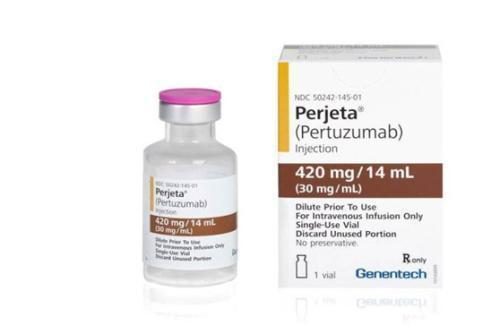
今天,國家藥品監督管理局批準帕妥珠單抗注射液(英文名:Pertuzumab Injection)進口註冊申請,聯合曲妥珠單抗(赫賽汀)和化療用於具有高複發風險的人表皮生長因子受體2(HER2)陽性早期乳腺癌患者的輔助治療。
乳腺癌是女性發病率最高的惡性腫瘤。
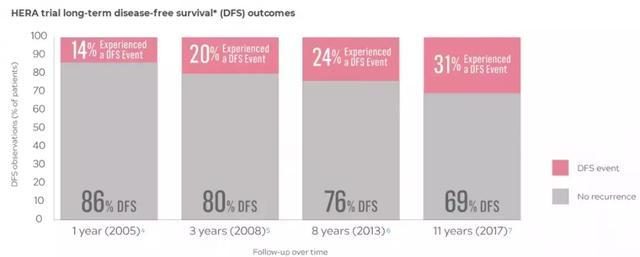
HER2陽性的早期乳腺癌患者接受赫賽汀聯合化療後,仍有約1/4的患者在10-11年後出現疾病複發或死亡,高危早期乳腺癌患者出現複發或死亡的比例更高。
帕妥珠單抗注射液為羅氏公司研發的一種新型抗HER2藥物,通過抑製HER2異源性和同源性二聚體產生抗HER2作用。
全球關鍵III期輔助治療研究顯示,與當前標準治療曲妥珠單抗聯合化療相比,帕妥珠單抗聯合曲妥珠單抗和化療用於具有高複發風險的HER2陽性早期乳腺癌患者輔助治療,顯著改善了患者無侵襲性疾病生存期(見下圖),不良反應可控。

鑒於本品臨床效益/風險優勢明顯,12月17日,國家藥品監督管理局批準本品進口註冊,與曲妥珠單抗和化療聯合用於具有高複發風險的HER2陽性早期乳腺癌患者的輔助治療。
根據一項名為APHINITY研究的3期臨床研究顯示,與當前標準治療曲妥珠單抗聯合化療相比,使用帕妥珠單抗聯合曲妥珠單抗和化療用於具有高複發風險的HER2陽性早期乳腺癌患者輔助治療,複發風險降低23%。
另外根據CLEOPATRA實驗顯示,對於晚期HER-2陽性乳腺癌患者,相比標準一線治療方案(使用曲妥珠單抗聯合化療),使用帕托珠單抗聯合曲妥珠單抗+化療。可以延長患者總生存期到56.5個月,接近5年。

「帕妥珠單抗+曲妥珠單抗(赫賽汀)+化療」聯合療法目前也已成為HER-2陽性乳腺癌患者的臨床治療金標準,已經在全球超75個國家獲批。
中國是乳腺癌高發國家,HER-2 陽性乳腺癌患者數量約佔全部乳腺癌的 20% 左右。據國家癌症中心數據統計,2014年中國女性乳腺癌新增病例27.89萬例。
在進口抗癌藥零關稅、國家組織進行腫瘤葯醫保談判、多個大陸曲妥珠單抗類似物接近申報上市的大背景下,帕妥珠單抗的獲批上市無疑會給中國乳腺癌患者提供更豐富的治療選擇。
這也意味中國HER-2陽性乳腺癌患者的治療基本與世界同步。
我們將持續關注新葯的資訊,藥物價格、入醫保、贈葯計劃如果出爐,會第一時間告知大家,請大家持續關注。
參考文獻
http://www.nmpa.gov.cn/WS04/CL2056/333925.html