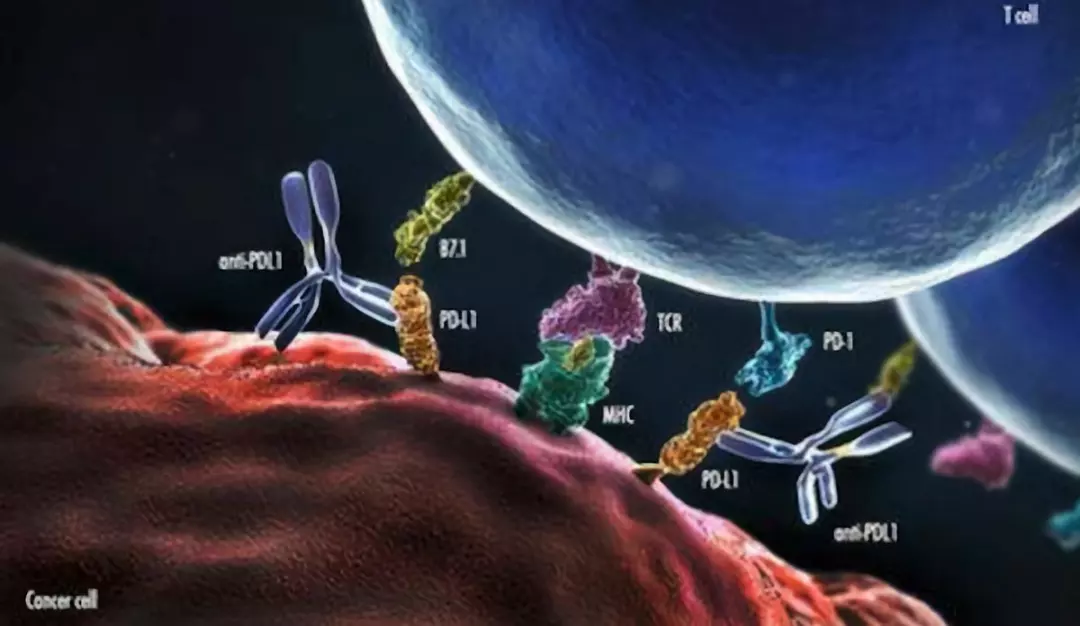
腫瘤免疫通過多個過程進行,其由抗原呈遞細胞(APC)的抗原呈遞組成,以教育效應細胞和效應細胞毒性細胞的破壞。然而,腫瘤免疫通常在腫瘤部位受到抑製。惡性轉化的細胞很少能夠在免疫系統的攻擊中存活下來,但存活的細胞會改變其表型以降低其免疫原性。
由此產生的細胞逃避免疫系統的攻擊並形成臨床上可辨別的腫瘤。腫瘤微環境同時含有多種免疫抑製分子和細胞以抑製腫瘤免疫。此外,肝臟微環境表現出免疫耐受性,通過門靜脈減少對大量暴露抗原的異常免疫反應,免疫功能障礙常與肝硬化有關,肝硬化在肝細胞癌(HCC)患者中廣泛存在。免疫療法旨在減少腫瘤負擔,但也有望預防非癌性肝臟病變進展為HCC,因為HCC發展或複發來自慢性炎癥狀態和/或肝硬化的非癌性肝臟病變,這些病變無法治癒和/或通過局部和/或全身治療根除。然而,癌症免疫療法應該通過使用兩種不同的措施來增強特異性腫瘤免疫:增強效應細胞功能,例如APC的抗原呈遞能力和細胞毒性細胞的腫瘤細胞殺傷能力,以及在免疫抑製性腫瘤微環境中重新激活免疫系統。
肝細胞癌(HCC)被列為第六大常見惡性腫瘤,是全球癌症相關死亡的第三大原因。儘管最近在預防和診斷方面取得了進展,但許多HCC病例仍然處於晚期診斷階段,因此很少有效和/或治癒性治療選擇,因此,他們的預後仍然很差。這些情況需要開發一種新的HCC治療策略,特別是晚期HCC。

HCC由慢性肝病引起,特別是肝硬化,由各種危險因素引起,包括慢性乙型肝炎或C病毒感染,黃曲霉毒素B1暴露,過量飲酒和非酒精性脂肪肝的發生。其他獨立的風險因素包括煙草使用,糖尿病和肥胖。隨著HBV和HCV感染髮病率的下降,非酒精性脂肪性肝病正在成為發達經濟體HCC的重要原因,因為這些國家患有代謝綜合征的患者數量正在迅速增加。
所有這些病因都引起持續的炎症反應,包括持續的氧化應激,持續的肝細胞壞死和再生,以及纖維化改變。這些事件可以通過在各種載客和驅動基因中積累體細胞遺傳改變和表觀遺傳修飾而導致HCC發展,並且隨著新一代測序技術的出現,這些變化已被廣泛闡明。在大約70%的HCC病例中觀察到異常端粒酶逆轉錄酶(TERT)激活,這是由其啟動子突變和擴增以及病毒基因組整合引起的。因此,TERT激活和隨後的端粒酶再激活可能是惡性轉化的關鍵事件,導致HCC細胞無限制增殖。在CTNB1(約30%)中也經常觀察到失活突變,其編碼β-連環蛋白。
此外,在WNT途徑的其他成員中檢測到失活突變,例如AXIN1(11%),AXIN2(1%),ZNRF3(3%)或APC(1%)。在HCC中也經常觀察到TP53的失活突變(~30%的病例),但很少與CNTB1一起檢測到突變,表明不同的分子途徑是HCC進化的原因。在涉及其他途徑的基因中觀察到另外的突變,包括染色質重塑,PI3K / AKT /哺乳動物雷帕黴素靶蛋白(mTOR)信號傳導,Ras / MAPK信號傳導,JAK / STAT信號傳導和氧化應激途徑。
在1p,4p-q,6q,8p,13p-q,16p-q,17p,21p-q,22q的廣泛基因組缺失中也經常觀察到DNA拷貝數改變,並且在1q,5p,6p,8q處獲得, 17Q,20Q,Xq的複發性同源缺失涉及各種基因,包括AXIN1,CDKN2A / CDKN2B,CFH,IRF2,MAP2K3,PTEN,RB1和RPS6KA3 。相反,更廣泛的DNA增益影響JAK3,MET和MYC,而11q13和6p21的焦點擴增導致擴增FGF3 / 4/19 / CCDN1和VEGFA。FGF19的局灶性擴增與腫瘤進展相關,而VEGFA的焦點擴增對索拉非尼(晚期HCC的一線治療)具有高度敏感性。

即使肝臟中沒有纖維化改變,大部分HBV感染的患者也會發生HCC,這表明HBV可以直接致癌。基於其體外調節細胞周期,信號通路和肝細胞DNA修復的能力,非結構性HBV蛋白HBx蛋白被提出作為致癌基因,但HBx直接轉化活性的證據很少。 。與其他DNA病毒一樣,HBV可引起插入突變,它可以在整合位點誘導DNA缺失,從而促進染色體不穩定和腫瘤抑製基因的失活。此外,將HBV基因組整合到具有增強子和啟動子活性的基因座中可以調節整合位點附近基因的表達和功能,並最終促進克隆增殖和惡性轉化。因此,整合位點的差異可以深刻地影響受影響基因的類型和隨後的分子病理變化。
隨著基因技術的出現,尤其是新一代測序技術,HCC分子變化的知識迅速擴大,但尚未有效地轉化為臨床實踐。一個主要原因是突變的驅動基因和相關途徑的類型在每種HCC情況下顯著不同。這些異質性可能阻礙靶分子的鑒定和/或選擇以產生分子靶向藥物。免疫療法可以克服這個問題,因為它可以增強宿主細胞的抗腫瘤活性,而不管肝癌發生中涉及的分子和信號途徑如何。在這篇綜述中,我們將討論HCC免疫治療的現狀和未來前景。HCC的其他臨床方麵包括藥物治療已在其他幾篇近期文章中進行了綜述。
已經提出各種免疫治療方式以根除或減少腫瘤負荷和/或在成功去除HCC患者中的原發性腫瘤後預防複發。如本文所討論的,已經從臨床前和/或I期臨床試驗獲得了有希望的結果,以評估HCC患者的各種類型的免疫療法。然而,迄今為止,只有使用抗PD-1抗體的免疫檢查點治療在II期臨床試驗中產生了有利的結果,並且這些結果需要在大規模RCT中進行驗證。
過繼免疫細胞療法在臨床應用於HCC治療之前有幾個難以克服的障礙。第一個涉及用於過繼轉移的細胞群的製備。目前,細胞製備尚未標準化,因此難以比較不同研究團隊報告的結果。此外,一些論文描述了從不符合良好生產規範(GMP)條件的條件下製備的細胞群獲得的結果。因此,應以標準化方式並在GMP條件下製備細胞以用於大規模RCT。

免疫療法固有的問題是它可以長期穩定疾病狀態而不減少腫瘤負荷,與化學療法和/或放射療法施加的效果相反。此外,HCC免疫治療的一個目標是在成功的局部和區域治療後預防腫瘤複發。因此,從與用於評估化學治療劑不同的觀點來看,絕對有必要設計一種評估HCC免疫治療的措施。
免疫功能障礙可以在癌症患者中以多種水準出現,包括抑製的抗原呈遞,降低的效應T細胞功能和免疫抑製性腫瘤微環境,因此,這些結果表明存在於個體癌症患者中的免疫抑製的不同機制。這些異質性可以解釋有限比例的患者中單一類型的免疫療法的功效。因此,幾種不同方式的組合可以協同增強免疫治療的有效性,未來的研究應該探索這一點。或者,這一發現可能源於幾種不同的患者隊列的存在,這些隊列對特定的免疫療法有不同的反應。如果是這樣,
總的來說,HCC的免疫治療仍處於起步階段。然而,大多數HCC可以從非癌性肝臟部分的慢性炎症性病變和/或肝硬化中重複發生,並且複發對HCC患者的長期預後有很大影響。然而,這些病變根本不能通過其他療法消除,只有免疫療法可以防止這些非癌組織進展為HCC。因此,絕對有必要擴大HCC的免疫療法以預防HCC複發,並最終改善HCC患者的預後。想了解更多相關信息可以關注領募。