不想錯過界哥的推送?


來源丨醫學界腫瘤頻道
作為侵襲性最強的一類肺癌,小細胞肺癌(SCLC)一直是老大難,治療進展幾十年鮮有突破,主要依賴放化療。
令人欣喜的是,近年來,SCLC領域也逐漸傳出好消息,尤其是今年9月下旬於世界肺癌大會(WCLC)公布的IMpower133研究,更是在一線治療取得重大進展,引起國內外專家廣泛關注!
適逢11月肺癌關注月,作為SCLC特刊,「醫學界」特別採訪了吉林省腫瘤醫院院長程穎教授,請她梳理下近年來SCLC領域的大事件、新進展。
1. 近期SCLC中有什麼較大的治療突破嗎?包括治療手段上的突破和治療線數上的突破,可否請您詳細談談?程穎教授:2018年,對於SCLC來說具有裡程碑式的意義,在免疫治療和靶向治療領域都取得了很大的進步,改寫了SCLC的治療指南和策略。
免疫治療是近幾年非常熱的研究領域,並且改變了包括NSCLC在內多個腫瘤的治療策略,在SCLC肺癌領域也開展了一些研究。
其中CheckMate 032研究是SCLC免疫治療現有結果中樣本量最大的研究,該研究比較了Nivolumab單葯,不同劑量的Nivolumab聯合Ipilimumab方案對複發SCLC的療效,研究分為非隨機隊列和隨機隊列。2015年ASCO上首次公布研究結果,2016年於Lancet Oncol在線發表,隨後在2017年WCLC上公布了CheckMate 032研究中關於腫瘤突變負荷(TMB)與療效的探索性分析結果,並發表在2018年Cancer Cell上。
研究發現:
-
在非選擇的患者中,SCLC能夠從免疫治療中取得持久獲益,尤其是聯合治療獲益更明顯。
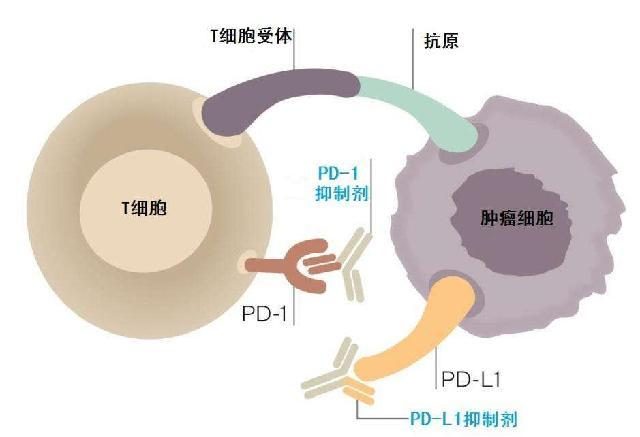
在標誌物的分析中,PD-L1表達不能預測Nivolumab±Ipilimumab治療療效;TMB的狀態與Nivolumab±Ipilimumab療效相關,高TMB的患者有更高的客觀緩解率(ORR),獲得無進展生存期(PFS)、總生存期(OS)的改善,尤其是聯合治療組。
研究認為在高TMB的SCLC患者免疫聯合治療有最大的臨床獲益,TMB是SCLC免疫治療潛在的標誌物。正是基於CheckMate 032研究的結果,2017年NCCN指南將Nivolumab±Ipilimumab作為複發SCLC治療新推薦,2018年8月FDA也基於這項研究批準Nivolumab三線治療複發SCLC,改寫了SCLC近20年來沒有新葯突破的窘境。
除了Nivolumab以外,另外一種PD-1抗體Pembrolizumab也在SCLC的後線治療中進行了探索,今年在ASCO會議上公布的Keynote158結果顯示:
Pembrolizumab在晚期SCLC尤其是PD-1陽性患者具有良好抗腫瘤活性和持久的應答。
基於該研究結果在10月10日剛剛發布的2019年第一版NCCN SCLC指南中,將Pembrolizumab作為一線治療後六個月內複發、PS 0-2分SCLC患者二線治療的2A類推薦。
除了後線治療,免疫治療在SCLC的一線治療中也取得了重大突破,在9月末剛剛結束的WCLC會議上,公布了IMpower133研究的結果。這是一項Atezolizumab聯合化療對比安慰劑聯合化療一線治療廣泛期SCLC的3期研究。
研究結果顯示:
-
Atezolizumab聯合EC方案,較單純應用EC方案治療,中位OS延長了2個月,達到了12.3個月;1年的OS率達到了51.7%,是單純化療組的1.3倍;
-
而中位PFS也從4.3個月延長至5.2個月,1年的PFS率更是單純化療組的2.5倍,達到了12.6%;
並且毒性反應可耐受。
這一研究使得Atezolizumab成為廣泛期SCLC一線治療近20年來首個取得OS改善的藥物。目前藥物上市申請已經遞交了FDA,並即將遞交EMA,2019年第一版NCCN也根據該研究的結果,將Atezolizumab+化療作為廣泛期SCLC一線治療的1類優選推薦。
除了免疫治療,靶向治療也是今年來的研究熱點。
在今年的WCLC會議上,我代表研究團隊報導了我國自主研發多靶點小分子TKI安羅替尼對比安慰劑三線及以上治療SCLC的2期研究——ALTER1202臨床研究結果,旨在對比安羅替尼與安慰劑三線及以上治療SCLC患者的療效及安全性。
研究結果表明:
-
安羅替尼組的中位PFS是安慰劑組的近6倍,達到了4.1個月,而安慰劑組僅為0.7個月,疾病進展風險下降了81%;
-
儘管兩組患者ORR沒有明顯差異,但安羅替尼組的疾病控制率是安慰劑組的5倍,達到了71.6%;
-
雖然目前OS成熟度僅為40%,但我們也觀察到了安羅替尼組的OS較安慰劑組延長了2個半月;
除了療效外,治療相關AE均安全可控。
ALTER 1202研究告訴我們安羅替尼可以改變SCLC三線及後線治療沒有藥物可用的困境,且口服方便,耐受性好,對於複發難治SCLC的後線治療意義重大。
2. IMpower133研究的成功是否有望改變SCLC的標準治療模式?
程穎教授:SCLC一線治療的模式在近20年裡均無明顯改變,而IMpower 133研究的成功,毋庸置疑在SCLC一線治療的歷史上畫上了濃墨重彩的一筆。
但在關注療效的同時,我們也要注意,在這個精準醫學時代,到底什麼樣的患者真正的能從維持治療中獲益,有沒有一個確切的生物標誌物指導治療?患者的獲益是在化療聯合免疫治療階段,還是在應用免疫治療的維持階段?最終患者是否可獲得生存獲益?相對於EP方案的廉價,EP+免疫治療後應用免疫維持治療,治療成本昂貴,藥物經濟學是否合適?這些問題也是在我們改變SCLC治療模式時必須要考慮的問題。
3. 您認為SCLC治療未來研究的大方向和發展趨勢是怎樣的?免疫治療會扮演其中一個重要角色嗎?
程穎教授:SCLC未來的主流研究方向主要有以下幾方面。
首先就是目前研究最多並且最炙手可熱的免疫治療,在SCLC的研究中同樣是研究的熱點,並且扮演著重要的角色。
既往免疫治療在SCLC中開展的研究多為二線或三線及以上,總共有十幾項研究,並且樣本量均較少。隨著今年WCLC報導了IMpower133的研究結果,免疫治療在SCLC的一線治療取得突破,且也開展TMB和PD-L1等免疫治療的生物標誌物的探索,Checkmate系列臨床研究多選用TMB為預測標誌物,而Keynote系列研究則選用PD-L1的表達水準,但無論TMB和PD-L1,對預測SCLC的治療療效均非常重要。
除了免疫檢查點抑製劑以外,還有兩種針對DLL3的新型的免疫治療藥物AMG757和AMG119正在進行臨床研究。
SCLC領域相對比較關注的第二個藥物就是Rova-T,DLL3作為Notch信號通路的配體之一,其在SCLC的表達率可以高達80%以上。既往的研究結果告訴我們,對於DLL3高表達的患者,尤其是緩解以後的患者,應用Rova-T治療可以使患者獲得超過7個月的OS,這相比於其他二線治療藥物所取得的療效是一個大幅的提高。
目前這個藥物正在開展維持治療和二線治療的研究,我們中國也參與了這些研究,正在招募患者中。
另外一個在SCLC開展的熱門靶向藥物——PARP抑製劑,在SCLC中的研究仍然處於早期階段。開展臨床研究的PARP抑製劑主要有Talazoparib、Veliparib、Olaparib,Niraparib,研究多為Ⅰ/Ⅱ期研究,未選擇人群,探索性研究發現SLFN11高表達的患者接受PARP抑製劑聯合化療治療OS更長。
除了靶向藥物外,化療藥物也有一些新葯正在SCLC領域進行探索。今年ASCO會議報導的海洋生物中提取物Lurbinectedin,研究結果顯示,在61例可評估療效患者中,ORR 40%左右,疾病控制率超過70%,中位OS將近1年。
基於此結果美國FDA已經於今年批準了該葯的孤兒葯資格,目前一項在全球範圍開展的隨機III期試驗ATLANTIS正在進行,期待結果公布。
專家簡介


程穎 教授
吉林省腫瘤醫院院長
吉林省腫瘤研究所所長
吉林省抗癌協會理事會理事長
吉林省肺癌診療中心主任
中國臨床腫瘤學會(CSCO) 副理事長
CSCO小細胞肺癌專業委員會主任委員
CSCO非小細胞肺癌專業委員會副主任委員
中國抗癌協會肺癌專業委員會副主任委員
中國抗癌協會腫瘤臨床化療專業委員會副主任委員
中華醫學會腫瘤學分會委員
全國醫師定期考核腫瘤專業編輯專業委員會副主任委員
國家衛生、計生委常見腫瘤規範化診療專家組成員
中國醫師協會肺癌培訓專業委員會副主任委員
吉林省醫師協會腫瘤醫師分會主任委員
吉林省醫學會腫瘤專業委員會主任委員
擔任《中華腫瘤雜誌》等多家雜誌編委。