卵巢癌是女性生殖器官常見的三大惡性腫瘤之一,發病率僅次於子宮頸癌和子宮內膜癌而位居第3位。據全國癌症登記中心數據顯示2015年中國大陸卵巢癌新發人數5.2萬例,死亡2.3萬例。但70%卵巢癌在初次就診時已是晚期,5 年生存率僅25%~30%。
卵巢癌和BRCA基因突變
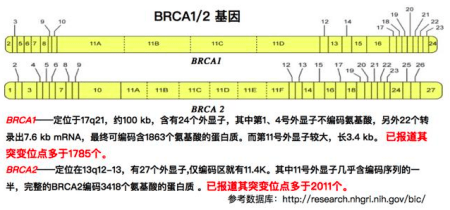
卵巢癌患者中5%~10%為遺傳性,遺傳性卵巢癌患者中有90%左右為乳腺癌易感基因(BRCA)的突變,為常染色體顯性遺傳。
普通人群中,卵巢癌和乳腺癌的發病率分別為(5~10)/10 萬和(30~80)/10 萬。高危人群如有乳腺癌和卵巢癌病史或家族史的婦女攜帶BRCA基因突變概率相對普通人群明顯增加。而攜帶BRCA1或BRCA2基因突變的婦女,卵巢癌的終身發病風險分別為39%和11%,乳腺癌分別為65%和45%;同時,其他腫瘤的發病風險也成倍增高(包括男性突變攜帶者),如攝護腺癌、男性乳腺癌、胰腺癌以及黑色素瘤等。對於已有乳腺癌且攜帶BRCA1或BRCA2基因突變的婦女,其10年內發生卵巢癌的風險分別為12.7%、6.8%。
中國首個多中心卵巢癌患者BRCA突變研究數據顯示,我國卵巢癌患者中28.45%存在BRCA突變。攜帶BRCA1或BRCA2基因突變的患者體內的腫瘤攜帶著特定的DNA修復缺陷,因此對PARP抑製劑尤其敏感。

PARP抑製劑臨床招募卵巢癌患者
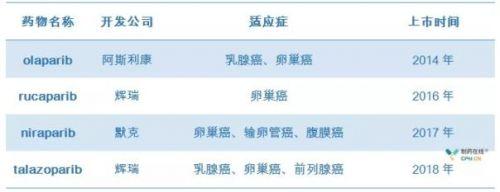
奧拉帕利在國內的成功上市也標誌著卵巢癌治療開始進入PARP抑製劑時代!雖然國內沒有獲批的PARP抑製劑。但國內諸多生物技術和製藥企業已經在PARP抑製劑研發和臨床治療方面取得了不少新的突破。像百濟神州旗下處於臨床階段的藥物BGB-290,是一種針對PARP1和PARP2的分子靶向、口服、強效且高度選擇性的抑製劑。
BGB-290在選擇性、DNA捕獲活性、口服生物利用度和腦組織穿透性方面可區別於其它PARP抑製劑,包括目前唯一獲得美國FDA和歐洲EMA許可的PARP抑製劑olaparib。
BGB-290Ⅱ、Ⅲ的臨床試驗已經通過了國家食品藥品監督管理總局和倫理委員會的批準。目前國內多家醫院正在為這項研究招募患者。
BGB-290用於鉑敏感的複發性卵巢癌患者III期研究的主要入選標準:
1.年齡≥18歲的女性。
2.組織學確診的高級別漿液性或子宮內膜樣卵巢癌(包括原發性腹膜癌和輸卵管癌)。
3.患者必須既往曾接受≥2線含鉑類藥物的治療方案。
a. 對於在研究入組之前的倒數第二線含鉑類藥物的治療方案:對鉑類藥物敏感,定義為在最後一次鉑類藥物給葯後超過6個月發生疾病進展。
b.對於在研究入組之前的最後一線含鉑類藥物的化療:患者必須完成≥4個周期含鉑類藥物的治療方案 。最後一線含鉑類藥物的治療方案不含貝伐珠單抗。
4.可以在最後一次鉑類藥物給葯後≤8周內完成隨機入組。
提示:以上為主要參加標準,最終入組情況以項目醫生為準。

BGB-290在中國晚期卵巢癌、輸卵管癌和原發性腹膜癌患者的II期單臂臨床研究的主要入選標準:
1、組織學或細胞學確診的卵巢癌、輸卵管癌、或原發性腹膜癌
2、攜有種系BRCA1/2突變且符合高級別(G2或G3級子宮內膜樣上皮癌亦可)上皮性、漿液性、透明細胞性卵巢癌(包括輸卵管癌或原發性腹膜癌)患者;
3、患者患有局部晚期或轉移性腫瘤,必須曾接受至少兩線化療後出現疾病進展
4、對鉑類藥物敏感,或對鉑類藥物耐葯的患者(以患者最後一次鉑類用藥是否大於6個月來定義藥物敏感或耐葯)
5、患者既往不能用過PARP抑製劑
6、 ECOG≤1
註:以上為主要入排標準,具體標準將依據研究方案由研究者評估
我們希望,國內PARP抑製劑藥物能儘早上市,為卵巢癌患者提供更多的治癒機會!
如果您想報名本項目或者想了解其他臨床招募項目可以關注微信公眾號「募海棠」。