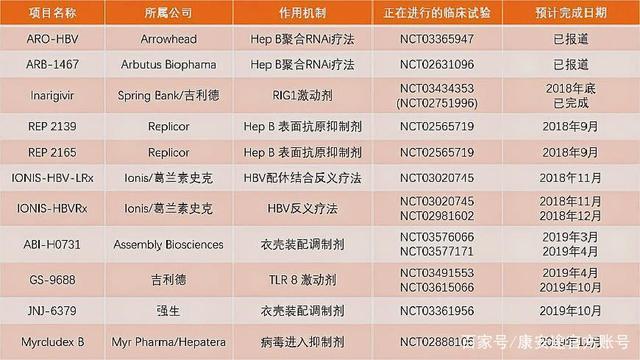
歌禮生物製藥公司的PD-L1單克隆抗體ASC22,正在國內對慢性B肝患者(CHB)積極開展臨床研究,這是一種採用皮下注射的PD-L1抗體,旨在實現功能性治愈HBV。歌禮公司最新公告顯示,ASC22獲得美國食品藥品監督管理局(FDA)批準新藥研究申請(IND),將在美國國內展開對慢性B肝患者的臨床試驗。
來自:歌禮製藥最新公告

B肝在研新藥ASC22,FDA批準新藥IND申請,將在美國開展臨床研究
一、2b期積極進展,已發表在2021美肝大會
早在2021年的美國肝病研究年會上,研究人員就發表過和ASC22相關的臨床研究積極數據。一項在我國國內開展的隨機、單盲、安慰劑對照、多中心的2b期臨床試驗(臨床試驗編號:NCT04465890),在149名慢B肝受試者中評估24周 1mg/kg 或 2.5mg/kg ASC22或匹配安慰劑每周一次(Q2W)與核苷(酸)類似物(NAs)聯合給藥的安全性與有效性。
這項國內2b期研究中期結果表明,在基線B肝表面抗原(HBsAg)水準≤500 IU/mL的受試者中,治療組中約19%(3/16)的受試者獲得B肝表面抗原清除,而安慰劑組中沒有受試者獲得表面抗原清除,並且在ASC22停藥後未見反彈,這部分受試者顯示出已經功能性治愈。
根據歌禮最新公告介紹,用於功能性治愈HBV的ASC22 2a期臨床試驗和2b期試驗,還入選了2021年美肝會最佳摘要。入選最佳摘要也說明,美肝會審查委員會對歌禮製藥在慢B肝功能性治愈方面研究的高度評價。
來自歌禮B肝新藥研發管道,可見PD-L1抗體ASC22正處在IIb期

二、科學家點評
作用機理方面,ASC22是一款新型B肝免疫候選藥物,能夠通過阻斷PD-1/PD-L1通路來實現功能性治愈HBV,即B肝表面抗原清除。來自歌禮製藥創始人、董事長兼首席執行官吳勁梓博士點評ASC22獲得FDA批準在美國開展治療B肝的臨床研究:ASC22(恩沃利單抗,Envafolimab)獲得美國FDA批準IND臨床試驗申請,使我們能夠在美國和全球開展旨在實現功能性治愈HBV的臨床試驗,同時,我們期待與慢性B肝功能性治愈領域的行業領導者合作。
在美國約有159萬慢性B肝患者,這款在研的皮下注射PD-L1抗體ASC22獲批IND,同樣對於美國慢B肝患者有益。

三、核心梳理
小番健康結語:2021年美國肝病年會上,歌禮的ASC22臨床試驗進展已入選了年會最佳摘要,ASC22是一種新型免疫在研藥物,原理上可通過阻斷PD-1/PD-L1通路來實現功能性治愈HBV。來自2021年美肝會已發表的研究進展顯示,在治療組中的16名受試者中的3名,實現了B肝表面抗原清除,並且在最後一次給藥後,這3名受試者的B肝表面抗原依然維持陰性,即表面抗原持續清除。
值得一提的是,ASC22治療組實現的約19%(3/16)B肝表面抗原清除率相較於現有療法(NAs或IFN)還是有大幅提高的。也希望有更多我國科研人員研發的在研創新藥物進入臨床研究。目前,ASC22在國內的臨床研究進度是2b期,在美國即將開展臨床研究。返回搜狐,查看更多
責任編輯: