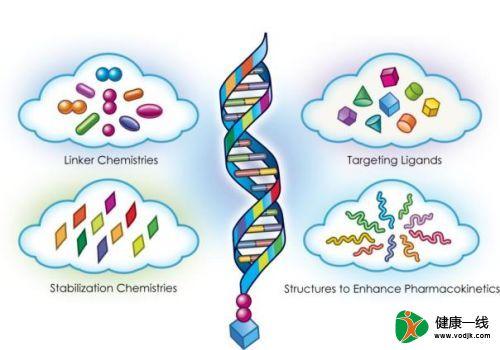
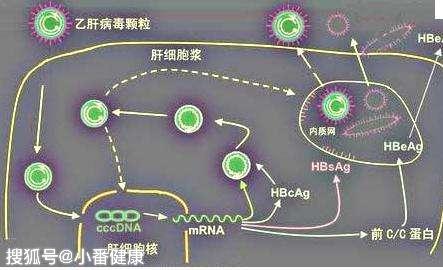
反義寡核苷酸(ASO),是全球科學家基於開發B肝在研新藥重要方向之一。ASO是短的合成核酸片段,可以特異性結合靶RNA序列以形成DNA:RNA雜交體(用於反義DNA)或RNA:RNA雙鏈體(用於反義RNA)。

B肝ASO對比RNAi,作用機制相近,GSK兩種候選藥物已進入II期
這主要可能通過核糖體阻斷,以阻止逆轉錄或翻譯,或者誘導RNA:DNA雜交體的RNase H介導的RNA切割。反義寡核苷酸最初是在1990年被應用於抗B肝病毒方面,全球已有許多關於ASO在基因療法方向的研究,支持其在HBV領域藥物開發的潛在作用。一些研究指出,靶向非編碼序列(比如包裝和聚腺苷酸化信號)的反義寡核苷酸,還可以有效抵抗HBV複製。
反義寡核苷酸應用於B肝藥物開發,主要面臨的問題是,不穩定性、細胞內傳遞效率低下、對靶標親和力不足和與反義寡核苷酸相關毒性等。一些研究已經提供富有建設性進展,如ASO可輕鬆在鹼基、磷酸二酯基和糖上進行修飾,用於增加對靶標的穩定性、溶解性、特異性和親和力。磷酸骨架最常被修飾的目標是,通過使用硫原子(硫代磷酸酯)或甲基(甲基膦酸酯)取代一個氧原子。

全球已有通過連接寡核苷酸的2'O原子和4'C原子,把核糖環鎖定的反義鎖定核酸(LNA)已成功用於HBV,沒有發現毒性證據。磷酸二酰胺嗎啉代寡聚物(PMO)是DNA樣的ASO,其脫氧核糖被六元嗎啉代環取代,磷酸二酯鍵被不帶電的磷酸二氨基酯鍵取代,都顯示出優越的性能,一些PMO已經進入臨床試驗階段。
載體和靶向部分(例如陽離子脂質體和膽固醇),已有被科學家成功地用於提高抗HBV ASO的細胞攝取。在鴨子HBV(DHBV)模型當中,基於聚乙烯亞胺的反義寡核苷酸遞送,可導致病毒血症顯著下降,並伴隨著肝內HBVDNA、RNA、核心抗原和表面抗原水準降低。通過將ASOs與配體連接,以進行受體識別,進而靶向肝細胞可以促進受體介導的內吞作用攝取,並顯著抑製B肝病毒複製。

目前,全球基於反義寡核苷酸(ASO)正在開發B肝在研新藥的主要有Ionis公司和葛蘭素史克公司合作開發的GSK836(IIa期)和GSK404(II期),Aligos Therapeutics 公司的ALG-020572和ALG-001075(臨床前研究)等。ALG-020572和ALG-001075是Aligos公司的ASO候選藥物,在今年第30屆亞太肝髒研究協會(APASL)年會上,該公司展示了4項研究進展:

作為該公司ASO候選藥物,非臨床研究中在慢性B肝患者中評估了上述兩種研究藥物的安全性和有效性,結果表明,相比同類反義寡核苷酸(ASO),ALG-020572和ALG-001075表現出更高優勢。從藥物作用機理上,ASO主要通過和HBV的mRNA結合,進而阻止轉變為病毒蛋白,起到抑製HBV複製作用。因此,反義寡核苷酸與RNAi療法,都屬於基因新療法,後續上述研究藥物如有進展,小番健康將繼續跟進(以上研究藥物未上市,正在進行臨床試驗以評估其安全性和有效性)。返回搜狐,查看更多
責任編輯: