指南與共識
慢性胰腺炎診治指南(2018,廣州)
中國醫師協會胰腺病專業委員會慢性胰腺炎專委會
期刊來源:中華胰腺病雜誌,
2018,18(5): 289-296
慢性胰腺炎是一種遷延不愈的難治性疾病,因癥狀頑固,需終身治療,嚴重影響患者生活品質,大大地加重了社會的公共醫療負擔。近年來,慢性胰腺炎在全球發病率不斷上升,病因機制和診療方式不斷更新,日本、美國和歐洲相繼頒發了臨床診療指南。中國醫師協會胰腺病專業委員會慢性胰腺炎專委會牽頭組織消化內科、膽胰外科、內分泌科、影像科和病理科等多學科專家,依據最新循證醫學證據和國內外最新研究結果,參照多部國際慢性胰腺炎指南,對我國2012年版《慢性胰腺炎診治指南》進行了修訂。
一
定義及術語
慢性胰腺炎(chronic pancreatitis, CP):CP是一種由遺傳、環境等因素引起的胰腺組織進行性慢性炎症性疾病,其病理特徵為胰腺腺泡萎縮、破壞和間質纖維化。臨床以反覆發作的上腹部疼痛和胰腺內、外分泌功能不全為主要表現,可伴有胰管結石、胰腺實質鈣化、胰管狹窄、胰管不規則擴張、胰腺假性囊腫形成等。
酒精性慢性胰腺炎(alcoholic chronic pancreatitis, ACP):CP患者平均乙醇攝入量男性超過80 g/d、女性超過60 g/d,持續2年或以上,且排除其他病因。
複發性急性胰腺炎(recurrent acute pancreatitis, RAP):患者至少有兩次急性胰腺炎發作史,緩解期無胰腺組織或功能異常改變,是一種特殊類型的胰腺炎。
遺傳性慢性胰腺炎:CP患者家族中,在兩代或以上的親屬中,存在至少2個一級親屬或至少3個二級親屬患CP或者RAP。
特發性慢性胰腺炎:指排除任何已知病因的CP患者。
脂肪瀉:患者大便內排出過多的脂肪,又稱油花樣腹瀉, 72 h糞便脂肪收集試驗測定大便脂肪含量超過7 g/d。
3c型糖尿病:是一種繼發於胰腺疾病的糖尿病,又稱胰源性糖尿病,常發生在CP患者中。
二
流行病學及病因
在全球範圍內,CP的發病率為9.62/10萬,死亡率為0.09/10萬,CP患者中以男性為主,其數量約為女性的2倍;美國成人CP發病率為24.7/10萬,患病率為91.9/10萬;日本CP發病率為14/10萬,患病率為52/10萬;印度CP的患病率最高,達到125/10萬;我國2003年CP患病率約為13/10萬,呈逐年增長的趨勢。
CP致病因素多樣,由遺傳、環境和(或)其他致病因素共同引起。酗酒是CP主要的致病因素之一,在西方國家及日本佔50%~60%,在我國約佔20%。目前認為遺傳因素在CP發病中起重要作用,常見易感基因包括PRSS1、SPINK1、CTRC和CFTR等。遺傳性慢性胰腺炎為常染色體顯性遺傳,外顯率為80%,主要突變位於PRSS1基因。我國特發性慢性胰腺炎主要致病突變為SPINK1 c.194+2T>C。此外,CP致病因素還包括高脂血症、高鈣血症、胰腺先天性解剖異常、胰腺外傷或手術、自身免疫性疾病等,吸煙是CP獨立的危險因素。RAP是形成CP的高危因素,約1/3的RAP患者最終演變為CP。
三
診斷標準及分型分期
(一)癥狀
腹痛是CP最常見的臨床癥狀,常為上腹部疼痛,可向腰背部放射。腹痛可分為兩型:A型為間歇性腹痛,包括急性胰腺炎以及間斷髮作的疼痛,疼痛發作間歇期無不適癥狀,可持續數月至數年;B型為持續性腹痛,表現為長期連續的疼痛和(或)頻繁的疼痛加重。我國CP患者中A型腹痛佔80%以上,B型腹痛佔5%,約10%的患者無腹痛癥狀。
胰腺外分泌功能不全早期可無任何臨床癥狀,後期可出現體重減輕、營養不良、脂肪瀉等,我國CP患者脂肪瀉發生率為22.9%。胰腺內分泌功能不全可表現為糖耐量異常或者糖尿病,我國CP患者糖尿病發生率為28.3%。CP可出現胰腺假性囊腫、膽總管狹窄、十二指腸梗阻、胰瘺、胰源性門靜脈高壓、胰源性胸腹水、假性動脈瘤等併發症。診斷CP後,隨訪8年有1.3%的患者可進展為胰腺癌。
(二)體征
上腹部壓痛,急性發作時可有腹膜刺激征。由於消化吸收功能障礙可導致消瘦、營養不良,青少年患者可影響發育。當並發巨大胰腺假性囊腫時,腹部可捫及包塊。當胰頭顯著纖維化或假性囊腫壓迫膽總管下段時,可出現黃疸。
(三)影像學檢查
1.X線:部分患者可見胰腺區域的鈣化灶、陽性結石影(圖1)。
2.腹部超聲:可見胰腺區伴聲影的高回聲病灶、胰管形態變化等。因其敏感度不高,僅作為CP的初篩檢查。此外,對於假性囊腫等CP併發症具有一定的診斷意義。
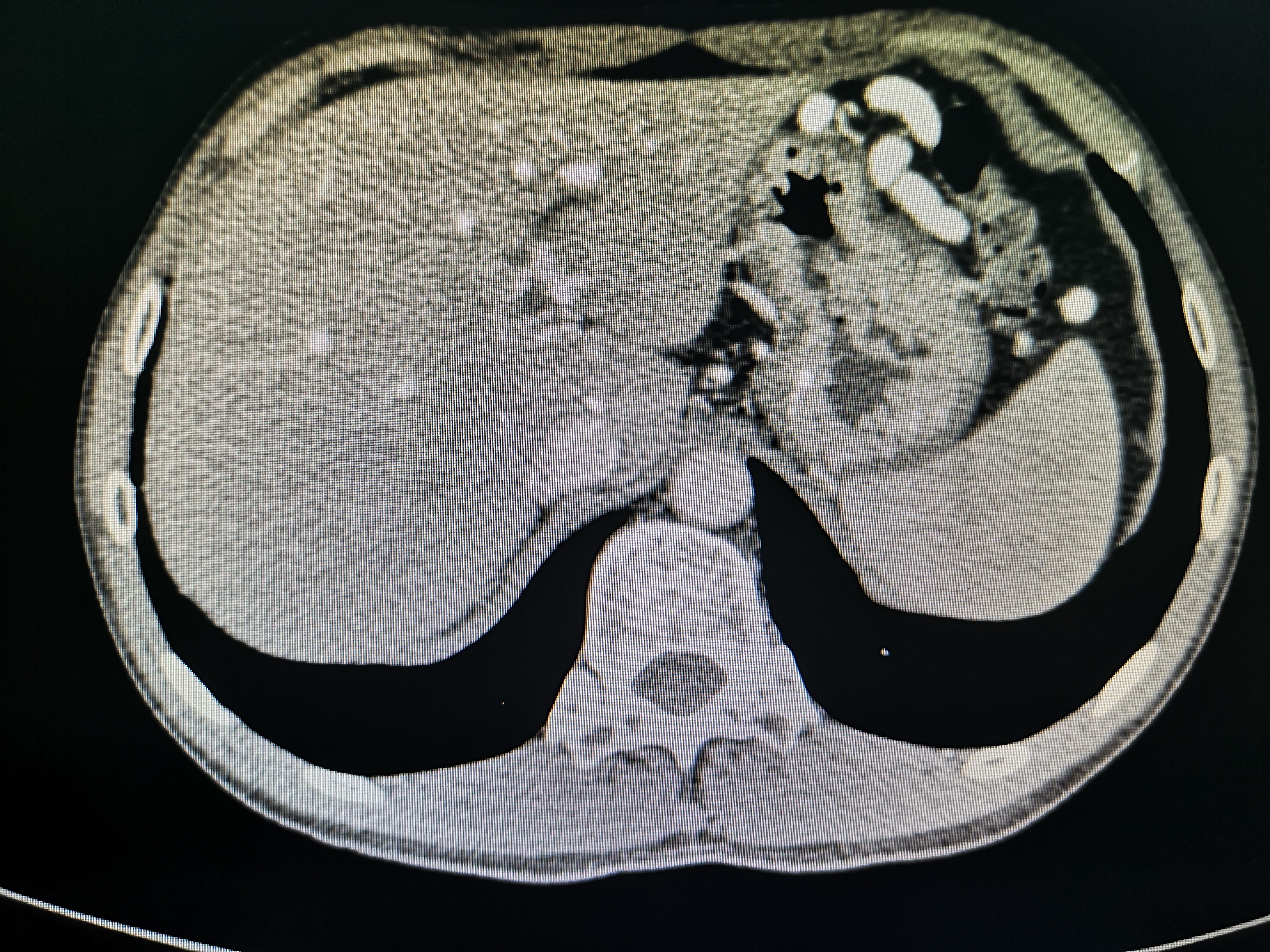
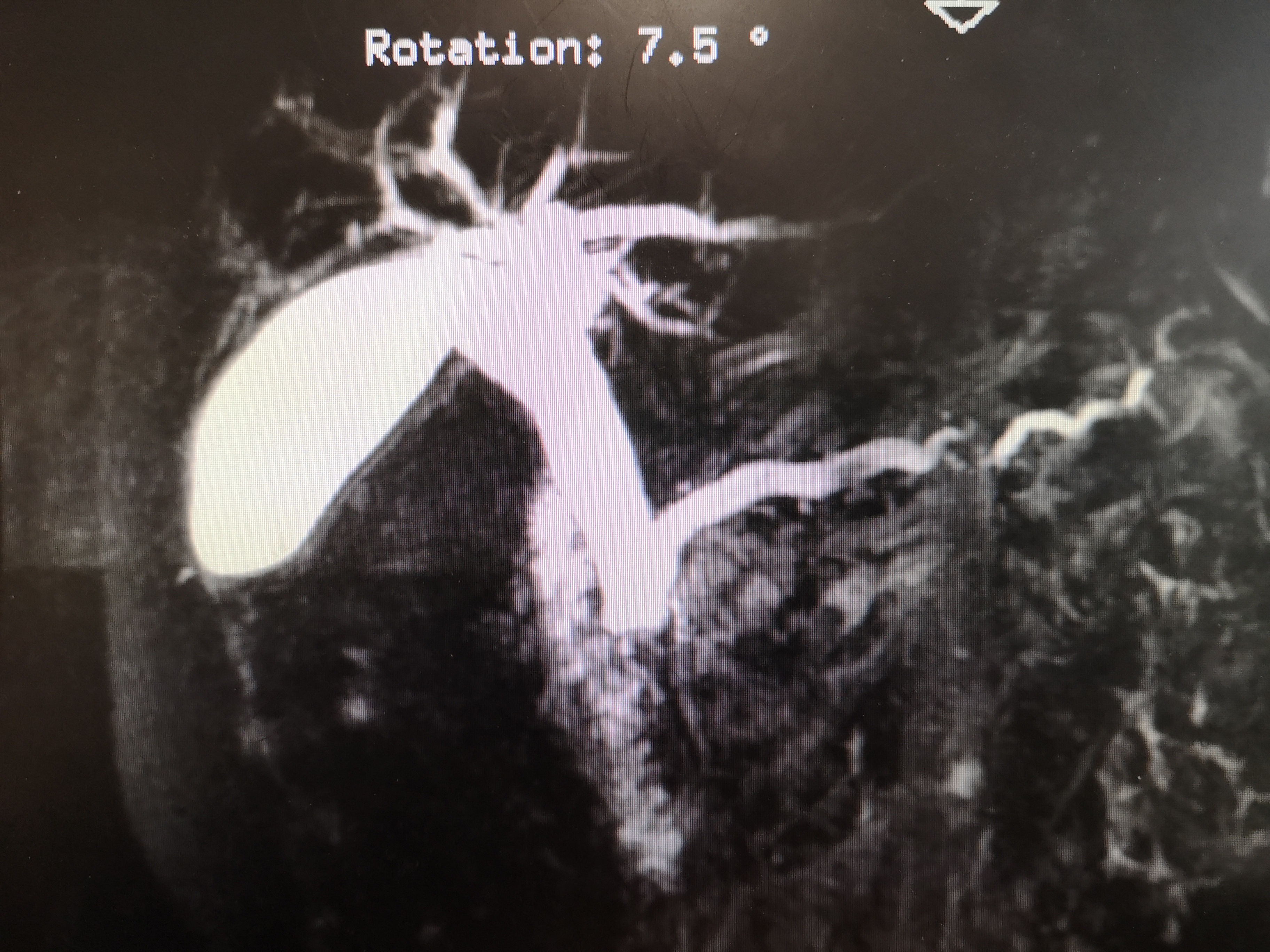
3.電腦斷層掃描(CT)、磁共振成像(MRI)、磁共振膽胰管成像(MRCP):CT檢查的典型表現為胰腺鈣化、胰管擴張、胰腺萎縮,其診斷的敏感度及特異度分別為80%、90%以上。CT是顯示胰腺鈣化的最優方法(圖2),平掃CT檢查可顯示胰腺微小鈣化灶。常規MRI掃描對CP的診斷價值與CT相似,對胰腺實質改變檢測敏感,但對鈣化和結石的顯示不如CT。MRCP主要用於檢查膽、胰管的病變,如主胰管擴張、胰腺先天變異、膽管擴張或狹窄等(圖3)。
4.內鏡超聲(EUS):主要表現為胰腺實質異常及胰管異常,如胰管結石或胰腺鈣化、胰管狹窄、胰管擴張等(圖4)。EUS診斷CP的敏感度高,對早期CP的診斷具有優勢。EUS引導下的細針穿刺抽吸活檢(EUS-FNA)主要用於腫塊型CP與胰腺癌的鑒別。
5.內鏡下逆行膽胰管造影(ERCP):是診斷CP的重要依據,但因其為有創性檢查,目前僅在診斷困難或需要治療操作時選用。依據劍橋分型,CP可分為輕度:分支胰管病變(超過3個),主胰管正常;中度:主胰管病變,伴或不伴分支胰管病變;重度:主胰管阻塞、嚴重不規則擴張、結石,有假性囊腫形成 (圖5)。ERCP術中組織及細胞學檢查有助於鑒別膽管狹窄的良惡性。

圖1 腹部平片示胰腺多髮結石

圖2 上腹部CT示胰腺多髮結石

圖3 MRCP示主胰管擴張,可見多發充盈缺損影

圖4 EUS示胰頭部胰管內見兩枚強回聲,伴後方聲影

圖5 示主胰管不規則擴張
(四)實驗室檢查
1.胰腺外分泌功能檢測:包括直接和間接試驗。直接試驗是評估胰腺外分泌功能最敏感、最特異的方法,但因成本高,屬侵入性檢查,臨床應用受限。間接試驗包括糞便檢測、呼氣試驗、尿液試驗和血液檢測,其敏感度和特異度相對不足,常用的檢測方法有糞便彈性蛋白酶-1檢測、13C混合三醯甘油呼氣試驗(13C-MTG-BT)。胰泌素刺激MRCP可通過十二指腸充盈程度對胰腺外分泌功能進行半定量分級評估。
2.胰腺內分泌功能檢測:糖尿病的診斷標準為空腹血糖(FPG)≥7.0mmol/L或隨機血糖≥11.1mmol/L或口服葡萄糖耐量試驗(OGTT)2 h血糖≥11.1mmol/L。尚未診斷糖尿病的CP患者建議每年進行1次血糖檢測。3c型糖尿病患者胰島β細胞自身抗體陰性,胰多肽基線水準下降,存在胰腺外分泌疾病,可與其他類型糖尿病相鑒別。
3.基因檢測:重點對於特發性、青少年(起病年齡低於20歲)以及有胰腺疾病家族史的CP患者,可行基因檢測,以CP患者外周靜脈血DNA為樣本,針對我國CP相關基因,如PRSS1、SPINK1、CTRC、CFTR等進行基因測序分析。
4.其他實驗室檢查:急性發作期可見血清澱粉酶升高,如合併胸、腹水,胸、腹水中的澱粉酶含量往往明顯升高。血鈣、血脂、甲狀旁腺素、病毒、IgG4等檢查有利於明確病因。CP也可出現血清CA19-9增高,如明顯升高,應警惕合併胰腺癌的可能。脂溶性維生素、血清白蛋白、前白蛋白、鎂、視黃醇結合蛋白等指標有助於判斷機體營養狀況。
(五)胰腺病理組織檢查
胰腺活檢方法主要包括CT或腹部超聲引導下經皮胰腺穿刺活檢、EUS-FNA以及通過外科手術進行的胰腺活檢。由於活檢屬有創檢查,且CP具有特徵性的影像學表現,目前不常規應用,主要用於CP與胰腺癌的鑒別診斷。
CP的基本組織學改變為胰腺腺泡組織的減少和纖維化。纖維化包括小葉間、小葉旁纖維化,或合併小葉內纖維化,可能伴隨胰腺組織的慢性炎症浸潤,胰管擴張等。根據其組織病理改變,CP可分為慢性鈣化性胰腺炎、慢性阻塞性胰腺炎和慢性炎症性胰腺炎。慢性鈣化性胰腺炎最多見,表現為散發性間質纖維化及胰管內蛋白栓子、結石形成及胰管損傷。慢性阻塞性胰腺炎因主胰管局部阻塞、胰管狹窄致近端擴張和腺泡細胞萎縮,由纖維組織取代。慢性炎症性胰腺炎主要表現為胰腺組織纖維化和萎縮及單核細胞浸潤。當出現併發症時,也可見胰腺外器官的病理變化,如膽道梗阻、門靜脈受壓、血栓形成等。
(六)診斷標準與流程
1.診斷標準
主要診斷依據:(1)影像學典型表現;(2)組織學典型表現。次要診斷依據:(1)反覆發作上腹部疼痛;(2)血澱粉酶異常;(3)胰腺外分泌功能不全表現;(4)胰腺內分泌功能不全表現;(5)基因檢測發現明確致病突變;(6)大量飲酒史(達到ACP標準)。
主要診斷依據滿足1項即可確診;影像學或者組織學呈現不典型表現,同時次要診斷依據至少滿足2項亦可確診(表1)。
2.診斷流程詳見圖6。


圖6 CP診斷流程圖
(七)臨床分期
根據CP的疾病病程和臨床表現進行分期(表2),對治療方案選擇具有指導意義。臨床上也可根據胰腺功能是否出現不全表現,分為代償期和失代償期。

四
治療及預後
CP的治療原則為祛除病因、控制癥狀、改善胰腺功能、治療併發症和提高生活品質等。
(一)一般治療
CP患者須禁酒、戒煙,避免過量高脂、高蛋白飲食,適當運動。
(二)內科治療
1.急性發作期治療:治療原則同急性胰腺炎。
2.胰腺外分泌功能不全的治療:主要應用外源性胰酶替代治療(pancreatic enzyme replacement therapy,PERT)。首選含高活性脂肪酶的腸溶包衣胰酶製劑,於餐中服用。療效不佳時可加服質子泵抑製劑(PPI)、H2受體拮抗劑(H2RA)等抑酸劑。營養不良的治療以合理膳食+PERT為主,癥狀不緩解時可考慮補充中鏈三醯甘油。脂溶性維生素缺乏時可適當補充維生素D,尚無臨床循證證據推薦補充維生素A、E、K。
3.糖尿病的治療:改善生活方式,合理飲食。懷疑存在胰島素抵抗的患者,排除禁忌後可選用二甲雙胍治療,其他口服降糖藥物不良反應顯著,不做首選;口服藥物效果不佳時改為胰島素治療。對於合併嚴重營養不良患者,首選胰島素治療。由於CP合併糖尿病患者對胰島素較敏感,應注意預防低血糖的發生。
4.疼痛的治療:
(1)一般治療:禁酒、戒煙、控制飲食。
(2)藥物治療:胰酶製劑、抗氧化劑及生長抑素對疼痛緩解可能有效。止痛藥:治療遵循WHO提出的疼痛三階梯治療原則,止痛藥物選擇由弱到強,盡量口服給葯。第一階梯治療首選對乙醯氨基酚,其消化道不良反應較非甾體類抗炎葯的發生率低;第二階梯治療可選用弱阿片類鎮痛葯如曲馬多;第三階梯治療選用強阿片類鎮痛葯,但應注意腸麻醉綜合征的發生,隨著藥物劑量增加,約6%的患者發展成痛覺過敏、腹痛程度加重。
(3)因胰管狹窄、胰管結石等引起的梗阻性疼痛,可行內鏡介入治療。其他介入治療方法如CT、EUS引導下的腹腔神經阻滯術等,短期疼痛緩解率約50%,但其遠期止痛效果不佳,併發症發生率較高,目前開展較少。
(4)內科及介入治療無效時可考慮手術治療。對於部分有疼痛癥狀並伴有主胰管擴張的CP患者,在中長期疼痛緩解方面,手術優於內鏡治療。
(三)內鏡介入治療
CP內鏡介入治療的主要適應證為胰管結石、胰管狹窄、胰腺假性囊腫、膽管狹窄等,有利於緩解胰源性疼痛,改善患者生活品質。
1.主胰管梗阻的治療:CP可根據主胰管是否通暢分為主胰管梗阻型與非主胰管梗阻型。主胰管梗阻通常由胰管狹窄、胰管結石、胰管解剖異常等因素導致。對於疼痛伴主胰管梗阻的患者,內鏡治療可有效緩解癥狀。通過內鏡治療解除梗阻後,CP患者疼痛完全緩解或部分緩解率可達71%及24%。內鏡治療是解決CP梗阻性疼痛的首選方法。內鏡治療後,臨床上宜評估6~8周,如果療效不滿意,可考慮手術治療。
(1)胰管結石的治療:胰管結石根據X射線可否透過分為陽性結石與陰性結石,可單獨或多發存在,主要分布於胰頭部。對於體積較小的主胰管結石,ERCP可成功完成引流。對於>5 mm的主胰管陽性結石,首選體外震波碎石術(ESWL)治療,碎石成功後可再行ERCP取石,ESWL+ERCP的主胰管結石完全清除率達70%以上,主胰管引流率達90%。與ESWL聯合ERCP治療相比,單純ESWL治療可能也獲得理想的結石清除及疼痛緩解。ESWL術後併發症主要包括胰腺炎、出血、石街、穿孔、感染等,發生率約為6%,大多數經內科保守治療可痊癒。(2)主胰管狹窄的治療:治療原則為解除狹窄,充分引流胰液。ERCP胰管支架置入是最主要的治療方法,輔以胰管括約肌切開,狹窄擴張等操作,疼痛緩解率可達70%以上。治療首選置入單根胰管塑料支架,可定期或根據患者癥狀更換支架,支架通常留置6~12個月。如10 Fr支架留置12個月狹窄未改善,可考慮置入多根塑料支架或全覆膜自膨式金屬支架。ERCP治療時,對於主胰管嚴重狹窄或扭曲,導致反覆插管不成功者,可以嘗試經副乳頭插管;對於ERCP操作失敗者,可採用EUS引導下胰管引流術(EUS-PD),該技術難度大、風險高,僅推薦在有豐富內鏡經驗的部門開展。
2.CP繼發膽總管狹窄的治療:CP合併良性膽總管狹窄的發生率約為15%,其中約半數患者會出現相應癥狀。當膽總管狹窄合併膽管炎、梗阻性黃疸或持續1個月以上的膽汁淤積時,可行ERCP下膽道支架置入治療。置入多根塑料支架者可定期或根據癥狀更換支架,治療周期常為12個月,其長期有效率與膽道自膨式覆膜金屬支架相仿,均為90%左右,明顯優於置入單根膽道塑料支架。
3.胰腺假性囊腫的治療:當胰腺假性囊腫引起不適癥狀、出現併發症(感染、出血、破裂)或持續增大時,應予以治療。我國CP假性囊腫的發生率約為18%,男性風險高於女性。對於無併發症的胰腺假性囊腫,內鏡治療成功率達70%~90%,效果與手術相當,是首選的治療方法。對於與主胰管相通的、位於胰頭或體部的小體積(
4.青少年CP的內鏡治療:青少年CP患者多以腹痛起病,糖尿病、脂肪瀉、膽管狹窄等相關併發症發生率低。內鏡治療(ERCP、ESWL)可有效緩解腹痛、減少胰腺炎的發生,有效率達50%~70%。內鏡治療的併發症主要為術後急性胰腺炎,其發生率與成人相仿。內鏡治療青少年CP是安全有效的。
(四)外科手術治療
1.手術指征:(1)保守治療或者內鏡微創治療不能緩解的頑固性疼痛;(2)並發膽道梗阻、十二指腸梗阻、胰腺假性囊腫、胰源性門靜脈高壓伴出血、胰瘺、胰源性腹水、假性動脈瘤等,不適於內科及內鏡介入治療或治療無效者;(3)懷疑惡變者;(4)多次內鏡微創治療失敗者。
2.手術方式:遵循個體化治療原則,根據病因、胰管、胰腺及胰周臟器病變特點、手術者經驗、併發症等因素進行術式選擇。主要包括胰腺切除術、胰管引流術及聯合術式三類。
(1)胰腺切除術:標準胰十二指腸切除術(PD)或保留幽門胰十二指腸切除術(PPPD)適用於胰頭部炎性腫塊伴胰膽管及十二指腸梗阻、不能排除惡性病變、胰頭分支胰管多發性結石者。胰體尾切除術適用於炎性病變、主胰管狹窄或胰管結石集中於胰體尾部者;中段胰腺切除術適用於胰腺頸體部局限性炎性包塊,胰頭組織基本正常,胰尾部病變系胰體部炎性病變導致的梗阻性改變者;全胰切除術適用於全胰炎性改變、胰管擴張不明顯或多發分支胰管結石、其他切除術式不能緩解疼痛者,有條件的中心推薦同時行自體胰島移植,以保留患者內分泌功能。
(2)胰管引流術:該手術最大限度保留胰腺的功能,主要為胰管空腸側側吻合術,適用於主胰管擴張、主胰管結石、胰頭部無炎性腫塊者。
(3)聯合術式:指在保留十二指腸和膽道完整性基礎上,切除胰頭部病變組織,解除胰管及膽管的梗阻,同時附加胰管引流的手術。主要手術方法有Beger術及其改良式、Frey術、Izbicki術(改良 Frey術)及Berne術。Beger術又名保留十二指腸的胰頭切除術(DPPHR),主要適用於胰頭增大的CP患者。該術式與PD或PPPD相比,術後併發症及患者生活品質改善程度相當。Frey術適用於胰頭腫塊較小且合併胰體尾部胰管擴張伴結石的患者,胰頭切除範圍較前者小,有局部複發和減壓引流不充分的可能性。Izbicki術較Frey手術胰頭切除範圍大,包含鉤突中央部分,同時沿胰管長軸「V」形切除部分腹側胰腺組織,可以做到主胰管和副胰管的引流,引流效果較好。Berne術切除部分胰頭組織,確保膽管和胰管引流,保留背側部分胰腺組織,不切斷胰腺。該術式相對簡單,嚴重併發症較少,住院時間短,在緩解疼痛、保留胰腺內、外分泌功能等方面與Beger術相似。
(五)CP的治療流程
CP的治療是內科、外科、消化內鏡、麻醉及營養等多學科的綜合治療,治療流程詳見圖7。建議採取內科藥物體外震波碎石內鏡介入外科手術的(MedicineESWLEndotherapySurgery,MEES)階梯治療模式。

圖7 CP的治療流程
(六)預後及隨訪
CP是一種進行性疾病,部分患者病情相對穩定,持續進展者可發生內、外分泌功能不全或胰腺癌,應定期隨訪,通過實驗室檢查、CT/MRI檢查、問卷調查等方式,對患者胰腺內外分泌功能、營養狀況、生活品質等進行評估。此外,鑒於腫塊型CP與胰腺癌鑒別困難、且為胰腺癌的高危因素時,建議3個月隨訪1次,行腫瘤指標、影像學等檢查;若未見明顯異常,可適當延長隨訪時間。
參加本指南修訂的專家(按姓氏筆畫排序):
王偉(上海交通大學醫學院附屬瑞金醫院胰腺中心)、王華(安徽醫科大學肝病研究所)、王錚(西安交通大學第一附屬醫院肝膽外科)、王琳(空軍軍醫大學西京醫院普外科)、王鵬(復旦大學附屬腫瘤醫院中西醫介入科)、王立生(深圳市人民醫院消化內科)、王巨集光(吉林市人民醫院消化內科)、王單松(復旦大學附屬中山醫院胰腺外科)、王春友(華中科技大學附屬協和醫院胰腺外科)、王修齊(河南省人民醫院消化內科)、車在前(上海交通大學瑞金醫院急診科)、白辰光(海軍軍醫大學附屬長海醫院病理科)、白雪莉(浙江大學附屬第二醫院胰腺外科)、馮纓(中華消化雜誌編輯部)、呂芳萍(中華胰腺病雜誌編輯部)、朱克祥(蘭州大學第一醫院普通外科)、任旭(黑龍江省醫院消化內科)、任延剛(中國實用內科雜誌編輯部)、劉丕(南昌大學第一附屬醫院消化內科)、劉一品(濱州醫學院煙台附屬醫院消化內科)、劉立新(山西醫科大學第一醫院消化內科)、劉改芳(河北省人民醫院消化科)、劉傑民(貴州省人民醫院內鏡科)、許威(武警後勤學院附屬醫院消化內科)、許曉勇(安徽醫科大學第一附屬醫院消化內科)、孫昊(西安交通大學第一附屬醫院肝膽外科)、孫志廣(江蘇省第二中醫醫院消化內科)、杜奕奇(海軍軍醫大學附屬長海醫院消化內科)、李剛(海軍軍醫大學附屬長海醫院肝膽胰外科)、李強(黑龍江省醫院消化內科)、李鵬(首都醫科大學附屬北京友誼醫院消化分中心)、李靜(四川大學華西醫院消化內科)、李延青(山東大學齊魯醫院消化內科)、李兆申(海軍軍醫大學附屬長海醫院消化內科)、李啟勇(樹蘭(杭州)醫院肝膽外科)、李明陽(解放軍總醫院消化內科)、李曉斌(北京協和醫院普通外科)、李惠萍(溫州醫科大學附屬第一醫院胰腺炎診治中心)、楊紅(北京協和醫院消化內科)、楊雲生(中國人民解放軍總醫院消化內科)、楊妙芳(南京軍區總醫院消化內科)、楊建鋒(杭州市第一人民醫院消化內鏡)、楊智清(陸軍軍醫大學西南醫院肝膽外科)、肖斌(南京醫科大學第一附屬醫院膽胰中心)、吳浩(海軍軍醫大學附屬長海醫院消化內科)、吳晰(北京協和醫院消化內科)、吳國生(空軍軍醫大學西京醫院移植外科)、鄒文斌(海軍軍醫大學附屬長海醫院消化內科)、辛磊(海軍軍醫大學附屬長海醫院消化內科)、沈岩(浙江大學附屬第一醫院胰腺外科)、張紅(陝西中醫藥大學基礎醫學院病理生理學)、張波(復旦大學附屬腫瘤醫院胰腺外科)、張蕾(上海市第一人民醫院影像科)、張明剛(中日友好醫院消化內科)、張榮春(空軍軍醫大學西京醫院消化內科)、陸崬(福建醫科大學附屬第一醫院消化內科)、陸逢春(福建醫科大學附屬協和醫院胰腺外科)、阿依努爾·阿合曼(新疆維吾爾自治區人民醫院消化內科)、陳丹磊(海軍軍醫大學附屬長征醫院胰腺外科)、陳汝福(中山大學孫逸仙紀念醫院胰腺外科)、陳國棟(北京大學人民醫院消化內科)、邵卓(海軍軍醫大學附屬長海醫院胰腺外科)、邵成偉(海軍軍醫大學附屬長海醫院影像科)、邵曉冬(瀋陽軍區總醫院消化內科)、林青(中山大學孫逸仙紀念醫院胰腺外科)、旺加(西藏自治區人民醫院消化內科)、金鋼(海軍軍醫大學附屬長海醫院胰腺外科)、周小江(南昌大學第一附屬醫院消化內科)、周思思(青海省人民醫院消化內科)、郎韌(首都醫科大學朝陽醫院胰腺外科)、趙義軍(安徽醫科大學第一附屬醫院胰腺外科)、胡良皞(海軍軍醫大學附屬長海醫院消化內科)、賀奇彬(南京鼓樓醫院消化內科)、袁方(北京怡德醫院腎臟病科)、賈玉良(皖南醫學院弋磯山醫院消化內科)、黨彤(包頭醫學院第二附屬醫院消化內科)、殷濤(華中科技大學附屬協和醫院胰腺外科)、郭旭(解放軍總醫院消化內科)、郭濤(北京協和醫院消化內科)、唐才喜(中南大學湘雅醫學院株洲醫院肝膽外科)、唐湧進(中華消化內鏡雜誌編輯部)、黃力(中山大學附屬第一醫院膽胰外科)、黃李雅(寧夏醫科大學總院消化內科)、曹亞南(上海交通大學瑞金醫院內分泌科)、常曉燕(北京協和醫院病理科)、韓鈞凌(解放軍187醫院消化內科)、覃山羽(廣西醫科大學第一附屬醫院消化內科)、程禮(上海市第一人民醫院消化內科)、雷宇峰(山西省煤炭中心醫院消化內科)、蔡建庭(浙江大學醫學院附屬第二醫院消化內科)、蔡振寨(溫州醫科大學附屬第二醫院消化內科)、廖專(海軍軍醫大學附屬長海醫院消化內科)、譚向龍(解放軍總醫院肝膽外二科)、顏廷梅(中國實用內科雜誌編輯部)
主要起草者:鄒文斌、吳浩、胡良皞、任旭、金鋼、王錚
原創: 慢性胰腺炎專委會
來源:胰腺病雜誌
攜手消化,天天乾貨!