核苷(酸)類似物(NAs),比如最早開發的拉米夫定,以及此後繼續被廣泛使用的恩替卡韋,在抑製部分HBV患者的逆轉錄方向均顯示出良好抗病毒作用,但耐藥性依舊是NA尚未解決的問題。

B肝NA藥物,解讀其抑製機理,ASC42對PBC臨床研究獲受理
B肝病毒是慢性肝病的病原體,不僅會增加LC發生風險,並且還會增加HCC發生風險。全球在B肝研究領域方向,還需要開發更高效和安全性的方法,而且還需要開發出更方便和準確地檢測HBV基因組複製的方法。
開發B肝新機制藥物固然很重要,但開發一種簡易高效,用於檢測HBV感染或基因組複製的方法,不但有助於開發抗HBV藥物,而且還有助於深入研究HBV複製機制。自美國科學家巴魯克布隆伯格發現B肝病毒之後,基於這一重要基礎研究發現,廣大臨床研究也對HBV病毒進行深入探索。

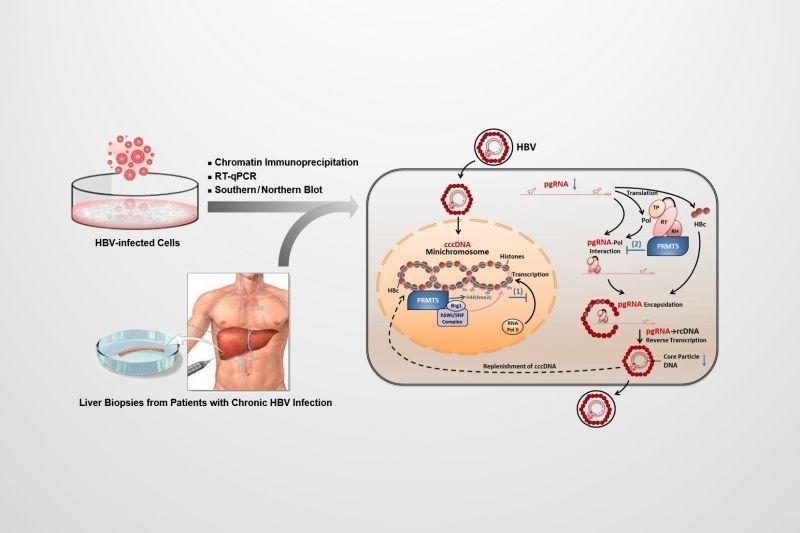
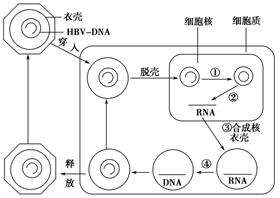
B肝病毒的粒子,包含著一個不完整的雙鏈DNA基因組,隨後在其生命周期中,在細胞核轉運站化成為共價閉合環狀DNA(cccDNA)。由於前基因組pgRNA是從cccDNA轉錄的,所以,細胞核中的cccDNA基因組非常穩定地存在,作為病毒複製模板來建立慢性HBV感染。這是在對B肝病毒這種DNA病毒進行大量的深入研究之後,得到的主要科學觀點,第一,cccDNA它非常穩定,第二,cccDNA它在細胞核裡面。
此外,B肝病毒的複製機制也很複雜,在一段時間,其複雜複製機制也在一定程度阻礙了全球B肝研究,而且科學界還缺乏在體外和體內檢測HBV基因組複製的方法。伴隨著口服核苷或核苷(酸)類似物(NA)的開發上市,NA也改變了全球對慢性B肝的認識和藥物治療格局,並且NA依然沿用至今,成為HBV藥物領域主力。

NAs作用機理,它們主要是通過靶向B肝病毒聚合酶(Pol),來抑製B肝病毒複製的。Pol催化前基因組RNA中間體的逆轉錄步驟,形成成熟、部分雙鏈、松弛的HBV環狀DNA基因組。正如此前小番健康科普的,B肝病毒還有一個由其病毒基因組的核形式、我們稱它為共價閉合環狀DNA(cccDNA)在內在穩定性特點,現有的NA藥物都不可能實現完全根除HBV;
NA藥物需要長期使用,才可以起到強效抑製HBV複製,而長期使用NA也會導致抗病毒耐藥性發生,所以,NA藥物開發一直在朝著選擇高耐藥屏障高特點方向進行研發,這也是建立在以往如拉米夫定、阿德福韋酯等低耐藥屏障抵抗特徵的長期研究,發現了NA藥物的主要風險。
導致對抗病毒藥物耐藥性源於B肝病毒遺傳變異,這種變異是在逆轉錄過程中,由於低保真HBV Pol固有地產生,導致受感染宿主內同時存在不同,但密切相關的病毒變體,一般定義為準種和隨後的選擇病毒突變體,這些病毒變異體對抗現在抗病毒藥物時,具有其複製優勢特點。也有越來越多的臨床科研人員認可這樣一種觀點,即宿主免疫反應在誘導清除慢性病毒感染背景下也是相關的,以此可作為開發B肝新藥的一個方向。

小番健康結語:歌禮製藥子公司甘萊製藥公司正在開發的ASC42,在原發性膽汁性膽管炎(PBC)患者的中國臨床試驗申請獲得受理。值得一提的是,ASC42是一種FXR激動劑,它已經先後在我國申請用於治療非酒精性脂肪性肝炎(NASH)、慢性B肝(CHB)和原發性膽汁性膽管炎(PBC)三種不同適應症的臨床試驗,可見其適應症較為廣泛。
從該公司藥物管線更新看,ASC42在NASH方向正處於1期,在CHB方向剛啟動2期(ASC42+干擾素+核苷類似物),最近ASC42對PBC的臨床研究申請獲得受理。返回搜狐,查看更多
責任編輯: