不想錯過每日推送?
戳上方藍字「醫學界呼吸頻道」關注我們
並點擊右上角「···」目錄,選擇「設為星標」


目前炙手可熱的免疫治療,是不是所有肺癌患者均能從中獲益呢?來聽聽韓寶惠教授怎麼說!
報導專家|韓寶惠教授 上海交通大學附屬胸科醫院
整理|Cosine
來源|醫學界呼吸頻道
在剛剛結束的2018世界肺癌大會上,免疫治療是不容忽視的新興力量。彷彿不談及免疫治療就是掉隊,就是落後。
不可否認,免疫治療目前已成為癌症治療中一顆冉冉升起的新星,而其中又以肺部腫瘤領域的進展最快。
11月30日,來自上海交通大學附屬胸科醫院的韓寶惠教授在上海中山肺癌論壇上為我們詳細解讀了「免疫治療在肺癌診治中的最新進展」,讓我們一起聆聽韓教授的精彩講解。


Fig 1:韓寶惠教授會議現場照片
對免疫治療的基本認識:找準漏洞、對症下藥
韓寶惠教授認為,我們首先要理解免疫治療,不單單是免疫檢查點、PD1、PDL1,還包含著細胞因子療法、T細胞和治療性疫苗。免疫檢查點、PD1、PDL1,僅是眾多免疫製劑中的一種。


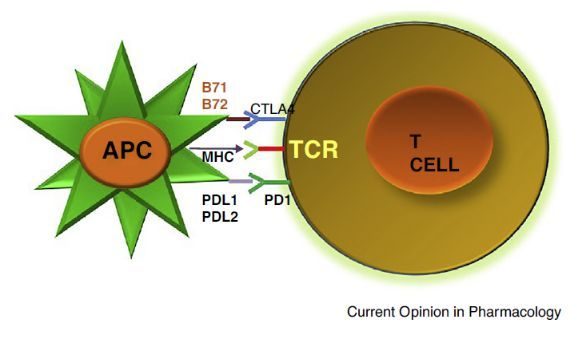
Fig 2. 人體內完整的免疫通路
其次,我們應該明確為什麼今天免疫治療取得了突破。
這是因為過去我們認為免疫治療應該強化免疫,但過去的事實已經證明這一思路是錯誤的、無效的。
目前的理念是:腫瘤是由於免疫有漏洞有缺陷而發生發展,免疫治療的目標應該是尋找存在的漏洞,而非強化免疫。
再次,我們應該理解免疫檢查點機制。免疫檢查點是免疫通路的剎車片,當它激活後就會抑製T細胞的作用,而當下大熱的免疫檢查點PD1、PDL1抑製劑就是抑製這一檢查點,從而釋放T細胞,恢復其功能。
基於上述內容,如今免疫治療在肺癌中取得成就,是因為我們發現了肺癌患者免疫的缺陷,即PDL1高表達而抑製T細胞作用,所以對症下藥,通過PD1、PDL1抑製劑彌補了這一缺陷,從而獲得非常好的療效。
所以我們要認識到,免疫治療要找準患者免疫缺陷的部分,然後研究彌補缺陷的方法,像精準醫學一樣,精準施治。而精準施治的前提就是精準判斷免疫缺陷的部位,只有這樣才能提高免疫治療的效率。從而把過去的「冷腫瘤」變成「熱腫瘤」,但是哪些患者的腫瘤可以發生這一轉變,則需要我們尋找生物標記物作為明確免疫缺陷的航標。


Fig 3. 目前已知的根據免疫表型和免疫缺陷的環節制定的治療性策略
當下的臨床研究,主要以下從五大方面推進了免疫治療在肺癌中的臨床實踐。

 播放GIF
播放GIF
方向一
驅動基因陰性非小細胞肺癌(NSCLC)患者中的進展:療效甚佳
目前中國肺癌患者中,三分之二的腫瘤都是驅動基因突變陰性,所以在這一領域的進展對於我國肺癌的臨床實踐有很大的指導意義。
目前,免疫治療的地位已經從二線方案上升為一線方案,運用方法由單葯使用拓展為聯合用藥。
一項關於單抗+化療與單一化療的臨床Meta分析[1]比對發現,免疫+化療的聯合方案可以使客觀緩解率(ORR)由單葯的23%提高到免疫聯合的61.4%,同時無進展生存率(PFS)和總生存率(OS)也有相應改善的趨勢。所以, 免疫聯合化療將會解決在驅動基因陰性的人群的問題。同時,一項研究分析發現[2],在組織多肽特異性抗原(TPS)>50%的NSCLC患者中,PDL1表達越高,患者使用免疫檢查點PDL1抑製劑發的療效越好,PDL1是一個可預測免疫治療持續獲益的生物標記物。另一項研究[3]也顯示,在PDL1高、中、低表達的三個亞組中,PDL1抑製劑均有療效,但PDL1低表達患者獲益的程度確實與高表達組有區別,證明了 PDL1的表達與PDL1抑製劑的療效具有線性正相關關係。這提示我們在一線、二線乃至後線治療中,想要達到更精準的治療,就要檢測患者的PDL1表達強度,從而提高治療效率,儘可能減少毒副反應。
方向二
驅動基因陽性NSCLC患者中的進展:免疫治療的療效有限
綜合一線、二線患者使用免疫治療的統計數據,客觀事實是:即使PDL1高表達的患者可以運用PDL1抑製劑進行治療,但療效仍有限。雖然今年有一項研究發現[4],免疫治療+厄洛替尼治療陽性突變患者的臨床療效不錯,但由於其樣本僅有20例,容量太小,仍需大樣本的研究進一步證實確認。方向三
局部晚期NSCLC患者中的進展:免疫治療前移
局部晚期NSCLC患者常規進行放化療後隨訪,當複發後再次進行治療。一項對放化療以後的患者進行的研究[5]發現,讓一組患者遵循常規服用安慰劑和隨訪,另一組則使用12個月的PD1單抗治療。單抗組的PFS和OS的結果很理想,能夠降低死亡總風險32%。這將可能改變IIIa期患者局部放化療後的臨床實踐活動,患者可以不必等待、觀察隨訪、複發後再治療,完全 可以在放化療後加用免疫治療,減少癌症的複發和轉移。

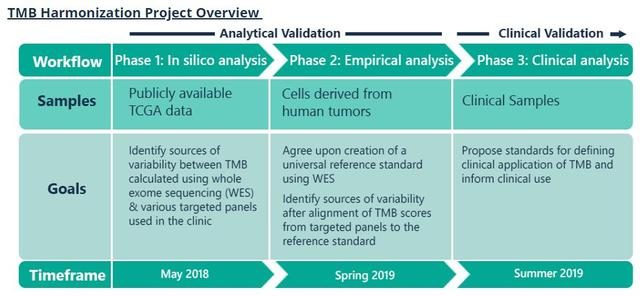
Fig 4. 針對局部晚期NSCLC患者研究的納入標準與具體分組
不過,韓教授也提及,這一研究同樣發現使用免疫治療1年肯定提高了毒副反應的發生,其中亞洲患者的肺炎發生率升高,這將在一定程度上限制了免疫療法的應用。我們在對患者使用免疫治療時,應特別注意免疫相關炎症的發生。
方向四
NSCLC患者早期新輔助治療
還有研究發現,免疫療法可進一步前移到患者實行手術前,和化療一起作為新輔助治療的一部分,同樣能獲得較好的療效。
方向五
在小細胞肺癌(SCLC)患者中的進展:有一定療效
在過去的30-40年中,SCLC患者的主力治療方案一直是化療,免疫治療徒勞無功。
但近來研究發現[6],標準化療+免疫藥物Atezolizumab能使患者的OS改善,從10.3個月的生存期延長到12.3個月,雖然ORR和PFS的結果仍為陰性。這說明,免疫治療在SCLC患者的維持、鞏固階段有效,但在初期階段療效不佳。由於Atezolizumab在NSCLC患者中有豐富經驗,故而其在SCLC患者中的毒副反應尚可控。聽了韓寶惠教授為我們解析的世界肺癌大會上關於免疫治療的進展,總結如下:
1.驅動基因陰性的晚期NSCLC:免疫治療成為主流;
2.驅動基因陽性的晚期NSCLC:療效有限,謹慎探索;
3.局部晚期NSCLC:大有前途,潛在新的治療模式;
4.NSCLC早期新輔助:免疫治療前移帶來生存優勢;
5.SCLC最新進展:免疫聯合成功但需努力。


肺小結節不「糾結」,葛棣教授教你如何選擇治療方案!


如何看待肺癌免疫治療的爭議與共識,陸舜教授這麼說……




參考文獻:
1.MK Doherty, et al. WCLC 2018.P1.01-16.
2.Aguilar EJ, et al. WCLC 2018, MA04.05.
3.Papadimitrakopoulou VA, et al. WCLC 2018, OA05.07.
4.Rudin CM, et al. WCLC 2018, MA15.02.
5.Anto年 SJ, et al. WCLC 2018, PL02.01.
6.Liu SV, et al. WCLC 2018, PL02.07.
重要!福利!來了!
快來參與下方海報內新葯認知調研
我們將隨機抽取20名醫生用戶
送2019《醫學界》專屬枱曆!
界友們請速速參與起來~