在現有調降B肝病毒新藥物開發策略中,已經被科學家探索到的包括先天免疫激動劑、干擾素刺激基因 (ISG)、siRNA/shRNA、小干擾RNA、單鏈寡核苷酸和末端核苷酸轉移酶等。我們先來談談先天免疫激動劑這個方向的藥物設計和開發。

B肝現有新機制,介紹設計思路,描述代表藥物開發難度
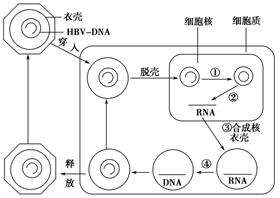
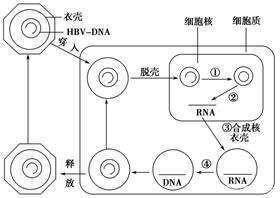
可以作為病原體相關分子模式之一,外源RNA能夠被先天免疫傳感器識別,例如TLR3(針對 dsRNA)、TLR7/8(對ssRNA)和RIG-I(對5'三磷酸 RNA)等。以美國吉利德科學公司的在研藥物TLR7激動劑GS-9620為例,在其臨床前土撥鼠WHV慢性感染和HBV黑猩猩模型研究中,GS-9620都表現出了持續顯著地降低感染模型的病毒載量。
但是,當GS-9620進入1b/2a期臨床試驗時,研究人員觀察到在慢B肝患者中,並沒能觀察到GS-9620對HBVDNA和B肝表面抗原(HBsAg)水準的顯著臨床變化。當沒有直接抗病毒活性的條件下,GS-9620可以誘導IFN-α、其他細胞因子和肝內T細胞和B細胞聚集體。

根據以往該方向已經公開披露的臨床開發數據來看,儘管在HBV領域所使用的新策略——先天免疫激動劑,可以增強HBV抗原呈遞,但整體免疫反應可能還不足以抵消慢B肝患者體內的B肝病毒複製。吉利德科學的科學家,曾經使用TLR8 激動劑GS-9688刺激的PBMC分離及培養模型,處理顯示GS-9688可促使原代肝細胞中病毒標記物減少。
SB 9200 (Iranigivir),是一種RIG-I/NOD2激動劑已被終止臨床開發。科學家發現,RIG-I對B肝病毒複製具有雙重作用。RIG-I可以感知HBV pgRNA的5' ε 區域,並誘導III型干擾素產生。還可以通過結合ε區域,RIG-I與病毒聚合酶之間競爭的相互作用,這也在實質上抑製了聚合酶介導的病毒衣殼化。

科學家也是基於以上對RIG-I的深入認識,進而將相關靶點藥物SB9200推進到臨床前動物模型研究中,結果表明,經過SB9200處理可以降低土撥鼠血清與肝髒的WHVDNA水準和肝內HBVRNA水準。
以上幾種是以往比較有代表性的針對HBV的先天免疫激動劑,有部分已經在臨床試驗過程中被終止開發。這種先天免疫調節劑主要受限的理由是在PBMC可以表現出更理想的反應,而並非是在受到感染的肝細胞中表現出更好的反應!激動劑所觸發的IFN-α和ISG,最後通過免疫調節機制調節肝細胞。

小番健康結語:先天免疫激動劑中的TLR7/8激動劑和RIG-I激動劑,已被廣泛應用HBV領域藥物開發。科學界以往發現,PBMC分泌的細胞因子,可能會導致肝髒中發生意料不到與潛在的破壞性免疫反應發生。這些都是當前針對先天免疫激動劑方向需要解決的問題,以上也能夠說明相關靶點藥物開發難度和基本設計思路。返回搜狐,查看更多
責任編輯: