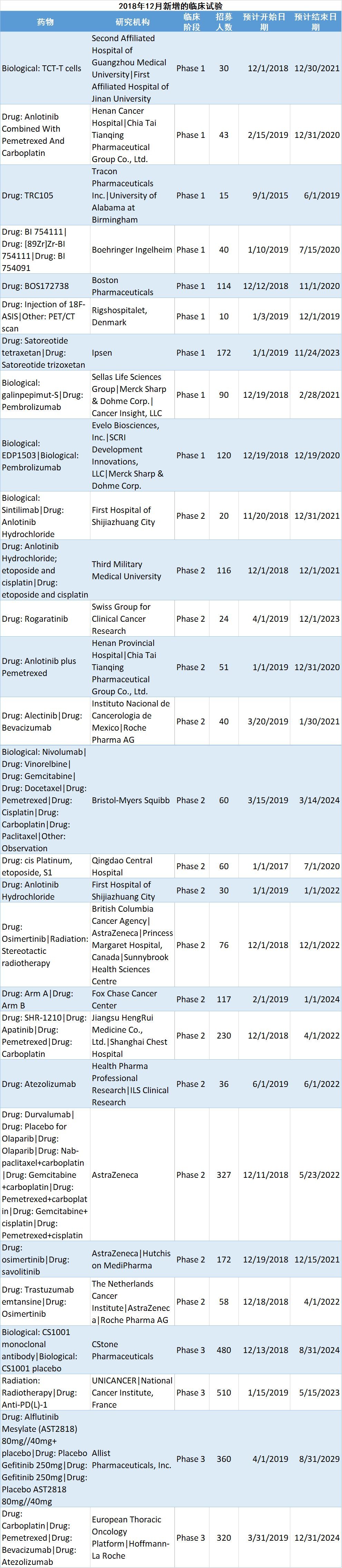
參考消息網6月20日報導世衛組織首席科學家蘇米婭·斯瓦米納坦6月18日介紹了當前全球新冠肺炎疫苗研製計劃的進度,引發外媒關注。
年底之前或現曙光
據埃菲社6月18日報導,世界衛生組織18日稱,近200個新冠肺炎疫苗研製計劃中,有4個(2個在中國、1個在美國、1個在英國)即將進入第三階段試驗,這是量產前的最後一個階段。
世衛組織首席科學家蘇米婭·斯瓦米納坦說,10支疫苗即將結束第二階段測試,其中有4個將在“大約兩周後”進入第三階段臨床試驗。
這4支疫苗分別是阿斯利康製藥公司與英國牛津大學合作研製的疫苗、美國疫苗研究中心與莫德納公司研製的信使核糖核酸疫苗,以及中國兩家醫學機構各自研製的疫苗。
報導稱,疫苗研製的第二階段要在100名志願者身上做測試,第三階段則要在數千人身上做測試,這個過程一般要持續至少一年或一年半,由於疫情嚴重,很多機構正嘗試加快疫苗研製速度。
斯瓦米納坦在記者會上說:“幸運的是,今年年底之前可能有一兩種疫苗被成功研製出來,但我們必須觀察目前臨床測試的結果。”
報導稱,如果有多種疫苗被證實有效並投入量產,斯瓦米納坦預計2021年有望生產出近20億劑,到時候必須考慮哪些群體和地區優先使用。
斯瓦米納坦說,世衛組織將與成員事先制定草案,明確在供應有限的前期階段應當如何分配疫苗。
斯瓦米納坦說:“我們建議優先考慮一線工作者,如醫生和護士,以及救護車駕駛員、警察、店員、清潔工和更加暴露的人群。”
報導指出,需要優先考慮的其他人群還包括老年人以及擁有可能使其表現出更嚴重症狀病史的人,例如糖尿病患者、肥胖人群和慢性呼吸道疾病患者等。
斯瓦米納坦說:“還應優先考慮工廠、監獄、養老院和貧民窟等風險地區的人群。每個國家都有較高風險的情形。”
斯瓦米納坦指出,疫苗的成功研製有助於緩解目前全球針對疫情采取的強力措施,如社交隔離、核酸檢測、追蹤和隔離疑似病例等。
據報導,斯瓦米納坦並不認為以最快速度進行研製就能確保生產出來的疫苗安全,因為“針對數千人進行的臨床測試在確保疫苗無副作用方面是足夠的”,但“零風險”是不可能的。
何時量產尚存變數
據法國《新觀察家》周刊6月16日報導,截至6月中旬,全球有183支團隊在進行新冠肺炎疫苗研發。法國製藥工業協會疫苗部門負責人克萊爾·羅歇表示:“這真的很多了。通常情況下,全球所有疾病的在研疫苗也就200支左右。”
法國巴斯德研究所科學部負責人克里斯托弗·當費爾說:“研究、試驗和投產,要拿到一支疫苗通常要10到15年。”
報導稱,由兩名法國人牽頭的兩家藥企似乎在“領跑”。一家是斯特凡·邦塞爾領銜的美國莫德納公司。這是一家想要掌控基於遺傳基因的一種顛覆性技術的企業,其市值目前已經達到了240億美元。邦塞爾擁有該公司9%的股份,並且已經開始進行新冠肺炎疫苗的第三期臨床試驗:就是要對數以千計的志願者進行試驗,以評估疫苗的有效性並確保沒有副作用。這是疫苗被批準上市前的最後一個階段。
另外一個領跑的法國人名叫帕斯卡爾·索裡奧,他主導著英國和瑞典合資企業阿斯利康製藥公司。要到今年秋初,他才能明言該公司與牛津大學聯合研發的疫苗是否有效。他表示,一旦疫苗研發成功,從10月起就可以開始批量製造。
報導稱,疫苗製造是個大市場,規模可以達到650億歐元(大約5138億元人民幣)左右。它算不上製藥業裡最賺錢的業務,但是回報仍然是很豐厚的。據業內人士透露,疫苗的利潤完全值得各藥企去冒險。法國賽諾菲巴斯德公司研發部負責人讓·朗解釋說:“跨過三個臨床試驗階段,就像穿越三座死亡山谷一樣。”他目前手裡有兩個新冠肺炎疫苗項目,其中有一個採用和美國莫德納公司一樣的技術。
疫苗研發及上市失敗的案例並不鮮見。賽諾菲集團2015年開始研發的麻疹疫苗,在投入了20億歐元之後,僅在十多個國家被批準用於特定人群,因為該疫苗有副作用。賽諾菲根本收不回成本。
據報導,製造疫苗的過程十分複雜,這也使得全球疫苗製造僅集中在幾大跨國藥企手中:賽諾菲、默克、輝瑞、葛蘭素史克以及強生。儘管近幾年也看到印度血清研究所發展迅速,其推出的肺炎球菌疫苗價格僅為傳統藥企的七分之一,但它根本無法與“非專利藥”大型藥企抗衡。一旦專利保護失效,這些大公司能以很低的成本生產藥物。與其製造“專利期內”的疫苗,不如用化學手段複製藥品更劃算。