肝癌是全球第2大腫瘤死亡原因,每年的肝癌死亡患者大約75萬例。全球每年新確診的肝癌患者大約有78萬例, 其中80%新發於中國、日本等亞洲國家。肝細胞癌約佔原發性肝癌的85%~90%。早期肝細胞癌的治療方法較多,包括手術、射頻消融、乙醇注射、化療栓塞等,但對於不可手術切除的肝細胞癌,治療選擇非常有限,預後極差,醫療需求遠未得到滿足。今天我們就一起來梳理一下肝癌的靶向治療藥物以及免疫治療藥物。
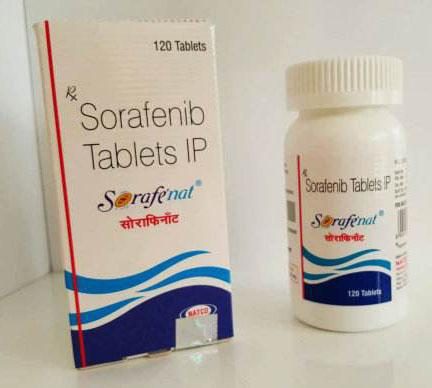
索拉非尼(肝癌一線)
商品名:多吉美
通用名:索拉非尼
廠家:Bayer
規格:200mg*60(原研)、200mg*120(仿製)
服用劑量:每次400mg,每天兩次
國內上市:是
價格參考:原研25000 每月 VS 仿製 900每月
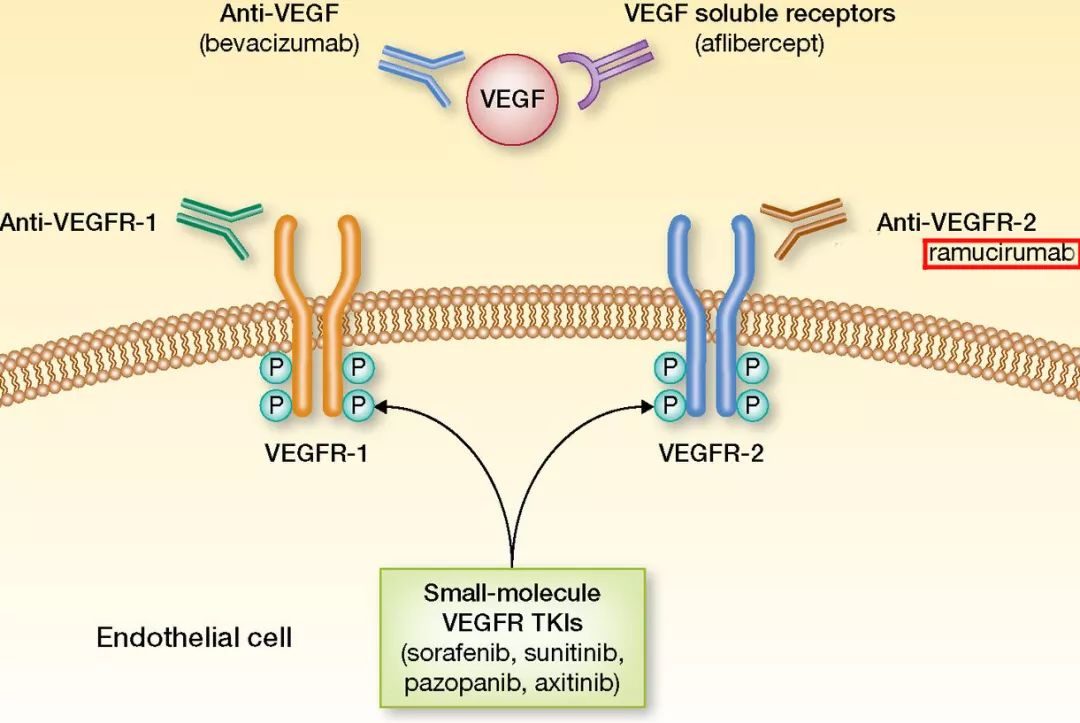
索拉非尼是一種新型多靶點抗腫瘤藥物,可同時作用於腫瘤細胞和腫瘤血管。它具有雙重的抗腫瘤作用:既可通過阻斷由RAF/MEK/ERK介導的細胞信號傳導通路而直接抑製腫瘤細胞的增殖,還可通過抑製VEGFR和血小板衍生生長因子(PDGF)受體而阻斷腫瘤新生血管的形成,間接地抑製腫瘤細胞的生長。

★獲批適應症
1、用於治療晚期腎細胞癌(一線)。
2、用於治療不能切除的肝細胞癌(一線)。
3、用於治療局部複發或轉移的進展性的放射性碘難治性分化型甲狀腺癌。
★肝癌臨床數據
研究對全球肝癌治療決策和索拉非尼治療肝癌研究(GIDEON)的國際資料庫中345例中國患者進行亞組分析。安全評估包括不良事件(AE)和嚴重不良事件(SAEs),依據美國國家癌症研究所常見術語標準3.0版進行分級。
結果顯示,在研究納入的331例患者中,98%患者的索拉非尼起始劑量為800mg/d。中位治療時間為22周(範圍:0.1~116周),中位總生存期(OS)為322天(10.7個月)。
大約50%的患者至少有一個不良事件,6%的患者有3~4級不良事件。29%的患者發生了藥物相關的不良反應,3.6%的患者發生了3~4級的藥物不良反應。總體而言,23%的患者(n=77)出現嚴重不良事件,其中只有1個事件為藥物相關(0.3%)。Child-Pugh分級A級和B級的患者在總體不良事件、嚴重不良事件和死亡方面沒有差異。
最常見的藥物不良反應是皮膚病(24%)、手足皮膚反應(20%)、胃腸道反應(11%)和腹瀉(11%)。大多數不良反應為開始口服索拉非尼後30天內出現。
★腎癌臨床數據
在2008年ASCO上,研究人員報告了在中國進行的索拉非尼治療晚期腎細胞癌患者的開放、多中心、非對照臨床研究結果。共入組62人經索拉非尼 400mg bid 治療31周後,可評價患者57人,其中1人(1.75%)獲得CR,11人(17.5%)獲得PR,36人(52.6%)獲得PD,病情控制率73.50%,PFS為41周(10.25個月)。
主要不良反應為:手足綜合症(16%)、腹瀉(4.8%)、高血壓(3.2%)。這一結果表明, 索拉非尼治療中國轉移性腎癌療效顯著,不良反應多為輕、中度。索拉非尼對中國人群的療效和不良反應可能與西方人群存在差異,治療過程中應重視防治高血壓和心腦血管。
★甲狀腺癌臨床數據
甲狀腺癌尤其是分化型甲狀腺癌(DTC)的發病率正逐年升高,外科手術、術後放射性碘治療(RAI)以及 TSH 抑製治療是 DTC 的主要治療策略,但部分患者最終可能發展為 RAI 難治性 DTC。憑藉國際多中心 III 期 DECISION 研究的充分證據,口服多激酶抑製劑索拉非尼獲得CFDA批準用於 RAI 難治性 DTC 的治療。
III期DECISION研究是一項國際多中心、安慰劑對照研究。既往未接受過化療、酪氨酸激酶抑製劑、靶向作用於VEGF或VEGF受體的單克隆抗體或者針對甲狀腺癌的其他靶向藥物治療的共417例局部晚期或轉移性、進展性、RAI難治性、分化型甲狀腺癌(乳頭狀、濾泡狀、許特爾細胞和低分化型)患者,被隨機分配接受400 mg口服索拉非尼每日兩次(207例患者)或匹配安慰劑(210例患者)治療。96%的隨機分組患者患有轉移性疾病。
研究顯示,與安慰劑相比,索拉非尼顯著延長了無進展生存期(PFS),即此項研究的主要終點(HR=0.59[95% CI,0.46-0.76];p<0.001),這表示與安慰劑治療患者相比,索拉非尼治療患者的疾病進展或死亡風險降低41%。索拉非尼治療患者的中位PFS為10.8個月,與之相比安慰劑治療患者為5.8個月。
索拉非尼組中最常見的治療期間不良事件包括手足皮膚反應、腹瀉、脫髮、體重減輕、疲勞、高血壓和皮疹。
樂伐替尼(肝癌一線)
商品名:樂衛瑪
通用名:樂伐替尼
廠家:日本衛材
規格:4mg*20(原研)、10mg*20(原研)、4mg*30(仿製)、10mg*30(仿製)
國內上市:否(預計近期上市)
價格參考:仿製約為原研的1/7
關於樂伐替尼的獲批適應症及臨床數據、不良反應等資訊請參考文章《孟加拉Beacon全球首仿樂伐替尼上市(附完整臨床數據)》,在此不再贅述。


關於一線選擇索拉非尼還是樂伐替尼,需由醫生根據患者的實際情況給出建議!從樂伐替尼和索拉非尼的對照臨床實驗(中國患者亞組)來看,兩組的中位OS為15個月 VS 10.2 個月,同時樂伐替尼組使死亡風險顯著降低 27%(HR 0.73)。次要終點方面,相比索拉非尼組,兩組中位PFS為9.2 VS 3.6 個月,HR 0.55,中位疾病進展時間(TTP)為11.0 VS 3.7 個月,HR 0.53,客觀緩解率(ORR)也獲得具有臨床意義的顯著改善:21.5% vs 8.3%,OR 3.17。顯然,樂伐替尼療效優於索拉非尼!
瑞戈非尼(肝癌二線)
商品名:拜萬戈
通用名:瑞戈非尼
廠家:Bayer
規格:40mg*28(原研)、40mg*28(仿製)
服用劑量:28天的前21天,每日口服一次,每次160mg,配合低脂餐。
國內上市:是
價格對比:原研30000 每月 VS 仿製 6000每月
瑞戈非尼是一款口服多激酶抑製劑,可阻斷涉及腫瘤生長和進展過程中涉及血管生成、腫瘤形成、轉移和腫瘤免疫的多種蛋白激酶,包括 VEGFR 1~3、TIE-2、RAF-1、KIT、RET、RAF-1、BRAF、PDGFR、FGFR 以及 CSF1R。這些激酶單獨或共同作用,控制腫瘤的生長、間質微環境的形成和疾病進展。


★獲批適應症
1、用於治療既往接受過以氟尿嘧啶、奧沙利鉑和伊立替康為基礎的化療,以及既往接受過或不適合接受抗VEGF治療、抗EGFR治療(RAS野生型)的轉移性結直腸癌(mCRC)患者。
2、既往接受過甲磺酸伊馬替尼及蘋果酸舒尼替尼治療的局部晚期的、無法手術切除的或轉移性的胃腸道間質瘤(GIST)患者。
3、既往接受過索拉非尼治療的肝細胞癌(HCC)患者。


★肝癌臨床數據
2016 年 12 月發表於柳葉刀(The Lancet)雜誌的國際多中心Ⅲ期 RESORCE 研究評估了瑞戈非尼用於索拉非尼治療後出現進展的肝癌患者的療效和安全性。其結果提示,瑞戈非尼顯著改善患者的總生存期(中位 OS 10.6 個月 vs. 7.8 個月,P<0.0001),與安慰劑對照組相比,瑞戈非尼組患者死亡風險顯著降低 37%。


圖1:瑞戈非尼顯著改善索拉非尼治療後進展肝癌患者的OS
無進展生存期(PFS)方面瑞戈非尼組同樣具有顯著優勢(中位 PFS 3.1 個月 vs. 1.5 個月,P<0.0001),以上治療獲益在所有預先界定的亞組中均得以維持。此外,經瑞戈非尼治療的患者還具有更高的緩解率和疾病控制率。


圖2:瑞戈非尼顯著改善索拉非尼治療後進展肝癌患者的PFS
RESORCE 研究的探索性分析顯示,從既往索拉非尼治療開始,索拉非尼和瑞戈非尼序貫治療方案可使肝癌患者中位生存時間延長至 26 個月。這對於苦無實質進展已久的肝癌內科治療無疑具有突破性意義。
瑞戈非尼常見的副作用有虛弱和乏力、手足綜合征、腹瀉、食欲不振、高血壓、口腔潰瘍、感染、聲音或音調變化、疼痛、體重減輕、胃痛、皮疹、發燒及噁心。嚴重副作用發生率不到 1%,包括肝損傷、嚴重出血、皮膚起水泡和脫皮、需要緊急處理的嚴重高血壓、心臟病發作及腸道穿孔。
卡博替尼(肝癌二線)
商品名:Cabometyx
通用名:卡博替尼
廠家:美國Exelixis
規格:20mg*84+80mg*28(原研)、60mg*30(仿製)
國內上市:否
價格參考:原研60000+ VS 仿製 9800
卡博替尼(cabozantinib),代號XL184,是一個多靶點小分子酪氨酸激酶抑製劑。184的靶點包括MET、VEGFR1 2 3、ROS1、RET、AXL、NTRK、KIT九大靶點。目前已獲批甲狀腺髓樣癌和腎癌,而對於肺癌、肝癌、攝護腺癌、多種癌症骨轉移都有相關臨床研究。


★肝癌臨床數據
一項國際多中心的大型三期臨床試驗(代號CELESTIAL)表明,卡博替尼作為二線治療藥物,可以顯著延長肝癌患者的生存期,減輕56%的死亡或者進展風險。
該臨床招募760位晚期肝癌患者,其中70%的患者經過一次系統治療(比如索拉非尼)後進展,30%的患者經過兩次系統治療後進展。470名患者使用卡博替尼治療,每天60mg,每天一次,237名患者使用安慰劑。兩組患者的中位無進展生存期(mPFS)5.2個月VS 1.9個月,中位總生存期為10.2個月 VS 8個月。其中,對於隻經過索拉非尼治療的患者來說,卡博替尼組的中位總生存期高達11.3個月 VS 安慰劑組7.2個月,無進展生存期是5.5月 VS 1.9個月。
卡博替尼組常見3-4級副作用包括:手足綜合征(17%),高血壓(16%),轉氨酶升高(12%),乏力(10%)和腹瀉(10%)。
關於卡博替尼獲批其他適應症的相關臨床數據請參考文章《九靶點卡博替尼我可以嘗試嗎?》
雷莫盧單抗(肝癌二線)
商品名:Cyramza
通用名:雷莫盧單抗(Ramucirumab)
廠家:禮來
規格:100mg(原研)、500mg(原研)
國內上市:否
價格參考:原研6200(100mg)
雷莫盧單抗是一種單克隆抗體受體拮抗劑,設計用於結合VEGFR2的胞外結構域,從而阻斷VEGF的結合併抑製受體激活。


★獲批適應症
1、2014年4月獲批單葯治療含氟脲嘧啶或鉑劑化療進展的進展期 / 轉移性胃癌或胃食管結合部腺癌。
2、2014 年 11 月獲批與紫杉醇聯合治療進展期胃癌 / 胃食管結合部腺癌。
3、2014 年 12 月獲批與多西他賽聯合治療含鉑化療進展的轉移性非小細胞肺癌。
4、2015 年 4 月獲批與 FOLFIRI 聯合治療含有貝伐單抗、奧沙利鉑、氟脲嘧啶的 1 線治療進展的轉移性結直腸癌。
★使用劑量
1、胃癌 8 mg/kg,大於 60 分鐘靜脈輸注,每 2 周 1 次,可以單葯應用,與紫杉醇合用時先於紫杉醇應用;
2、非小細胞肺癌 10 mg/kg,第 1 天大於 60 分鐘靜脈輸注,每 3 周 1 次,多西他賽前使用;
3、結直腸癌 8 mg/kg,大於 60 分鐘靜脈輸注,每 2 周 1 次,FOLFIRI 方案前使用。
★肝癌臨床數據
2018年4月4日,禮來公司公布了雷莫盧單抗作為單一療法二線治療肝細胞癌(HCC)的臨床3期研究REACH-2的頂線積極數據。雷莫蘆單抗用於基線AFP升高的肝癌二線治療,三期臨床試驗獲得成功。
在REACH研究中,共入組了565名一線治療失敗的晚期肝癌患者,1:1分組,其中283名患者接受雷莫蘆單抗治療(8mg/kg,2周一次),另外282名患者接受安慰劑治療。兩組的中位總生存期為9.2個月 VS 7.6個月, OS雖有改善但無統計學意義。然而,該試驗卻發現了 雷莫盧單抗單一製劑令人鼓舞的活性,在關鍵次要終點及某些患者亞群中存在有意義的改善。
研究人員隨後對REACH數據進行了進一步分析,其中包括一項亞組分析,在亞組分析中,對於那些AFP超過400ng/ml的高危患者中,雷莫蘆單抗組的中位總生存時間為7.8個月,安慰劑組只有4.2個月,幾乎翻了一倍,有顯著的統計學差異。該分析表明基線AFP高表達的患者使用雷莫盧單抗OS獲益。根據這些研究結果,第三階段REACH-2研究開始實施。
這項全球、隨機、雙盲、安慰劑對照的REACH-2III期臨床試驗,比較了雷莫盧單抗和安慰劑在對索拉非尼不耐受或使用後疾病進展的、並表現出高AFP血清水準(≥400 ng/mL,原發性肝癌特異性標誌物)的肝癌患者中的療效。該試驗於2015年開始,在全球20個國家共招募了292名患者,是首個在通過生物標誌物檢測分類的患者群體中進行的3期HCC試驗。結果顯示,研究抵達了總生存期(OS)的主要終點,和無進展生存期(PFS)的次要終點。
REACH-2 研究的安全性數據與之前研究的結果一致,與對照組相比,雷莫盧單抗治療組最常見(發生率 ≥ 3%)臨床分級 ≥ 3 的不良事件發生頻次更高,主包括高血壓和低鈉血症。
免疫治療:Opdivo
商品名:Opdivo(歐狄沃)
通用名: Nivolumab(納武單抗)
廠家:BMS(百時美施貴寶)
規格:100mg(原研)、40mg(原研)
國內上市:是
價格參考:9260(100mg)、4591(40mg)
關於Opdivo的獲批適應症、使用方法、不良反應、使用前注意事項?請閱讀文章《O葯今日國內開售和我有什麼關係?》


Opdivo聯合樂伐替尼,12周後腫瘤消失?請閱讀文章《肝癌晚期的終極大招是PD-1+樂伐替尼?》
★肝癌臨床數據
2017年9月美國FDA批準Opdivo用於接受過索拉非尼治療後的肝細胞癌(HCC)患者。
在CheckMate-040臨床研究中,154例索拉非尼治療後進展或不耐受的HCC患者入組。14.3%(95% CI: 9.2-20.8; 22/154)的患者在Opdivo治療後出現緩解。完全緩解率為1.9%(3/154),部分緩解率為12.3%(19/154)。在獲得緩解的患者中(n=22),緩解時間範圍為3.2至38.2+個月,91%的患者緩解時間達6個月或更長,55%的患者緩解時間達12個月或更長。
Opdivo相關的警告與注意事項包括:免疫介導的非感染性肺炎、結腸炎、肝炎、內分泌疾病、腎炎和腎功能不全、皮膚不良反應、腦炎、其他不良反應;點滴反應;胚胎胎兒毒性等。
免疫治療:Keytruda
商品名:Keytruda
通用名:Pembrolizumab(派姆單抗)
廠家:MSD(默沙東)
規格:100mg(原研)、50mg(原研)
國內上市:已獲批
價格參考:29000(港版100mg)、15000(港版50mg)
作為免疫治療領域的「明星」藥物,Keytruda於2014年9月4日獲得美國FDA批準登上癌症治療歷史舞台,獲批的首個適應證是轉移性黑色素瘤。之後陸續在非小細胞肺癌、頭頸癌、淋巴瘤、消化道腫瘤(胃癌)、婦科腫瘤(宮頸癌)等領域獲批,表現出強大的廣譜抗腫瘤效果。


★肝癌臨床數據
2016 年歐洲腫瘤內科學會上,有學者彙報了關於Keytruda治療晚期 HCC 的2項臨床研究,分別為 KEYNOTE 240 和 KEYNOTE 224,兩項研究正在進行中,目前尚無數據更新。
值得一提的是 Truong 等報導 1 例採用Keytruda治療有效的轉移性 HCC 患者。該 HCC 患者男性,75 歲,經根治性左半肝、膽囊切除術後 3 年出現複發轉移伴甲胎蛋白 ( AFP) 升高 ( >2 000μg / L) ,口服索拉非尼5 個月 AFP 繼續升高( 8 87 μg / L) ,且影像學檢查提示,病情進展,後改用Keytruda治療,經 6 個周期治療後發生戲劇性改變,腫瘤迅速減小,AFP 降至正常水準( 1. 7μg / L) 。這是第 1 例報導的關於Keytruda對索拉非尼治療失敗的轉移性 HCC 患者治療有效的個案。
2018年7月25日,我國FDA正式批準PD-1單抗KEYTRUDA(帕博利珠單抗,Pembrolizumab)的中國上市申請,用於經一線治療失敗的局部晚期或轉移性黑色素瘤的治療。Keytruda成為繼Opdivo之後第二款在中國上市的PD-1抑製劑,該葯從申請到獲批用時不到六個月,刷新了中國進口抗癌腫瘤生物製劑最快審批記錄。
綜上述,對於不可切除的晚期肝癌,索拉非尼和樂伐替尼是一線用藥,耐葯後可以考慮瑞戈非尼、卡博替尼、雷莫盧單抗以及免疫治療、聯合治療等方案。
【重要提示】文章資訊僅供參考,具體治療謹遵醫囑!
期待更多的新葯上市,造福更多的肝癌患者!更多指導和交流加暖暖:tatahealthy
本文由【全球好葯資訊】原創發布,轉載請註明出處!