記者 | 梁昌均
本周(3月31日至4月6日)政策方面,醫療器械臨床試驗審批也進入默示許可製時代。本周僅有13家藥企發布年報,智飛生物(300122.SZ)業績翻倍,獨家產品暫停生產致股價大跌;通化金馬(000766.SZ)和福安藥業(300194.SZ)涉足工業大麻,引發深交所炒作股價的質問。另有7家藥企股東計劃減持,平安方面計劃減持雲南白藥(000538.SZ)3%股份,華大基因(300676.SH)被查出三大問題要求被整改。研發層面,人福醫藥(600079.SH)、華東醫藥(000963.SZ)、通化東寶(600867.SH)取得進展。
行業政策
4月4日,國家藥監局發布公告,注銷85個藥品批準文號,其中53個是由於企業主動申請,13個是因已撤銷藥品批準證明文件,另外19個藥品批準文號被注銷是由於企業被依法吊銷《藥品生產許可證》,而這19個被被注銷的批準文號均來自處於退市倒計時的長生生物(002680.SZ)旗下的長春長生生物科技有限責任公司,注銷產品包括此前涉事的狂犬病疫苗、百白破疫苗等18個疫苗產品和胸腺肽注射液。
4月4日,國家藥監局再次公開征求《關於進一步完善藥品關聯審評審批和監管工作有關事宜的公告(征求意見稿)》意見,進一步明確原料藥、藥用輔料、藥包材與藥品關聯審評審批和監管有關事宜,其中提出對仿製國內已上市的原料藥,登記時可以不與藥品製劑關聯,即單獨登記,經審評通過後,登記狀態標識為“A”,不再發給藥品批準文號;藥用輔料、藥包材已取消行政許可,平台登記不收取費用。
原料藥企業的審批制度造成了批文的稀缺性,在一定程度上也助推了原料藥價格上漲,甚至壟斷。原料藥批文取消,或將推動原料藥市場競爭更加激烈,這也被業內視為國家打破原料藥價格壟斷的重要舉措。
4月1日,國家藥監局發布關於調整醫療器械臨床試驗審批程序的公告,提出自臨床試驗審批申請受理並繳費之日起60個工作日內,申請人在預留聯繫方式、郵寄地址有效的前提下,未收到國家藥監局器審中心意見(包括專家谘詢會議通知和補充資料通知)的可以開展臨床試驗;同意開展臨床試驗的,審查結果將通過器審中心網站告知申請人,不再發放臨床試驗批件。這意味著,自去年7月國家藥監局推出藥物臨床試驗默示許可製後,該方式又拓展至醫療器械,審批程序進一步優化。
重要動態
智飛生物業績翻倍 獨家產品暫停生產
本周僅有13家藥企發布2018年年報,其中天壇生物(600161.SH)、紅日藥業(300026.SZ)、廣生堂(300436.SZ)、吉林敖東(000623.SZ)、億帆醫藥(002019.SZ)5家企業淨利潤出現不同程度下降。
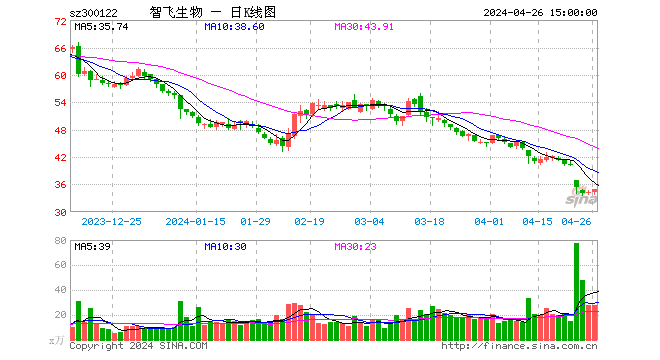
在8家淨利潤出現增長的企業中,智飛生物(300122.SZ)增長最為強勁。根據4月3日晚該公司發布的年報,去年實現營收52.28億元,同比增長289%;淨利潤14.51億元,同比增長236%。該公司擬每10股派發5元,合計分紅8億元。
智飛生物目前共有5種自主產品和6種代理或協議推廣產品在售,其中全球獨家品種AC-Hib三聯疫苗和代理的默沙東HPV疫苗是公司業績的核心推動力。
去年智飛生物自主產品疫苗收入12.42億元,同比增長近26%,佔公司營收的比重從上年的74%左右大幅下降至24%,但其毛利率仍維持在高位,達到95.42%。其中AC-Hib三聯疫苗是自主產品的核心,去年其批簽發近644萬支,同比增長約37%,是公司批簽發量最多的品種。光大證券預計AC-Hib三聯疫苗去年銷售550萬支,貢獻收入超11億元,同比增長38%。
值得注意的是,AC-Hib三聯疫苗面臨暫停生產。4月1日晚智飛生物發布公告稱,去年11月向北京市食藥監局提交AC-Hib三聯疫苗再注冊申請,目前行政程序尚未完成,公司尚未收到再注冊批件。鑒於原藥品批準文號有效期至2019年4月1日,因此在未獲得再注冊批件之前將暫停AC-Hib三聯疫苗生產。
這直接導致4月2日智飛生物跌停,單日市值蒸發近83元;4月4日,在業績大幅增長的情況下,該股仍大跌4.73%,市場擔憂情緒明顯。智飛生物稱,若AC-Hib三聯疫苗不再獲批注冊,將對公司2019年及今後的經營業績產生較大影響,其在回應媒體時稱此次並不涉及AC-Hib三聯疫苗的產品質量問題,且還有一定庫存。
據中泰證券研報,目前智飛生物生產有600萬支左右AC-Hib三聯疫苗(原生產批件有效期內生產),後續有望陸續批簽發,基本可以滿足一年左右需求。按中性預期該產品在2019年獲得再注冊批件,則對2019-2020業績沒有影響;若悲觀預期則再注冊無法獲得批件,新的三聯苗凍乾劑型有望於2020年底獲批,則三聯苗缺貨0.5-1年,對2020年淨利潤有一定影響。
代理產品則成為智飛生物業績貢獻的第一大主力,去年實現收入38.88億元,同比大幅增長1319%,對公司營收的貢獻從上年的20%大幅增加至74%,同時其毛利率也增長近12個百分點達到41.28%。這主要系公司代理的默沙東的四價HPV疫苗、九價HPV疫苗迅速放量所致,去年批簽發量分別為380萬支、122萬支,其中四價HPV疫苗同比增長992%。
2018年11月5日,智飛生物與默沙東就四價和九價HPV疫苗約定了自2019年至2021年6月30日期間共計約180.02億元的產品基礎採購金額。若AC-Hib三聯疫苗無法及時再獲批生產,HPV疫苗將成為業績核心增長點,有望填補一定業績空缺。
兩家藥企涉足工業大麻 華仁藥業確定合作方式
3月31日晚,通化金馬(000766.SZ)稱,公司與吉林省農科院、通化市二道江區人民政府共同簽署《工業大麻合作項目協議》,探索工業大麻育種、種植及研發。合作期限五年,公司將分期支付研發經費,研發經費總額約3838萬元。深交所4月1日下發關注函,要求公司說明開展工業大麻的必要性、相關資質、技術與人才儲備,以及是否存在主動迎合市場熱點、炒作股價、配合股東減持的情形。
4月1日,福安藥業(300194.SZ)稱,公司與在美國內華達州拉斯維加斯擁有成熟的工業大麻種植基地、加工設備和銷售渠道的兩家企業Red Realty LLC、Golden Way Investor, LLC簽訂了《合作意向協議》,擬利用各自優勢在工業大麻綠色種植,工業大麻產品提取、深加工等領域開展合作。當日深交所下發問詢函,要求公司說明是否涉嫌炒作股價、合作必要性、可行性和發展前景、是否具備技術與人才儲備、合作對方情況等。
4月3日,繼在3月28日簽訂合作框架協議後,華仁藥業(300110.SZ)公布具體合作方式,公司與雲南素麻、侯傑計劃共同設立合資公司,合作在雲南建設工業大麻綠色工廠,打造中國第一家工業大麻溫室大棚種植基地。合資公司注冊資本約為1.33億元,公司現金出資持股45%,雲南素麻以種植技術及相關資質評估作價方式出資持股35%。
簡評:這三家企業因工業大麻本周股價上漲明顯,業績巨虧的福安藥業更是連續拉出五個漲停,而通化金馬得控股股東及其一致行動人此前計劃減持不超過10%股份,也被深交所質問是否存在配合股東減持情況,華仁藥業兩大股東在4月2日晚稱合計減持不超過4%股份,但市場不懼減持繼續推動該股上漲。目前計劃布局工業大麻的企業幾乎都還未實際開展業務,近期多個部門也要求加強工業大麻審批和管理,工業大麻概念股表現受到一定程度打擊,後續仍存在諸多風險。
亞寶藥業控股股東轉讓8.18%股份
4月4日晚,亞寶藥業(600351.SH)稱,控股股東山西亞寶投資集團有限公司(下稱亞寶投資)將其持有的公司6300萬股無限售流通股(佔總股份的8.18%)轉讓給廣東晉亞紓困股權投資合夥企業(有限合夥)(下稱晉亞紓困),晉亞紓困將上述股份的表決權、提案權及參加股東大會的權利委託給亞寶投資全權行使。此次股份轉讓價格為7.4元/股,轉讓價款合計為4.66億元。
簡評:亞寶投資此次轉讓股份是為了紓解資金的暫時流動性困難,而晉亞紓困是山西國投旗下企業,亞寶藥業則是繼東傑智能、振東製藥後山西第三家被地方國資背景企業紓困的A股公司。但有所不同的是,此次晉亞紓困將標的股份表決權等仍交由亞寶投資行使,僅要求未來董事會換屆提名一名非獨立董事。此次轉讓完成後,亞寶投資持有公司17.13%股份,仍為控股股東。
其他藥訊
7家藥企股東要減持 平安計劃減持雲南白藥3%股份
本周浙江醫藥(600216.SH)、藥石科技(300725.SZ)、盤龍藥業(002864.SZ)、華仁藥業(300110.SZ)、雲南白藥(000538.SZ)、葵花藥業(002737.SZ)、複旦複華(600624.SH)等7家企業股東計劃減持,其中引發市場關注的是雲南白藥持股9.40%的第三大股東中國平安人壽保險股份有限公司(下稱平安人壽)計劃減持不超過3124萬股(佔總股本的3%),減持原因為系資金周轉需要。4月3日午間雲南白藥發布該消息後,其股價午後開盤大幅下挫,跌幅一度超過3%。

平安人壽於2008年以近14億元通過定增成為雲南白藥重要股東,該項投資已浮盈數倍,而其在去年8月就已發布過減持計劃,但最終未減持,此次則是延續。值得注意的是,該股東代表董事還在雲南白藥吸收合並控股股東事項中投出唯一的反對票,且公司業績持續疲軟,繼續推進減持或反映出平安方面對雲南白藥未來預期有所降低,平安集團則回應稱此次減持系其整體投資組合再平衡和動態調整的一部分。按最新股價和減持上限計,平安人壽此次有望套現約27億元。
華大基因被查出三大問題責令整改
4月4日晚,華大基因(300676.SH)稱,收到中國證監會深圳監管局下發的責令改正措施的決定。經檢查發現,公司主要存在三大問題:一是存在訂單型收入確認依賴的系統存在漏洞,因跨期撤銷交付並導致相關收入成本核算跨期問題,使得公司2017年少計收入50萬元、淨利潤42萬元;同時存在樣本編碼重複並導致收入重覆核算問題,使得公司2017年多計收入38萬元、淨利潤32萬元。
二是部分項目型收入核算與會計政策不一致,公司2017年多計收入1328萬元、淨利潤1245萬元。三是規範運作程度不高,存在部分執行的財務制度不規範、關聯方員工參與公司項目工作、向關聯方華大智造預付款超過合約約定(多支付0.31億元)等情形。深圳監管局要求公司責令改正,並對實控人及董事長汪建、總經理尹燁和財務總監陳軼青出具警示函。
華潤方面要約收購江中藥業不足1.5萬股
4月3日晚,江中藥業(600750.SH)稱,華潤醫藥控股對公司發起的要約收購期限屆滿,在3月4日起至4月2日要約收購期間,公司股東預受要約股份共計816,175股,撤回預受要約股份共計801,518股,最終有17個账戶共計14,657股股份接受收購人發出的要約。
海思科獲得海外產品獨家許可權
4月1日晚,海思科(002653.SZ)稱,公司全資子公司四川海思科與美國公司eXIthera簽署《股權認購協議》及《獨家許可協議》,擬使用600萬美元認購eXIthera發行的278.71萬股普通股,並獲得其產品EP-7041在中國境內的獨家許可。該產品已在澳洲完成Ⅰ期臨床並即將在美國遞交臨床申請,有望成為抗凝血和抗血栓藥物市場的主流藥物。
研發進展
人福醫藥產品獲批注冊
4月3日晚,人福醫藥(600079.SH)稱,控股子公司宜昌人福藥業有限責任公司收到國家藥監局核準簽發的鹽酸安非他酮緩釋片的臨床試驗通知書,豁免藥代動力學試驗。該產品適用於治療中重度抑鬱症以及季節性情感障礙,去年6月獲得美國FDA批準文號
華東醫藥產品ANDA獲暫時批準
4月3日晚,華東醫藥(000963.SZ)稱,公司全資子公司杭州中美華東製藥有限公司向美國FDA申報的注射用泮托拉唑鈉凍乾粉針無菌注射劑的ANDA(即美國仿製藥申請)已獲得暫時批準(指美國FDA已經完成該藥品的所有審評流程,但存在相關專利未到期的情形)。該產品主要適用於急性上消化道出血,目前美國境內廠商僅為原研公司日本武田製藥。
通化東寶糖尿病產品注冊獲受理
4月2日晚,通化東寶(600867.SH)稱,收到西格列汀二甲雙胍片(Ⅱ)藥品注冊申請受理通知書。該產品由默沙東原研開發,2007年3月在美國上市,用於Ⅱ型糖尿病的口服治療,次年在歐盟獲批上市,2012年我國批準進口。目前國內未有仿製藥品批準上市,有2家廠家對該藥品進行了申報生產注冊。