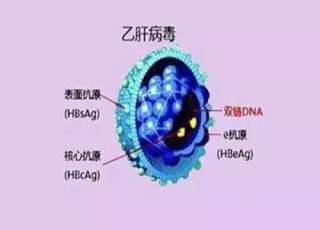
較早進入我國的核苷類似物(NA)抗病毒藥物拉米夫定(LAM),LAM為葛蘭素史克公司研發。2020年歐洲肝髒研究年會上(EASL 2020),葛蘭素史克研究人員也對外公布了旗下B肝在研新藥ISIS 505358(GSK328836)的進展。

B肝在研新藥505358,抑製穩定NA,3名表面抗原顯著下降
在制定目標方面,通過了解藥物開發背景與目的很重要。目前,全球肝病領域臨床醫生或科研人員比較認同的是功能性治愈,其中促使B肝表面抗原陰轉就成為實現功能性治愈的主要結果指標。這是因為B肝表面抗原可以通過抑製宿主對B肝病毒的免疫應答,在維持與B肝病毒持續感染中起著重要作用。ISIS 505358,即GSK328836(更名後)是一種2́-MOE修飾反義寡核苷酸(ASO),針對所有HBV-RNA。
EASL 2020上,GSK研究人員公布的在研B肝新藥GSK328836,主要是評價其在慢性B肝患者中的抗病毒活性和安全性。這是一項2a期、隨機、雙盲、安慰劑對照研究,已於2020年8月28日11:00-11:15對外界公布。ISIS 505358抑製穩定核苷類似物(NA)方案的慢性B肝患者(CHB)和未感染B肝患者的表面抗原抑製。

試驗方法如下:所有受試者B肝表面抗原陽性大於或等於6個月,篩查時,B肝表面抗原水準需大於50IU/mL。NA組均是穩定方案大於或等於12個月,血漿HBV-DNA低於定量下限(LLoQ,20IU/mL)。初發受試者HBV-DNA大於或等於2乘以10的3次方,排除標準包括:肝硬化;HCV、HIV或HDV合並感染;ALT或AST>5xULN或膽紅素>1.1xULN。
e抗原陽性與陰性受試者都符合條件。300毫克ISIS 505358(ASO)或安慰劑在第1天、第4天、第8天、第11天、第15天和第22天皮下注射。第29天為對乙型肝炎病毒療效的初步評估。結果表明,在NA組受試者的平均B肝表面抗原(HBsAg )log10 IU/mL±SE變化,ISIS 505358(ASO)組為-2.514±0.783(n=4),安慰劑組為-0.008(Pbo,n=2)。

葛蘭素史克公司資料圖
ISIS 505358(ASO)組有3名受試者下降大於3.0log10IU/mL,其中1名小於<LLoQ(0.05IU/mL)。另一個在第36天達到<LLoQ。對於新生兒,ASO(n=12)的B肝表面抗原(HBsAg)平均變化為-1.556±0.398(p=0.001 vs Pbo,n=6),HBV-DNA的B肝表面抗原(HBsAg)平均變化為-1.655±0.427(p<0.001)。
有3名和4名ISIS 505358(ASO)組受試者的B肝表面抗原和HBV-DNA減少量分別大於3.0 log10 IU/mL,其中有2名和1名的水準也降至<LLoQ。本研究發生了1名SAE:有1名B肝表面抗原和HBV-DNA降低到<LLoQ的受試者,在ASO治療後ALT升高到781 U/L(24xULN)。其他HBsAg<LLoQ的受試者出現ASO後ALT信號,峰值在1.7~15xULN之間。

ALT耀斑無症狀,可自行分辨。300毫克ISIS 505358(ASO)組受試者(17名中的5名)最常見不良事件發生在注射部位(紅斑、疼痛、瘙癢、腫脹和/或瘀傷)。結果表明,ISIS 505358/GSK328836治療4周後,無論是在穩定的NA方案還是在未曾接受NA方案的CHB中,B肝表面抗原水準均顯著降低。在未成年受試者中,同樣觀察到HBV-DNA顯著減少,耐受性和安全性總體良好,可以接受更長的治療時間。

小番健康結語:本研究已經在EASL 2020年會公布,由葛蘭素史克公司資助的在研B肝新藥ISIS 505358(現稱GSK328836)是基於反義寡核苷酸(ASO)覆蓋所有HBV-RNA設計的藥物。這是一項已進展到第2期a部分的臨床試驗,評估ISIS 505358抑製NA方案的慢性B肝患者和未接受NA的慢性B肝患者中的表面抗原抑製。返回搜狐,查看更多
責任編輯: