芬太尼是一種強效麻醉性鎮痛藥,適用於治療疼痛和手術鎮痛,其鎮痛效果約為嗎啡的80倍。但同時,它又是繼傳統毒品、合成毒品之後的第三代毒品——“實驗室毒品”中的重要成分。本身是在臨床麻醉、術後鎮痛以及ICU鎮靜中的好藥,卻又成了“實驗室毒品”中的重要成分,這是為什麽呢?在中科院SELF格致論道講壇上,中國科學院生物物理所副研究員葉盛為我們揭秘,到底藥從哪裡來?
出品:"SELF格致論道講壇"公眾號(ID:SELFtalks)

以下內容為葉盛在中科院SELF講壇演講實錄:
很高興有這樣一個機會,能跟大家交流一些有關於藥物研發的故事。我來自於中國科學院生物物理研究所,如果你曾經聽過我的名字,很可能是因為這本書——《大滅絕時代》,它是我翻譯的一本科普書。
這本書的原著——《第六次大滅絕》,今年剛剛獲得了普立茲獎,足以說明它的寫作水準是非常高的,而且這本書介紹的科學知識非常嚴謹,是非常前沿的研究成果。
如果用一句話來概括這本書講了什麽事情,那就是:人類自從誕生之日起,就一直在持續不斷地破壞著我們的環境,毀滅著這個地球上生存的其他物種。你們可能會問,我們該怎麽辦?很遺憾這本書裡沒有給出答案。
其實對於這個問題有兩種不同的思想,其中一種思想認為我們應該退回一個低技術水準的時代,甚至退回到刀耕火種的時代。

這張圖片大家猜猜是什麽?這不是拍戰爭場面的電影,更不是真實的戰爭場面,這是華北某地焚燒秸稈的現場,這些煙霧對我們PM2.5做出了巨大的貢獻。實際上,回到低技術水準意味著嚴重的汙染。
另一方面,低技術水準意味著低供給能力。我們全球有60億人口,中國有13億人口,回到刀耕火種的時代我們吃什麽?所以說此路不通。那麽我們應該怎麽做?在我看來,我們應該進一步發展我們的科學技術,這就包括了方方面面的事情。
下面我要談談跟自己的科研工作相關的,藥物研發的幾個小故事,而這些小故事其實恰恰體現了科學技術進步對於我們人類的拯救。

首先我將從抗生素開始講起。大家可能不知道,在沒有抗生素的時代,一個傷口就可能是致命的。如果你去看病的話,醫生給你開的藥方可能會含有蜂蜜、豬油、蛋黃、活蚯蚓,甚至是死去小動物的屍體。這還不是最可怕的,如果是在戰場上受到槍傷的話,當時的醫生認為火藥是有毒的,怎麽消毒?他們會用滾燙的接骨木油澆到在你的傷口上,這種痛苦可想而知。
在沒有抗生素的時代,上手術台就像上刑場一樣可怕。曾經有一個著名的外科大夫,在一次截肢手術中死去了三個人:他的病人、他的助手,還有一位監視者,三個人中有兩個死於傷口感染。所以在沒有抗生素的時代,醫學真是非常尷尬的一件事情。

抗生素是被怎麽發現的呢?實際上青霉素,也就是第一個抗生素的發現,是非常偶然的事件。當時,一位研究微生物的科學家弗來明發現,他培養細菌的一個平板上有一個地方不長細菌,反而長了黴菌。通過進一步研究發現,黴菌分泌的一種物質能夠溶解周圍的細菌,這種物質就是後來的青霉素。
接下來,通過另外兩位科學家的努力,真正實現了抗生素的大規模工業化生產,才讓青霉素真正成為一種實用化的藥物。這三位科學家一起獲得了1945年諾貝爾生理及醫學獎。
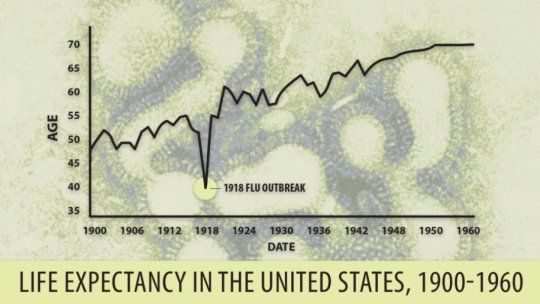
有人做過統計,現代醫學使我們人類平均壽命延長了20年,而在這20年中有10年是抗生素所貢獻的,可以想像抗生素的發現對於我們人類來說非常重要的。
除了偶然發現的藥物以外,還有一些藥物是意外獲得的,文縐縐一點就是“有意栽花花不開,無心插柳柳成蔭”,俗一點就是“打哪指哪”。

首先讓我們看看這種藍色的小藥丸——“偉哥”,藥品名叫萬艾可。這個藥物最早研究的時候是用來治療心血管疾病的,然而在它的臨床實驗中,科學家偶然發現這個藥物有一些非常有趣的生理副作用。最終,萬艾可成為一種治療勃起障礙等男性性功能疾病的藥物。
第二個想講的例子是一種叫做二甲雙胍的藥物,如果你身邊親朋好友當中有人患有二型糖尿病的話,你可能聽說過它,因為它是胰島素治療的時候一個重要的輔助藥。它非常非常的便宜,每天只需要花你幾毛錢或者幾塊錢。
而現在,科學家發現這種藥很可能具有一個價值不菲的副作用,那就是能夠延緩衰老。美國食品藥品管理局在2015年批準將於次年在美國進行二甲雙胍抗衰老的臨床實驗,雖然科學家還不能讓大家返老還童,但很可能將為大家提供一種真正意義上延緩衰老速度的藥物。
第三個藥物叫格列衛,這個藥物最初被製藥公司合成出來,是用於做炎症治療研究的,後來成為了治療白血病的藥物,這種藥對於慢性淋巴細胞白血病有一個非常好的療效。這種藥物在最終上市的時候還登上了《時代周刊》的封面,可見它對我們是非常非常重要的藥物。
除了這些意外收獲以外,我們可以看一下這些意外是不是有什麽必然性呢?實際上在格列衛上市的時候,研究它的科學家們只是知道這種藥物能夠抑製一種蛋白質的作用。具體怎麽抑製的?科學家們並不清楚。

在幾年之後,是我們結構生物學家解析得到格列衛和那種蛋白質在一起的三維結構。圖上五彩繽紛的飄帶代表蛋白質,而格列衛是用白色、藍色和紅色的小球表示的,分別代表了碳原子、氮原子和氧原子。
那我們可能就會想了:我們現在有了蛋白質和藥物在一起的樣子,如果把藥物拿掉只剩下蛋白質的樣子,我們有沒有可能根據這個形狀去設計出格列衛這樣的藥物呢?如果可以的話我們就不需要做大量篩選了,也不用浪費時間做很多前期研究了。實際上,這樣的想法是絕對可行的,它就是“基於結構的藥物設計”。
大家知道,很多疾病是由於基因的問題引起的,特別是癌症,而基因都要翻譯成蛋白質才能行使功能,而我們結構生物學家可以研究這些蛋白質的三維結構,通俗地說就是看看蛋白質長什麽樣子。
然後,我們研究它的樣子和它的功能兩者之間的聯繫,最後我們試圖尋找一些小分子的藥物,能夠抑製這個蛋白質的功能,它們就很有可能成為將來的藥物。在這個階段,我們稱之為“先導化合物”。
下面再舉個更加通俗易懂的例子,讓我們來想象一個齒輪,齒輪長什麽樣子?中間有孔,整體是圓形的,外面有齒,這個樣子跟它功能之間有什麽關係?孔是為了插軸,圓形為了轉動,外面的齒是為了和其他齒輪咬合在一起。
我們有沒有可能想辦法抑製它的功能?當然可以。很簡單,我們只要找一個楔子,讓它的形狀和齒與齒之間的空間是一致的。我們把這個楔子釘到齒輪上,這個齒輪就不能工作了。所以大家想象一下,如果把這個楔子移到蛋白質身上,它就是藥物先導化合物,這個就叫做基於結構的藥物設計,而這正是我所做研究工作的一部分。
下面講兩個實際的例子,都是我親身參與的。第一個例子是關於SARS病毒的,2003年的時候SARS在我們國家曾經肆虐了很長一段時間,當時我在清華大學的實驗室讀博士,被封校關在了裡面。
大家可能覺得封校是件讓人很鬱悶的事情,但其實不然。當時的清華大學在我看來是最像大學的時候。為什麽?因為不允許室內聚集,大家也不用上課和自習了,學生們每天都在草坪上打打牌、看看書、做做遊戲,過得不亦樂乎。
然而,對於我們實驗室的學生來說,這種不亦樂乎的日子很快就結束了,因為我們的導師饒子和院士從華大基因那裡拿到了SARS病毒的全基因組。我們的學生都回到了實驗室,開始日以繼夜地生產SARS病毒的蛋白質,然後打成包,免費派發給全國任何想做抗SARS研究的實驗室。我們同時自己也對這些蛋白質做研究,希望得到SARS病毒全部蛋白質的三維結構。
實際上,就在2003年,我們獲得了人類第一個SARS病毒的蛋白質結構,就是圖上所展示的SARS病毒主蛋白酶結構,我們可以看到上面有一個用黃色、藍色、紅色的小球表示小分子抑製劑,這個抑製劑可以非常好地抑製SARS主蛋白酶的活性,也就是說它很有可能成為一個抗SARS的藥物。
但是從2003年到現在,這個故事仍然是未完待續。為什麽?因為我們現在找不到SARS病人做臨床了,所以這個藥物不能走下去了。其實它說明了一個很簡單的道理:基於結構的藥物設計也好,或者其他藥物設計方法也好,都只是在藥物研發長河中,非常上遊的一小段,而下遊還有很多的事情需要其他的研究組、實驗室、製藥公司參與進來共同完成的。
第二個例子是我從美國回國之後,這兩年所做的研究工作之一,這個工作跟艾滋病毒有關係的。右邊的圖展示的是艾滋病毒侵染人體細胞的示意圖,其中非常關鍵的一個蛋白叫做GP41,就是圖中間細細的螺旋。
實際上,已經有一種藥物叫做T20,它可以抑製艾滋病毒的侵染,而它抑製的機制就是這個T20模擬了GP41上的一小段。正是因為這個模擬出了問題,一個艾滋病人的體內已經有了認識GP41的抗體,當T20進來以後,這些抗體會把它當成病毒的蛋白消滅掉,所以這個藥物在人體內會非常容易被清除。
我們組做這個課題的時候就在想:有沒有辦法找到一個完全人工設計的多肽序列,使得它能夠起到T20的作用,卻又不會被人體識別呢?我們的確做到了這件事情。實際上我們從AP1到AP2到AP3,改進了三版的多肽藥物,到AP3的時候藥效已經超過了T20。
從整體形狀來說,它們跟T20都非常相像,但我們並沒有就此滿足,又進一步對AP3進行小小的修改。我們把尾部的三個氨基酸殘基做了一個調整,結果它們不再形成螺旋,而是甩出去形成一個勾子,正是這個勾子使得藥物能夠和GP41有一個比T20更強的結合能力。實際上,我們的這版藥物在實驗中表現出比T20強一個數量級藥效。接下來還要進行動物實驗、臨床實驗等等,就不是我們實驗室所能做的事情了。
到此為止,我們已經回答了“藥從哪裡來?”這個問題的第一個層面:藥從哪裡來?從最初偶然發現到後來的意外得之,再到現在我們基本上可以做到“指哪打哪”。
但是還包括了第二個層面的問題:如果我的疾病已經有藥物可以醫治它了,可是我沒有錢買,或者我有錢但是買不到,怎麽辦?
在這裡就我們不得不提到仿製藥的概念了。還是要說說萬艾可,它的專利在2014年過期了,去年我們國家20多家藥企提出要生產萬艾可的仿製藥,最終獲得批準的藥企在藥物上市之後的市場佔有率,現在已經超過了萬艾可。大家可能會說:“這很好啊,仿製藥就是春天,仿製藥就是救命稻草。”但事實真是這樣嗎?
我們再來看看格列衛這種藥物。格列衛的藥物專利今年到期,但是他們藥企成功申請延期兩年,更要命的是它的藥物結晶形式將於2019年到期,如果他們再申請延期兩年,那就意味著在2021年之前我們國家沒有任何一家藥企可以合法的生產格列衛的仿製藥。
面對這種狀態大家可能會說,那我們不吃仿製藥,就吃格列衛好了,但你可能吃不起。在2003年,格列衛用藥一年需要花費3萬美元,在2012年需要花費9萬2千美元,而今天的價格還要更高,這絕對不是普通家庭可以負擔得起的。
藥物價格為什麽這麽高?其中的原因有很多,我們今天要談的是技術方面的原因。藥物研發是非常漫長的過程,裡面牽扯很多環節,投入巨大。通常一個新藥在美國需要研發十多年時間,並投入十多億美元。
另外一方面,藥物研發的成功率太低了,一百個課題能有一個最終走到藥物就不錯了,另外99個失敗課題的研發成本都需要這一個成來的承擔。第三個原因是,專利技術壟斷使得藥企可以隨意地抬高藥價。
那我們不要專利了,忽視它不就行了嗎?實際上的確有人這樣做,咱們的鄰居印度就是世界第一大仿製藥國,他們的政府會以法令形式宣布某個藥關係到國計民生,非常重要,可以無視它的專利保護,於是他們的藥企就可以隨便生產這種仿製藥了。
那我們能這樣做嗎?歷史告訴我們,尊重知識產權是保護創新能力最基本的條件,這個問題上我們不可能開歷史的倒車。我們該怎麽辦?我個人認為解決方案仍舊在於科學技術的進步。
大家可能會覺得,科技發展之後,那些科學技術變得越來越酷炫,越來越高深莫測,是不是能夠研究的人變得越來越少了?其實不是這樣的。
舉個例子,在基因測序這件事情上,在世紀之初的時候,我們全世界的基因組科學家集合在一起,測了一個人類樣本的基因組。而現在只要花不到一萬塊錢,一周的時間,世界上很多實驗室,包括中國的實驗室,都可以幫你測你自己的基因組,這就是技術進步帶來的結果。
我們回到結構生物學這個領域。大家可能不知道,半個世紀以前我們的結構生物學是全球領先的水準,但那時候只有我現在所在的生物物理所,有屈指可數的幾個組做結構生物學。今天,隨著這個學科的不斷發展,技術門檻在不斷降低。
現在,全國將近200個實驗室都有能力做結構生物學研究。我們假設每個實驗室有五個藥物研發相關的課題,那就是一千個課題,這一千個課題中如果只有十分之一的成功,我們就將獲得一百個藥物先導化合物。
那麽把這一百個藥物先導化合物交給製藥公司之後,最終我們得到的或許只是兩三個真正成功的藥物。但我告訴大家,這已經非常多了。為什麽這麽說?我們國家到現在為止真正自主知識產權的創新藥物只有不到十個。
在這樣一種我稱之為“眾籌”的模式下,其實藥物研發的前期研究成本和前期研究風險都被平攤了。第二個好處,因為參與的研究組非常多,所以有著很強的選題多樣性,而且在每個課題上更具專業性。
第三點,這種方式整體上提高了我國自主創新藥物的研發能力,這意味著我們的藥企,特別是我們的病人,再也不用翹首以盼地等著別人的專利過期的日子了。

最後,我想用唐朝著名醫學家和藥物學家孫思邈的一句話,來結束我今天的演講。他在著作《千金要方》中寫到:“若有疾厄求救者,不得問其貴賤貧富,長幼姸媸,怨親善友,華夷愚智,普同一等,皆如至親之想。”
我想,在看病這件事情上,我們現在已經能夠做到“不問貴賤貧富”了,但是在用藥這件事情上,我們每個人的財富水準仍舊在很大程度上製約著用藥的種類和數量。我相信,隨著科技的進步,當然也包括其他方方面面的努力,在不久的將來,我們能夠做到“不問貴賤貧富,病者皆得其藥”。
SELF講壇全稱“SELF格致論道”講壇,是中國科學院全力推出的公益講壇,由中國科學院電腦網絡資訊中心和中國科學院科學傳播局聯合主辦,中國科普博覽承辦。SELF是 Science, Education, Life, Future的縮寫,旨在以“格物致知”的精神探討科技、教育、生活、未來的發展,嘗試打破過去純粹以“知識傳播”為主的科普形式,專注於思想的傳播,力圖從思想的源頭上促進公眾參與科學的積極性。關注微信公眾號SELFtalks獲取更多資訊。
本文出品自“SELF格致論道講壇”公眾號(SELFtalks),轉載請注明公眾號出處,未經授權不得轉載。