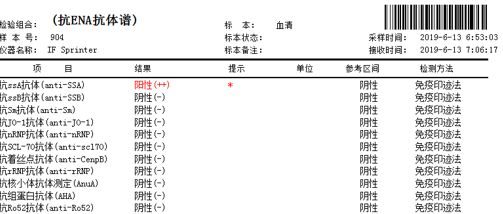
人的胃腸道內寄居著種類繁多的微生物,這些微生物稱為腸道菌群,其數量達10兆,包括正常菌群和過路菌群。它們與人體功能代謝和免疫系統共同進化,在維持系統平衡中至關重要。
腸道菌群紊亂可增加類風濕關節炎

有研究發現,腸道菌群紊亂可增加類風濕關節炎(rhrumatoid arthritis,RA),且與其發生髮展也有著密切的關係。在正常情況下,腸道菌群按一定的比例組合,各菌間互相製約,互相依存,在質和量上形成一種生態平衡。
當腸道菌群紊亂時,機體內環境發生變化,自身組織或抗原失去正常的免疫耐受能力,腸壁淋巴組織的動態平衡被打破,分泌一些新的炎症介質或原本分泌的炎症介質數量增多。
最終導致一系列的局部乃至全身的病理性免疫應答,大量自身抗體錯誤識別並攻擊自身組織,導致免疫系統出現障礙以及代謝的改變和各種疾病的發生。
腸道微生態多樣性降低誘導炎症發生


RA是一種以滑膜炎為病理基礎的系統性自身免疫性疾病。越來越多的證據揭示了腸道菌群紊亂與RA的關聯。
早在20世紀就有學者提出關於腸道菌群紊亂與RA之間的毒血症因子假說,認為腸道G細菌大量增殖,會導致腸道產生多種毒性代謝產物並進人血液循環,引起關節炎。
Vaahtovuo等研究人員通過對患者糞便組成分析,比較了早期RA和纖維肌痛(FM)患者腸道菌群的組成,發現RA患者糞便裡的雙歧桿菌、牙齦卟啉單胞菌菌群、脆弱擬桿菌、直腸球形梭菌群均顯著低於FM。
近年也有研究者發現,RA患者腸道微生物的多樣性降低,但放線菌門卻增加了。RA患者腸道細菌的變化,提示腸道菌群的紊亂可能誘導或者促進了RA的發生髮展。
乳酸桿菌可以有效緩解RA患者的病情
Shinebaum等研究人員研究發現,RA患者糞便中的產氣莢膜梭菌含量顯著多於正常組,並與RA病情活動程度相關,活躍期的RA梭狀芽孢桿菌含量顯著高於穩定期的RA,提示產氣莢膜梭菌可能參與了RA的發生髮展,並可用於疾病治療效果或者抗炎藥物療效的評估。
Gregersen等研究人員指出,在RA患者滑膜中能夠分離耶爾森菌屬等腸道菌的抗體,並認為外來抗原與人體自身抗原結構相似導致抗原交叉反應,發揮相似的免疫調節或抗原提呈功能,能夠增加RA的易感性,誘導與激活機體自身免疫應答,從而引起RA的發生髮展。
Round等研究人員認為,脆弱類桿菌能夠刺激調節性T細胞分泌IL-10製Th1細胞的激活,起到免疫抑製功能。Vaghef-Mehrabany等臨床研究顯示,乾酪乳桿菌可顯著降低RA患者血清TNF-a、IL-6和IL-12等促炎細胞因子,同時提供IL-10等抗炎因子水準。
副乾酪乳桿菌可以顯著降低RA的活動性,證明了乳酸桿菌可以有效緩解RA患者的病情。而Sjogren等研究指出,脆弱類桿菌與雙歧桿菌數量減少可以阻礙黏膜免疫系統的發育成熟,影響機體免疫功能,由此表明腸道菌群紊亂與RA的發生髮展是息息相關的。
益生菌補充劑改善RA患者臨床癥狀和代謝水準
有學者在做體外實驗研究發現,腸道細菌細胞壁產物肽聚糖能夠激發細胞因子的釋放,激發RF的分泌。Gomez等動物實驗發現,關節炎易感HLA-DRB1*0401小鼠腸道菌群主要是厚壁菌,而抗炎HLA_DRBl*0402小鼠腸道有大量的擬桿菌和放線菌。
Zamani B等研究顯示,予以RA患者服用8周益生菌膠囊,患者28個關節疾病活動評分有明顯改善,且血清胰島素水準、HOMA-B和hs—CRP水準顯著降低,說明益生菌補充劑能改善RA患者臨床癥狀和代謝水準。
臨床上,以腸道菌群一腸關節軸為治療靶向的治療方案早已應用,比如目前臨床上應用的改善病情的抗風濕葯柳氮磺胺吡啶等,均顯示出明顯療效。
?總之,腸道菌群紊亂在類風濕關節炎的發生和發展中起著重要作用,有的細菌有保護作用,而有的是促進作用。