12月21日,耶魯大學陳列平教授團隊(第一作者為王俊博士)在國際頂級期刊Cell上發表了題為Fibrinogen-like Protein 1 Is a Major Immune Inhibitory Ligand of LAG-3的論文,證明了纖維介素蛋白1(Fibrinogen-like protein 1, FGL1)是LAG-3的一個重要的功能性配體,並揭示了該LAG-3-FGL1通路在腫瘤逃逸中均起到令免疫系統「剎車」的作用,並以從免疫檢查位點的不同方面啟動免疫抑製。

這個發現或許可以解釋現有免疫療法在很多患者中無法發揮作用的原因。更重要的是,對於腫瘤新型免疫逃離線製的解析,將幫助我們攻克更多類型的癌症,使越來越多更多的患者受益!

陳列平教授簽名照
「只有25%-30%的腫瘤採用PD-1/PD-L1通路來抑製免疫反應,而其他腫瘤用了另外的分子通路或機理來逃脫免疫反應的攻擊,對於這些機理我們知之甚少。」陳列平教授說道。
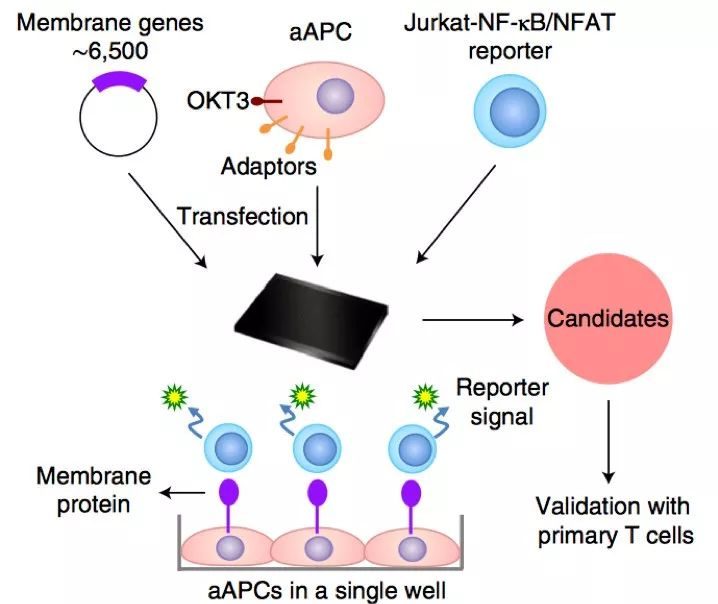
陳列平團隊在此研究中,首先利用他們團隊的Genome-scale receptor array(GSRA)技術來篩選LAG-3的結合蛋白(圖1)。借這個技術平台以快速檢測蛋白與蛋白之間的相互作用,篩選出一種名為FGL1的分子,它能夠於LAG-3緊密結合。

圖1 GSRA篩選LAG-3結合蛋白示意圖
然後,研究者分別在FGL1基因敲除FGL1-KO和LAG-3基因敲除LAG-3-KO小鼠中構建MC38腫瘤模型。最終在小鼠腫瘤模型中發現,不論是通過基因敲除還是抗體阻斷,阻斷FGL1-LAG-3相互作用都可以通過刺激腫瘤微環境中T細胞的活化和增值來提高機體對腫瘤的免疫與清除。
但問題是FGL1主要表達在肝臟和胰腺內,這和腫瘤又有什麼關係呢?
研究人員隨後對腫瘤資料庫進行了生物資訊學的統計分析,他們發現包括肺癌、乳腺癌、結腸癌等實體腫瘤FGL1的表達均被上調,這就可以一定程度的解釋FGL1與LAG-3結合啟動腫瘤免疫抑製的說法。
總之,本研究發現並證明了FGL1-LAG-3是腫瘤免疫逃逸的一條新通路,且可作為腫瘤免疫治療的潛在靶點,為免疫療法補充一塊重要的拚圖,或許可以解決現在PD-(L)1抑製劑療效不足的問題,使得免疫治療更加完善,讓更多的患者受益!
值得一提的是,陳列平教授今年10月份在Cell上發表了一篇題為A Paradigm Shift in Cancer Immunotherapy: From Enhancement to Normalization的重要綜述,特彆強調了「免疫正常化」的概念最終指導未來腫瘤免疫療法的設計。