2021美國肝病大會上(2021年11月12日至15日進行),研究人員公布了一款小干擾RNA分子(siRNA)AB-729的臨床試驗數據。AB-729是加拿大楊梅生物製藥公司(Arbutus Biopharma) 正在臨床開發用於治療慢性B肝病毒感染的基因沉默療法RNAi藥物。

在研B肝新藥AB-729,重複給藥後,可維持HBsAg穩健下降
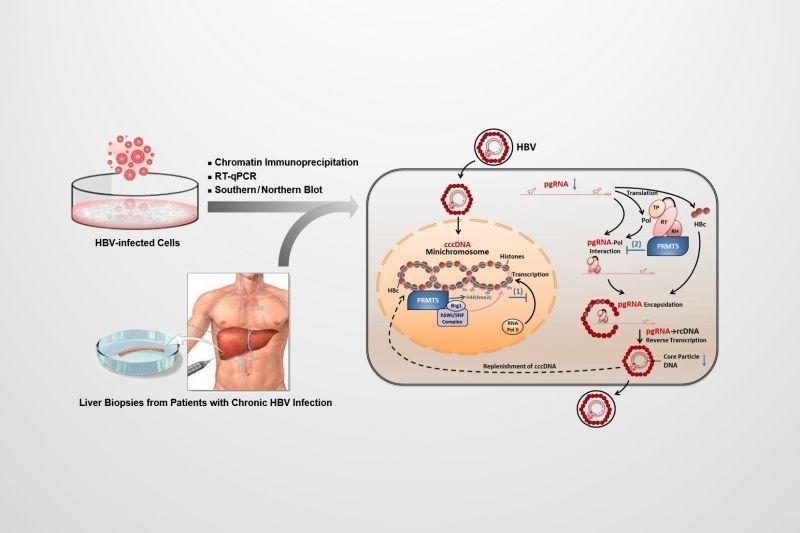
一、基因沉默RNAi療法
研究人員介紹,AB-729是一種N-乙酰半乳糖胺 (GalNAc) 偶聯的單觸發RNA干擾在研B肝新藥,可阻斷所有HBVRNA轉錄物,包括HBx,從而抑製B肝病毒複製和所有病毒抗原的水準。目前,AB-729正處於2期臨床開發階段。
在AB-729-001研究第3部分,有34名非肝硬化、B肝e抗原(HBeAg)陽性或陰性的慢B肝受試者,接受每4周1次給藥AB-729 60毫克組(Q4W,隊列 E,N=7),每8周60毫克組(Q8W,隊列) F,N=7),90毫克組 Q8W(隊列 I(N=6)和 G(N=7)),或每12周 90毫克組(Q12W,隊列 J,N=7)到第24周。
第1天,隊列G為HBVDNA+,並啟動TDF;所有其他隊列均在穩定的核苷(酸)類似物治療中受到病毒學抑製。符合條件的受試者(第20周B肝表面抗原水準降低>0.5 log10),可以繼續選擇AB-729到第48周:隊列E切換到AB-729 60mg Q12W,而其余隊列保持其初始方案。受試者在AB-729停藥後隨訪48周。
來自:2021年美肝會,停用 GALNAC-siRNA分子AB-729後,HBsAg水準保持低水準

二、重複給藥AB-729,可維持HBsAg穩健下降
結果表明,符合延長治療條件的34/34名受試者中,有33名受試者同意延長治療時間。迄今為止,觀察到各隊列的B肝表面抗原平均下降幅度相似(通過ANCOVA檢驗結果為p>0.05),在第20周後觀察到B肝表面抗原平均下降幅度趨於平穩狀態。
研究進展到目前為止,已有25/34 (74%) 受試者的B肝表面抗原(HBsAg)水準低於100 IU/mL,有可用數據的隊列E和隊列F中,分別有 3/7 和 3/5 受試者在最後一劑AB-729給藥後,上述表面抗原抑製效果可維持長達20周和16周。隊列G中,6/6名受試者在第24周時,HBVDNA無法定量有報告的數據。
安全性方面,沒有因不良事件導致的死亡或停藥。出現1名與藥物不相關的3級大腿囊腫破裂;所有其他不良事件均為1級或2級。最常見的不良事件與注射部位相關(發紅、疼痛或瘀傷,分別為 N=4、N=4 和 N=3事件);且均為1級,無劑量或間隔依賴性。
來自:楊梅製藥公司B肝新藥研發管道,可見RNAi機理AB-729正在進行2期研究中

三、安全性及有效性數據積極
研究人員給出的這項臨床研究結論是,重複給藥AB-729後,通常具有良好安全性與耐受性。重複給藥AB-729,B肝表面抗原水準維持平均穩健下降!目前為止,在劑量和或給藥間隔之間沒有觀察到有意義的差異。在使用最後一劑AB-729給藥後的20周內,一些受試者的表面抗原抑製程度保持在<100 IU/mL!這些數據支持AB-729作為實現功能性治愈HBV的基石聯合療法進行持續評估。
小番健康結語:這是一項剛剛在2021年美肝大會上,研究人員發表的進展。目前,在研B肝新藥AB-729正在進行第2期臨床試驗當中。這些數據旨在說明,在接受核苷(酸)類似物治療的慢B肝受試者中,停用AB-729後,受試者的表面抗原依然保持在低水準!研究已發表在2021年美肝會上。
目前,AB-729正進行多項組合用藥2期臨床試驗中,包括AB-729+核苷類或(PEG-IFN)α-2a、AB-729+vebicorvir(VBR,核心抑製劑)+核苷類、AB-729+ATI-2173+TDF、AB-729+VTP-300+核苷類(最後這項研究2022年初開始)。返回搜狐,查看更多
責任編輯: