一年前(2018年7月)《我不是葯神》上映後引發熱議,使大眾對癌症及「救命葯」有了更深入的認識;3個月後著名主持人李詠因癌去世,讓大眾倍感惋惜。對於癌症這一奪命殺手,幾乎家喻戶曉,但對於癌症的發病機制,目前尚不明確,這使得癌症治療困難重重。
科學家和臨床醫生從未停止過對癌症治療方法的開發和探索,但遺憾的是,目前不但尚無一種方法能夠完全治癒癌症(我們平時所說的癌症治癒,一般指的是患者5年內無複發)。而且,治療方法本身還存在著一定的缺陷,比如化療、放療,在殺傷腫瘤細胞的同時也會損害到正常細胞。
是否有一種方法,可以隻殺傷癌細胞而不破壞正常細胞呢?
2019年4月24日刊登於 Nature 的一篇文章,或可為這一治療理念提供新思路。原文題目為NAD metabolic dependency in cancer is shaped by gene amplificationand enhancer remodelling。

圖/Nature官網
煙醯胺腺嘌呤二核苷酸引關注
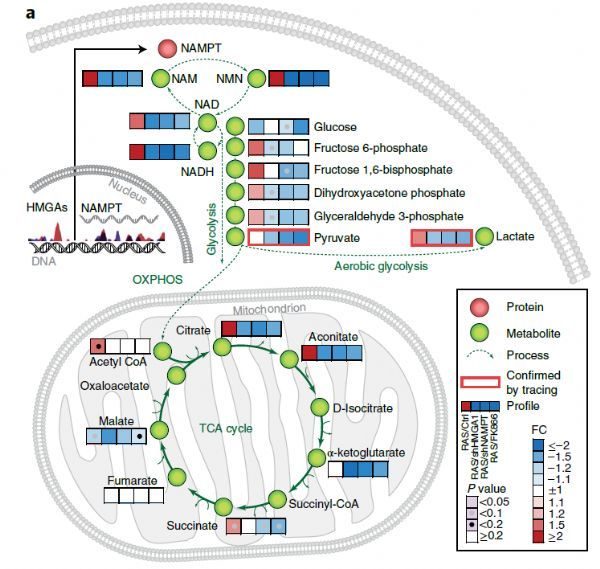
來自美國路德維格癌症研究所的SudhirChowdhry等研究人員關注到一種在代謝過程中,氧化還原反應所必需的小分子輔助因子——煙醯胺腺嘌呤二核苷酸(NAD)。NAD攜帶高能電子,通過氧化型NAD和還原型NAD,促進氧化磷酸化;同時,作為NAD依賴型酶的底物,NAD能夠將細胞代謝與表觀遺傳調控和DNA損傷修復聯繫起來。
NAD在哺乳動物的正常細胞中有三條合成途徑:
- 從色氨酸(Tryptophan)開始的從頭合成途徑
- 從煙酸(NA)開始的Preiss–Handler(PH)途徑
- 煙醯胺(NM)或煙醯胺核苷(NR)的補救合成途徑

圖1 NAD在哺乳動物正常細胞中的三條合成途徑
NAD在癌細胞中的合成途徑特殊
研究人員分析了19種組織的7000多個腫瘤樣本和2600個與之匹配的正常樣本(對照樣本),結合數學模型,開展廣泛的體外(細胞)、體內(裸鼠)研究。
結果發現,NAD在癌細胞中僅有一條合成途徑,而不同發病部位的癌症NAD的合成途徑不同。如:卵巢癌、攝護腺癌、胰腺癌等PH擴增的癌細胞系僅依賴PH途徑[限速酶:鹽酸磷酸核糖轉移酶(NAPRT)];而肺癌等非PH擴增的癌細胞系完全依賴於挽救合成途徑[限速酶:煙醯胺磷酸核糖轉移酶(NAMPT)。
癌症精準治療新思路
進一步研究發現,PH途徑和挽救合成途徑的限速酶抑製劑能夠使癌細胞內的NAD水準下降,導致完全、持續的腫瘤消退和大量的腫瘤細胞死亡。
與NAD在癌細胞僅一條合成途徑不同,正常細胞因能夠通過三條合成途徑中的任何一條維持細胞內NAD水準,故受到限速酶抑製劑的影響很小。

該研究提示不同發病部位的癌細胞中NAD的合成途徑不同,通過阻斷這一途徑,殺死癌細胞或可成為未來精準腫瘤學消滅癌細胞,且不傷害正常細胞的研究方向,為癌症治療提供了新的思路。
縮略詞
NAD:nicotinamide adenine dinucleotide 煙醯胺腺嘌呤二核苷酸
NAAD:nicotinic acid adenine dinucleotide煙酸腺嘌呤二核苷酸
NA:nicotinic acid 煙酸
QA:quinolinic acid 喹啉酸
QAPRT:quinolinic acid phosphoribosyltransferase 喹啉酸磷酸核糖轉移酶
NAMN:nicotinamide adenine dinucleotide nicotinic acid mononucleotide煙酸單核苷酸
NADSYN1:synthetase 1煙醯胺腺嘌呤二核苷酸合成酶1
NM/NAM:nicotinamide 煙醯胺
NR:nicotinamide riboside 煙醯胺核苷
NMN:nicotinamide mononucleotide 煙醯胺單核苷酸
NMNAT:nicotinamide mononucleotide adenylyltransferase 煙醯胺單核苷酸腺苷醯轉移酶
NAPRT:Nicotinate phosphoribosyltransferase 鹽酸磷酸核糖轉移酶
NAMPT:nicotinamide phosphoribosyltransferase 煙醯胺磷酸核糖轉移酶
參考文獻
[1] Sudhir Chowdhry, Ciro Zanca, Utkrisht Rajkumar, et al.NAD metabolic dependency in cancer is shaped by gene amplification and enhancerremodelling. Nature. 2019; 1-6.