近期,全球跨國製藥龍頭葛蘭素史克旗下B肝在研新藥GSK3228836完成Phase 2b臨床登記,此前該藥已經完成Phase 2a。試驗題目為第2期多中心、隨機、部分盲平行隊列研究,用於評估GSK3228836治療慢性B肝的有效性和安全性,最新發布時間是2020年6月26日,尚未開始招募。

B肝在研新藥GSK3228836,24周評估安全有效性,Phase2b臨床登記
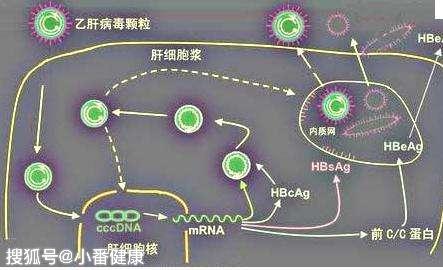
GSK3228836,是一種基於反義寡核酸設計用於降低B肝病毒重複感染,其中重點包含降低B肝表面抗原水準的反義創新藥。前期公開信息顯示,該藥在未接受任何治療的慢性B肝患者(CHB)和曾經接受核苷類藥物治療的CHB,該藥均表現出良好靶向性。這次2期後半部分研究,重點評估GSK3228836治療後,能否持續讓CHB獲得病毒學應答,葛蘭素史克本次試驗具體考量指標如下:

B肝表面抗原小於定量下限和血清HBV-DNA小於定量下限可以維持24周。本次2期試驗後半部分,還將繼續跟蹤該藥的4種方案中的安全性、藥效學、藥代動力學以及耐受性。初步估算本試驗將有440名參與研究,分為2個不同隊列,接受穩定的核苷類藥物和未曾接受核苷類藥物治療的參與者,每個隊列參與者會被隨機分配到4個不同組接受GSK3228836治療。
根據美國臨床試驗數據庫原文(上方英文截圖),該藥物第2期b試驗預計會在2020年8月28日啟動,初步推算完成日期:2022年4月1日,全部完成日期:2023年10月。根據葛蘭素史克本次試驗內容中,GSK3228836是一種無色至微黃色透明狀注射溶液,部門劑量強度是150毫克/毫升,不同劑量組按照每周皮下注射1次給藥。
2期試驗隊列1為300毫克的GSK328836+核苷類治療,符合條件的參與者會在第4天和第11天接受300毫克GSK328836,按照每周1次,治療24周;曾經接受核苷類藥物治療的慢性B肝符合條件參與者,在第4天和第11天每周服用1次300毫克GSK328836,治療12周,並在第4天和第11天服用300毫克GSK328836,每周1次,治療12周,隨後按照劑量逐步遞減至150毫克。

核苷類治療,主要指參與者在進行新藥研究中,還將繼續使用核苷類藥物治療,而安慰劑GSK3228836是一種無色透明注射液,每周採用皮下注射1次,單劑量強度150毫克/毫升。試驗入選標準:年滿18歲者,篩查前需記錄慢性B肝病毒感染持續超過或等於6個月,並且沒有接受過核苷類藥物治療;或在接受篩選前6個月,已經結束核苷類藥物治療;血清或血漿B肝表面抗原水準大於100IU/mL。
血清或血漿HBV-DNA水準:對未曾接受核苷類藥物治療者,HBV-DNA大於2000Iu/mL;接受過核苷類藥物治療者體內病毒載量已經被強效抑製,即HBV-DNA小於90Iu/mL;血清轉氨酶水準:對未接受核苷類藥物治療者,轉氨酶小於3倍ULN的最初將被納入。假如,得到獨立數據監測委員會同意的安全性數據後,轉氨酶標準可以適當擴大至小於5倍ULN;轉氨酶小於等於接受持續核苷類藥物治療的受試者,轉氨酶水準需小於等於2倍ULN。

小番健康結語:回顧一下關於B肝全新靶點,反義分子,英文名:Antisense Molecules。反義分子作用機制和RNAi近似,主要通過和體內B肝病毒mRNA結合來阻止轉化成為B肝病毒蛋白,進而是一種目前全球前沿的抑製B肝病毒複製方法。關於GSK328836的亮點:葛蘭素史克旗下目前有2種反義分子B肝在研新藥,這是其中一種2020年6月26日完成登記,公司預計會在今年8月28日完成所有2期後半部分招募並啟動。
GSK328836的2期前半部分研究數據顯示,受試者在第1天、第4天、第11天、第15天、第22天採用該藥皮下注射進行比較安慰劑持續4周治療,至第29天治療時,B肝表面抗原水準下降程度和該藥使用劑量呈直接相關性,有3名受試者的表面抗原水準大於3.0 log10 IU / mL,其中2名B肝表面抗原降至定量之下。在完成全部治療後至少28天與102天,受試者的表面抗原水準繼續保持在低於定量之下,表面抗原下降和轉氨酶突發性升高有關。若希望了解本試驗全部內容,可到美國臨床試驗數據庫查看英文原文內容。返回搜狐,查看更多
責任編輯: