責編丨迦 漵
自身免疫性疾病是人體的免疫系統錯誤地識別自身器官、組織和細胞,誘導免疫應答,繼而造成自身損傷的一類疾病。其發病率在整個人群中高達5%-8%,是位於心血管疾病和腫瘤之後的第三類主要疾病。目前已診斷的自身免疫疾病約有100種,常見的自身免疫疾病有:多發性硬化(multiple sclerosis,MS)、類風濕性關節炎(rheumatoid arthritis,RA)、自免疫性心肌炎(Autoimmune Myocarditis,AMC)、系統性紅斑狼瘡(systemic lupus erythematosus,SLE)、I型糖尿病、自身免疫性甲狀腺炎( autoimmune thyroiditis ,AITD)、銀屑病等。目前,大多數自身免疫疾病的發病機制還不明確,因此沒有完全治癒性的有效治療手段。臨床研究發現,自身免疫疾病發病的原位組織存在鐵離子的過量沉積【1】,如多樣性硬化病人的腦組織和風濕性關節炎病人的關節滑液等。但是,鐵離子沉積對這些疾病的發病中的功能仍然不清楚。
6月27日,上海交通大學醫學院/中科院上海生命科學研究院健康科學研究所常興研究組在Immunity上在線發表了題為Iron drives T helper cells pathogenicity by promoting RNA-binding protein PCBP1- mediated proinflammatory cytokine production的研究論文,發現了輔助性T細胞中鐵代謝通過調控促炎性細胞因子表達參與自身免疫疾病,並證明RNA結合蛋白PCBP1介導的轉錄後調控途徑為連接鐵代謝與細胞因子表達的調控的橋樑。


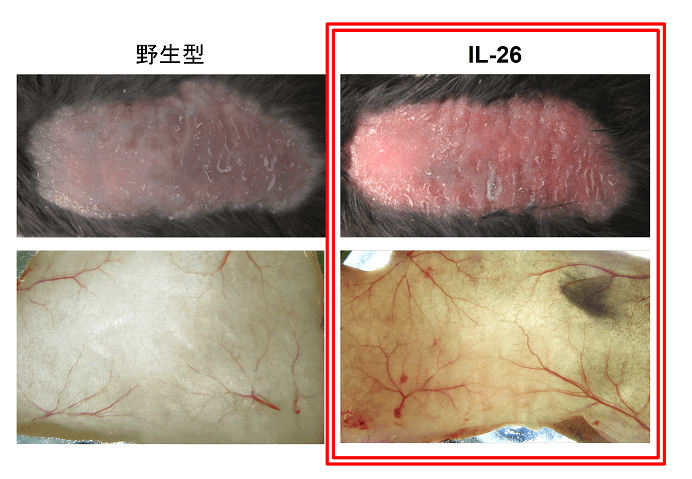
在這項研究中,研究人員首先發現,無論利用鐵離子敖合劑或基因缺陷小鼠改變T細胞中鐵離子含量,都會影響促炎性細胞因子(如GM-CSF,IL2等。GM-CSF-Granulocyte-macrophage colony-stimulating factor粒細胞-巨噬細胞集落刺激因子)的表達,進而影響多樣性硬化的小鼠模型EAE(實驗性自身免疫性腦脊髓炎experimental autoimmune encephalomyelitis,EAE,是目前公認的研究人類MS的動物模型)的發生。有趣的是,鐵離子對促炎性細胞因子的調控主要在轉錄後水準,通過影響促炎性細胞因子的mRNA的穩定性來實現。
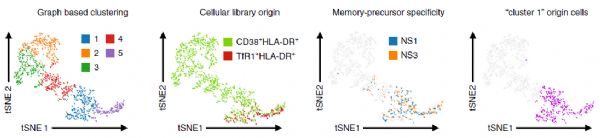
細胞因子表達調控的重要機制是RNA結合蛋白介導的轉錄後調控。隨後,研究人員利用高通量shRNA篩選,鑒定出具有鐵離子伴侶蛋白功能的RNA結合蛋白PCBP1可能參與該過程。T細胞中PCBP1缺陷與鐵離子缺陷類似,可以抑製GM-CSF的表達和EAE發生。更進一步的機制研究發現,PCBP1直接結合mRNA 3』UTR中富含UC的序列,促進GM-CSF等mRNA的穩定性和表達, 而通過CLIP(紫外交聯免疫沉澱結合高通量測序)等實驗也證明在全基因組水準PCBP1直接結合一些mRNA 3』UTR區富含UC的序列; 而鐵離子保護PCBP1蛋白不被Caspase剪切降解,增強靶基因mRNA的穩定性、促進促炎性細胞因子的產生, 提示PCBP1可以作為胞內鐵離子的感測器,調控免疫細胞轉錄組的動態變化和致病性。


該研究鑒定出調控GM-CSF表達的新的順式作用元件,及其相關的反式作用因子PCBP1,揭示了GM-CSF新的轉錄後調控機制;同時豐富了代謝環境通過RNA結合蛋白轉錄後調控基因表達的模型;闡釋了鐵代謝異常促進自身免疫疾病的機制,為多發性硬化等自身免疫疾病的治療提供的新的靶點和思路。
常興研究員是本文通訊作者,博士後王志章是本文第一作者。
參考文獻:
1、Ganz, T., & Nemeth, E. (2012). Hepcidin and iron homeostasis.Biochimica et Biophysica Acta (BBA)-Molecular Cell Research, 1823(9), 1434-1443.
BioArt,一心關注生命科學,只為分享更多有種、有趣、有料的資訊。關注投稿、合作、轉載授權事宜請聯繫微信ID:fullbellies 或郵箱:[email protected]