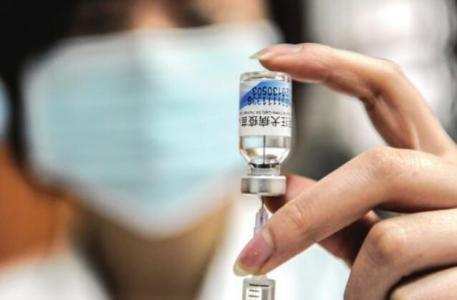
李克強就疫苗事件作出批示:國務院要立刻派出調查組
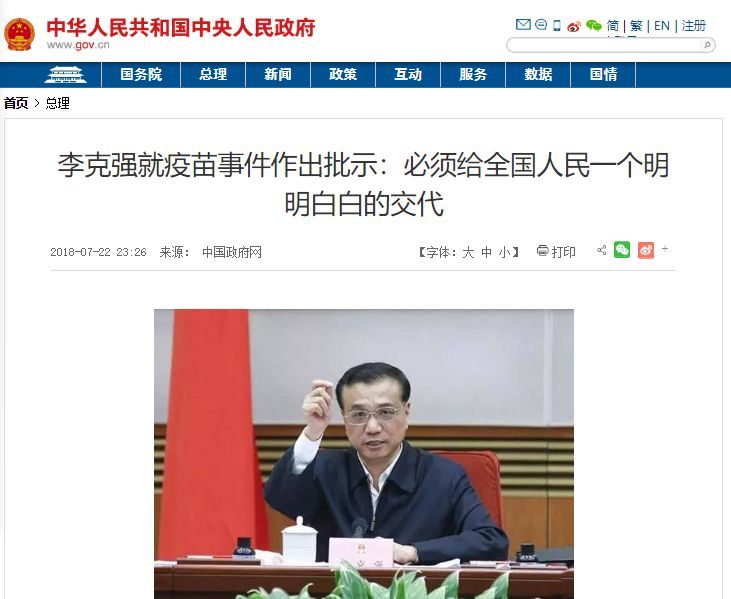

據7月22日中國政府網消息,李克強總理就疫苗事件作出批示:此次疫苗事件突破人的道德底線,必須給全國人民一個明明白白的交代。李克強在批示中要求,國務院要立刻派出調查組,對所有疫苗生產、銷售等全流程全鏈條進行徹查,儘快查清事實真相,不論涉及到哪些企業、哪些人都堅決嚴懲不貸、絕不姑息。對一切危害人民生命安全的違法犯罪行為堅決重拳打擊,對不法分子堅決依法嚴懲,對監管失職瀆職行為堅決嚴厲問責。儘早還人民群眾一個安全、放心、可信任的生活環境。
此前7月16日,李克強已就疫苗事件作出批示,要求徹查。
「長春疫苗事件」最新進展:
目前,國家葯監局已要求吉林省食品藥品監督管理局收回該企業《藥品GMP證書》,責令停止狂犬疫苗的生產,責成企業嚴格落實主體責任,全面排查風險隱患,主動採取控制措施,確保公眾用藥安全。吉林省食品藥品監督管理局調查組已進駐該企業,對相關違法違規行為立案調查。國家藥品監督管理局派出專項督查組,赴吉林督辦調查處置工作。國家葯監局也表示,對發現的違法違規問題絕不姑息,堅決依法依規嚴肅查處,涉嫌構成犯罪的,一律移送警察機構予以嚴懲。
根據藥品管理法,藥品的生產企業未按照規定實施《藥品生產品質管理規範》的,給予警告,責令限期改正;逾期不改正的,責令停產、停業整頓,並處五千元以上二萬元以下的罰款;情節嚴重的,吊銷《藥品生產許可證》。
國家葯監局負責人22日通報了長春長生生物科技有限責任公司違法違規生產凍乾人用狂犬病疫苗案件有關情況。
根據舉報提供的線索,7月5日,國家葯監局會同吉林省局對長春長生公司進行飛行檢查;7月15日,國家葯監局會同吉林省局組成調查組進駐企業全面開展調查。7月15日,國家葯監局發布了《關於長春長生生物科技有限責任公司違法違規生產凍乾人用狂犬病疫苗的通告》。
現已查明,企業編造生產記錄和產品檢驗記錄,隨意變更工藝參數和設備。
上述行為嚴重違反了《中華人民共和國藥品管理法》《藥品生產品質管理規範》有關規定,國家葯監局已責令企業停止生產,收回藥品GMP證書,召回尚未使用的狂犬病疫苗。國家葯監局會同吉林省局已對企業立案調查,涉嫌犯罪的移送警察機構追究刑事責任。
按照疫苗管理有關規定,所有企業上市銷售的疫苗,均需報請中國食品藥品檢定研究院批簽發,批簽發過程中要對所有批次疫苗安全性進行檢驗,對一定比例批次疫苗有效性進行檢驗。該企業已上市銷售使用疫苗均經過法定檢驗,未發現品質問題。為進一步確認已上市疫苗的有效性,已啟動對企業留樣產品抽樣進行實驗室評估。
另據中國疾病預防控制中心監測,我國的狂犬病發病率近年來逐步下降。
葯監局已部署全國疫苗生產企業進行自查,確保企業按批準的工藝組織生產,嚴格遵守GMP生產規範,所有生產檢驗過程數據要真實、完整、可靠,可以追溯。國家葯監局將組織對所有疫苗生產企業進行飛行檢查,對違反法律法規規定的行為要嚴肅查處。
負責人說,該企業是一年內被第二次發現產品生產品質問題。去年10月,原食葯監總局抽樣檢驗中發現該企業生產的1批次百白破疫苗效價不合格,該產品目前仍在停產中,有關補種工作原國家衛計委會同原食葯監總局已於今年2月進行了部署。
事件回顧:
7月15日,國家藥品監督管理局的一則通告,將疫苗事件再次推上了風口浪尖!


該通告稱:根據線索,國家藥品監督管理局組織對長春長生生物科技有限責任公司開展飛行檢查,發現該企業凍乾人用狂犬病疫苗生產存在記錄造假等嚴重違反《藥品生產品質管理規範》行為。此外,通告顯示,本次飛行檢查所有涉事批次產品尚未出廠和上市銷售,全部產品已得到有效控制。
7月18日,國家衛生健康委疾控局局長毛群安表示,國家藥品監督管理局發布《關於長春長生生物科技有限公司違法違規生產凍乾人用狂犬病疫苗的通告》後,疾控局密切關注事態發展,與國家藥品監督管理局保持密切溝通。據了解,國家藥品監督管理局正組織對企業的調查工作。根據《狂犬病暴露預防處置工作規範》,沒有完成全程接種程式的,可以選用其他廠家的狂犬病疫苗按原接種程式繼續接種。
此後,涉事公司長春生物的一則公告又將輿論推向了高峰!


7月19日晚,長生生物發布公告稱,其子公司長春長生收到了《吉林省食品藥品監督管理局行政處罰決定書》。決定書指出,長春長生生產的「吸附無細胞百白破聯合疫苗」(批號:201605014-01)「效價測定」項不符合規定。效價指標不合格,意味著接種後可能會影響接種兒童的白喉、破傷風和百日咳的免疫效果。
相對來說,雖然狂犬病致死率極高,可發生率低,問題狂犬疫苗也沒有流通上市,但百白破疫苗出事,全國家長陷入了恐慌:
百白破是一類(免費)疫苗,用來預防百日咳、白喉、破傷風三種比較危重的疾病,必須接種;被查出有問題的批次高達65萬支,數量眾多,觸目驚心。
大眾關心的6個問題與答案
1事件相關的百白破疫苗到底出了什麼問題
百白破疫苗的主要問題是:效價指標不合格。
帶來的後果是,可能影響免疫保護效果,但對人體沒有危害。
國家葯監局公告顯示,百白破疫苗的主要問題,檢驗時發現 「效價測定」 項不符合規定。
國家衛生計生委和河北、山東、重慶三省(市)衛生計生部門在去年11月已經組織專家對該情況進行評估,並承諾根據評估結果將採取相應措施,妥善處理。
2事件相關的百白破疫苗流通向哪裡?
此次被曝出的百白破疫苗事件,實際上是去年年底的問題,具體包括兩個生產企業,長春長生生物科技有限公司和武漢生物製品研究所有限責任公司。
官方數據顯示,這批「問題疫苗」,長春產的主要流通到山東,武漢產的主要銷往重慶市、河北省。


3事件相關的狂犬疫苗流通向哪裡?
河南省疾控中心回應稱:涉事批次未上市。
4之前打過的長春長生狂犬疫苗有問題沒?
"根據國家通告,所有涉事批次產品尚未出廠和上市銷售,全部產品已得到有效控制。」河南省疾病控制預防中心免疫規劃所副所長張延煬說,之前市場流通的長春長生狂犬病疫苗均是國家葯監局檢測合格、允許市面上使用的疫苗,所以大家不要擔心。
根據中國疫苗上市有關規定,所有疫苗產品,無論是進口還是國產,都需要經過生物製品批簽發(以下簡稱批簽發)程式才能上市。每批製品出廠上市或者進口時都要進行強製性檢驗、審核,批簽發過程中的檢驗的項目包括疫苗體內外的效力、安全性、理化檢驗等,檢驗不合格或者審核不被批準者,不得上市或者進口。
國家食品藥品監督管理局主管全國生物製品批簽發工作,承擔生物製品批簽檢驗或者審核工作的藥品檢驗機構由國家食品藥品監督管理局指定。生物製品批簽發檢驗或者審核的標準為現行的國家生物製品規程或者國家食品藥品監督管理局批準的其他藥品標準。
此次狂犬疫苗門事件曝光後,長春長生髮布公告稱,為了保證用藥安全,公司正對有效期內所有批次的凍乾人用狂犬病疫苗(Vero細胞)全部實施召回。根據長春長生近幾年對該疫苗不良反應監測,未發現因產品品質問題引起的不良反應。
5打了【問題疫苗】後,會產生什麼後果?是否可能有後遺症?
這批疫苗,對人體的安全沒有影響,最大的風險在於可能失效,導致無法預防對應的疾病。
很多家長擔心孩子接種問題疫苗,會帶來其他後遺症。實際上,疫苗的常見不良反應包括局部的紅腫熱痛、發熱、過敏等,一般都比較輕微。而過敏等比較嚴重的情況,發生率很低,對大多數人來說,疫苗是安全的。
疫苗產生的不良反應,多發生在接種後的24~48小時內,後期再發,或者產生後遺症的可能性很小。
6如何確定是否接種了不合格的疫苗?萬一接種到涉事的百白破疫苗怎麼辦?
家長可以查看兒童預防接種證上的百白破疫苗接種記錄,對比疫苗生產企業和批號,也可以顧問當時的接種部門。
百白破疫苗需分別於 3、4、5月齡和18月齡各接種1劑次,共接種4次。
正常來說,完成4次接種的兒童可得到較好的保護效果:
預防典型百日咳的效力約85%;
破傷風的保護效力為80~100%;
接種3次以上,對白喉的保護效力約為95%。
而被曝出的兩批次百白破疫苗,效價指標不合格,可能影響免疫保護效果。
家長如果確定孩子接種的是涉事的百白破疫苗,可以結合孩子接種的次數和批次情況,向當地疾控部門或接種部門顧問,看是否要繼續補種。
兒童預防接種證的第一頁,標註了孩子戶口所屬接種部門的電話
▼


版權聲明
大河健康報
全 生 命 周 期 的 健 康 呵 護
專業|專註|大愛|責任
統籌:於素文
編輯:宋崑崙
實習編輯:曹葉
TAG: |