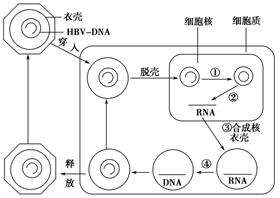
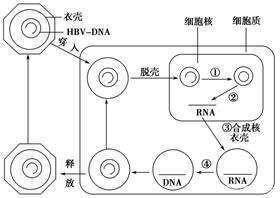
一些直接作用新型抗HBV藥物,正在臨床前或臨床研究階段,我們簡單科普一下,cccDNA抑製劑和核心蛋白變構調節劑(CpAM)分子藥物開發進展和作用機制。

B肝cccDNA抑製劑,存在早期遞送及成本問題,簡述在研藥物定位
目前,國內外對CpAM分子的開發熱情都很高,最近小番健康也持續科普了這個方向的藥物開發。NVR-3778是一款口服 II類CpAM分子,在其1期4周多中心、安慰劑對照臨床開發中,對HBVDNA調降能力有限,當進行組合療法研究時,研究人員使用了NVR-3778(每日2次,600毫克)+PEG-IFN的組合療法,結果表明,這種組合療法對HBVDNA產生了協同調降能力,平均調降 1.97 log。
然而,當停止這種組合療法後,所有受試者的HBVDNA和RNA水準恢復到基線水準,而且對B肝表面抗原、B肝核心抗原或B肝e抗原水準也沒有顯著調降作用。安全性方面,沒有觀察到嚴重不良事件。
正如,我們前面介紹的,CpAM分子設計沒有直接針對B肝表面抗原,但相關化合物在促使HBVDNA、HBVRNA或pgRNA方向,還是有一些積極研究數據支持這些化合物的進一步開發,但是,它們通常僅作為現有療法,如核苷類或干擾素的補充,而無法取代核苷類。通過最近科普,我們已經能夠看到已產生的相關CpAM分子仍有許多局限性。

讀者關心的另一個直接作用抗病毒藥物開發方向是cccDNA抑製劑。研究人員通常使用的是基因編輯三大工具來開發治療HBV新藥。以ZFN為例,它起初是使用鋅指結構域和Fok1核酸酶結構域設計的。鋅指結構域使用其基序識別 DNA 上的特定位點並與之結合。然後核酸酶修剪掉 DNA。
然而,由於ZFN的生產需要廣泛蛋白質工程,且需要為每個新基因組目標創建一個新的ZFN。因為應用這種技術需要比較高成本和時間周期長等特點,ZFN技術並沒有被全球多數研究人員認為是開發B肝創新藥有吸引力的方向。
基因編輯還有一種是TALENS,我們也將它稱為轉錄激活因子樣效應物核酸酶,是基因編輯核酸酶三大類之一。應用原理上,TALENS使用了轉錄激活因子樣效應子 (TALE) 蛋白的重複區域作為結合域和 Fok1 核酸酶用於其核酸內切酶的活性。想要實現這一目標,存在一定遞送問題(太大無法使用AAV載體包裝到所需細胞),並且要對每個DNA目標位點進行工程設計,也對特定的TALEN技術要求頗高。

小番健康結語:相信您已經看到全球B肝創新藥正朝著多方向進展,其中主要包括直接針對HBV生命周期和激活喚醒免疫兩大方向開發新藥。核心蛋白變構調節劑的開發相對進展積極,雖然這類化合物已有許多停止開發,主要集中在有效性方面沒有達到預期,但從開發策略看,這些化合物側重於作為現有療法的補充(NUC或IFN),而非替代藥物。
目前暫時沒有關注到cccDNA清除劑的藥物開發設計思路,全球的cccDNA抑製劑的開發進展還處在早期階段,一些基因編輯技術無論是在成本、遞送等方面都遇到了一些問題導致這一方向研究停滯。當然,開發針對HBV生命周期更多步驟的候選藥物,還是值得我們期待!因為它們也可能改變目前B肝藥物格局,尤其是進入抑製劑、衣殼組裝調節劑、PD-L1單抗以及靶向先天免疫的Toll樣受體激動劑等,它們的目標均是功能性治愈HBV;
從目標看,更高的B肝表面抗原清除率,應該是對這些藥物靶點所產生的候選藥物重要考核指標之一!同時,這些候選藥物無論是在作用機制或是單藥或組合療法中,還需要實現以有限時間功能性治愈HBV,這些定義高於現有NUC療法。簡單地講,全球對B肝在研新藥的考核更嚴格,它們必須在單藥或組合療法實現較高的B肝表面抗原清除且不會反彈,其他病毒標誌物正常化,不再讓慢B肝終身用藥(有限療法)。返回搜狐,查看更多
責任編輯: