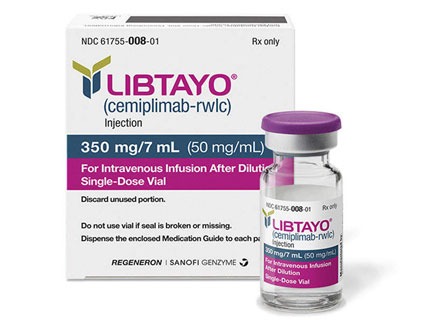
美國食品和藥物管理局(FDA)近日批準cemiplimab(商品名Libtayo,再生元製藥)用於治療轉移性皮膚鱗狀細胞癌(CSCC)或局部晚期不可切除的CSCC患者。
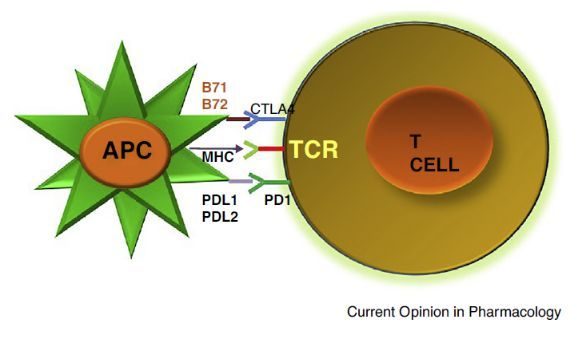
Cemiplimab是FDA首次批準專門治療CSCC晚期患者的藥物,它是一種針對PD-1路徑的靜脈注射免疫療法,可以幫助免疫系統對抗癌細胞。
「這種癌症到了晚期難以進行有效治療,所以要為患者找到新的治療方案。」FDA卓越腫瘤學中心主任、藥物評估和研究中心血液學和腫瘤學產品主任Richard Pazdur在一份新聞聲明中說。
Pazdur指出,這是第六種不同的免疫檢查點抑製劑,以FDA批準用於治療各種腫瘤(包括CSCC)的PD-1 / PD-L1途徑為靶點。「現在腫瘤學領域越來越關注並研製針對特定分子靶點的藥物。」
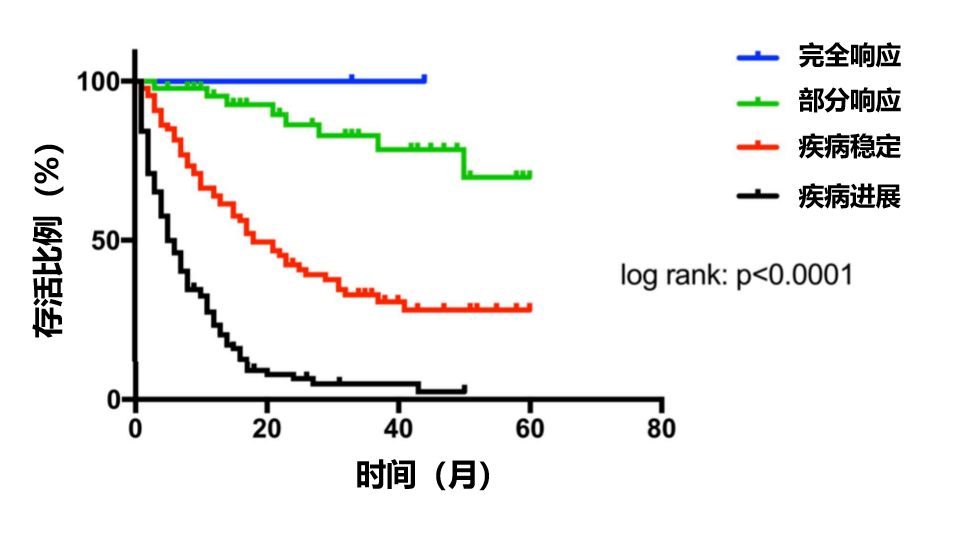
兩項開放標籤臨床試驗評估了cemiplimab的安全性和有效性,對108名患者(75名患有轉移性癌症,33名患有局部晚期癌症)進行療效評估。
近一半的患者(47.2%)cemiplimab治療有反應,這是該研究的主要終點。
cemiplimab的常見副作用包括疲勞、皮疹和腹瀉。與其他免疫療法一樣,該藥物可引起嚴重或危及生命的反應。這些包括免疫介導的不良反應風險,包括肺炎、結腸炎、肝炎和內分泌病以及皮膚病和腎臟問題。FDA表示,還應監測患者的點滴反應。
FDA表示,CSCC是美國第二大常見癌症,估計年發病率約為700,000例;大多數患者通過手術切除治癒。只有一小部分CSCC患者會進展到晚期,手術和放療沒有效果,是使用cemiplimab的適應證。