平台發布的臨床試驗資訊已經幫助不少患者成功入組試驗,目前接受報名的腫瘤相關臨床試驗也已經明顯擴增,覆蓋多種實體瘤(包括但不限於肺癌、乳腺癌、腸癌、甲狀腺癌、腺泡狀軟組織肉瘤等)。如果您身邊有合適參與臨床試驗的患者,請轉發給需要的他們!

多種實體瘤
1. 試驗簡介
評估皮下注射KN035單葯治療晚期實體瘤患者的安全性、耐受性、PK特徵和初步療效的單臂、劑量遞增I期臨床研究
2. 面向患者
包括但不限於:肺癌、乳腺癌、腸癌、甲狀腺癌、腺泡狀軟組織肉瘤等。
3. 關鍵入選標準
1)年齡18-75歲(含)男性或女性;
2)受試者必須經病理組織學確診的局部晚期或轉移性實體瘤患者,經標準治療無效(治療後疾病進展)或患者拒絕標準治療或無有效治療手段;包括但不限於:肺癌、乳腺癌、腸癌、甲狀腺癌、腺泡狀軟組織肉瘤等。
3)受試者至少有1個可測量的病灶(根據RECIST V1.1定義);
4 ECOG評分0或1分;如果已經活動不便、每天需長時間臥床的病友,不能入組;
5 預期生存≥12周。
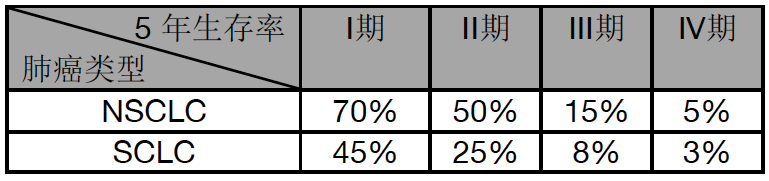
肺癌:非小細胞肺癌
1. 試驗簡介
SH-1028(第三代EGFR-TKI抑製劑)治療經EGFR-TKI治療後進展的T790M突變晚期非小細胞肺癌患者的臨床試驗。
2. 面向患者
經組織學或細胞學確診的非小細胞肺癌(NSCLC)患者;
3. 關鍵入選標準
1) 年齡18-75歲(含邊界值),性別不限;
2) 經組織學或細胞學確診的NSCLC患者;
3) 不適合手術或放療的局部晚期或轉移性NSCLC患者;
4) 既往接受過第一、二代EGFR-TKI(例如吉非替尼、厄洛替尼、埃克替尼或阿法替尼等)持續治療後有疾病進展的影像學依據;除此以外,可接受過其他線治療(化療僅限一線);
5) 須有與EGFR-TKI敏感性相關的EGFR突變(如E19del、L858R、L861Q、G719X等)患者,或根據Jackman標準,臨床曾受益於第一、二代EGFR-TKI治療(PR/CR、或SD持續≥6個月);
6) EGFR-TKI耐葯後經檢測證實有EGFR-T790M突變的患者;
7) 根據RECIST實體腫瘤療效評價標準,患者至少有1個可測量病灶;
鱗狀非小細胞肺癌
1. 試驗簡介
一線含鉑化療失敗的晚期或轉移性肺鱗癌患者中比較IBI308與多西他賽治療有效性和安全性的隨機、開放、III期研究。
2. 面向患者
l 細胞學或組織學確診;
l 含鉑輔助/一線後進展進展、鉑類不耐受;
l 非EGFR突變/非ALK重排;
l 局部晚期/轉移性或複發性鱗狀NSCLC
3. 關鍵入選標準
1)細胞學或組織學診斷為鱗狀非小細胞肺癌;
2)局部晚期、轉移性或複發性(即,不符合根治性放化療標準的IIIB期、IIIC期或IV期)NSCLC(按照UICC/AJCC分期系統第8版),以下三種情況均可:
一線含鉑化療期間或化療後(包括維持化療期間)出現疾病進展(RECIST v1.1),一線治療中允許將其中一種葯停葯、減量或同類藥物之間進行更換;
不能耐受一線含鉑化療方案(接受至少完整一周期治療)的毒性,必須改換其他系統治療方案;
根治切除術後,含鉑輔助化療後6月內疾病複發或進展;
3)至少有一個可測量病灶(RECIST v1.1);
4)男或女性≥18周歲,且≤75周歲;
5)ECOG PS評分為0或1;如果已經活動不便、每天需長時間臥床的病友,不能入組;
6)預期生存期≥12周;
乳腺癌:晚期HER-2陽性乳腺癌
1. 試驗簡介
注射用重組抗HER-2人源化單克隆抗體或安慰劑聯合卡培他濱治療HER-2陽性晚期乳腺癌的隨機、雙盲、多中心Ⅲ期臨床研究
2. 面向患者
經病理學確診的既往接受過紫杉和/或蒽環類治療失敗的、未接受過抗HER-2治療的、HER-2陽性的晚期乳腺癌患者。
3. 關鍵入選標準
1)18~70周歲;
2)經病理診斷為晚期乳腺癌,且至少有一個可測量的靶病灶(根據RECIST V1.1標準):根據實體瘤反應評估標準靶病灶至少有一條徑線可以被精確測量;靶病灶既往未接受過放射、介入等治療;
3)HER-2陽性;
4)既往接受過紫杉類和/或蒽環類治療失敗,複發轉移後治療≤一線;
5)預期生存期大於等於3個月;
6)ECOG評分≤2分;如果已經活動不便、每天需長時間臥床的病友,不能入組。
甲狀腺癌:甲狀腺髓樣癌(MTC)或分化型甲狀腺癌(DTC)
1. 試驗簡介
評價索凡替尼治療晚期甲狀腺髓樣癌和碘難治性分化型甲狀腺癌的療效和安全性的多中心、開放的II期臨床研究
2. 面向患者
經組織學或細胞學確診的甲狀腺髓樣癌(MTC)或分化型甲狀腺癌(DTC)(包括乳頭狀癌、濾泡狀癌、Hurthle細胞癌和其他變異型);
3. 關鍵入選標準
1)對本研究已充分了解並自願簽署知情同意書;
2)年齡≥ 18歲;
3)經組織學或細胞學確診的MTC或 DTC(包括乳頭狀癌、濾泡狀癌、Hurthle細胞癌和其他變異型),或經組織學或細胞學確診的頭頸部腺樣囊性癌(包括涎腺或非涎腺癌)。腫瘤為局部晚期和/或遠處轉移,失去手術指征或不能進行外放射治療;
4)受試者必須有可測量病灶;
5)ECOG 體力評分 0或1 分;如果已經活動不便、每天需長時間臥床的病友,不能入組。
6)DTC必須滿足放射性碘難治,距放射性碘治療結束至少6個月;
7)DTC患者入組前TSH的水準至少應≤ 0.1mU/L以下(或與之相應的其他部門水準);MTC患者入組前TSH應在正常範圍內;
腺樣囊性癌:頭頸部腺樣囊性癌
1. 試驗簡介
評價索凡替尼治療晚期甲狀腺髓樣癌和碘難治性分化型甲狀腺癌的療效和安全性的多中心、開放的II期臨床研究
2. 面向患者
經組織學或細胞學確診的頭頸部腺樣囊性癌(包括涎腺或非涎腺癌)。
3. 關鍵入選標準
1)對本研究已充分了解並自願簽署知情同意書;
2)年齡≥ 18歲;
3)經組織學或細胞學確診的MTC或 DTC(包括乳頭狀癌、濾泡狀癌、Hurthle細胞癌和其他變異型),或經組織學或細胞學確診的頭頸部腺樣囊性癌(包括涎腺或非涎腺癌)。腫瘤為局部晚期和/或遠處轉移,失去手術指征或不能進行外放射治療;
4)受試者必須有可測量病灶;
5)ECOG 體力評分 0或1 分;如果已經活動不便、每天需長時間臥床的病友,不能入組。
6)DTC必須滿足放射性碘難治,距放射性碘治療結束至少6個月;
7)DTC患者入組前TSH的水準至少應≤ 0.1mU/L以下(或與之相應的其他部門水準);MTC患者入組前TSH應在正常範圍內;
腺泡狀軟組織肉瘤
1. 試驗簡介
一項開放、單臂抗PD-1抗體GB226治療複發/轉移性/不可手術切除的腺泡狀軟組織肉瘤(ASPS)患者II期臨床研究。
2. 面向患者
組織學或細胞學確認的複發或轉移或不可手術切除的腺泡狀軟組織肉瘤(ASPS)患者。
3. 關鍵入選標準
1)年齡 18~75 周歲; 性別不限;
2)ECOG 評分 0-1;如果已經活動不便、每天需長時間臥床的病友,不能入組。
3)預期存活期大於 3 個月;
4)組織學或細胞學確認的複發或轉移或不可手術切除的腺泡狀軟組織肉瘤患者;
5)至少有一個可測量病灶,定義為單徑可以準確測量的病灶(RECIST:非淋巴結病灶最長徑,淋巴結病灶短徑);
註:以上為部分主要標準,最終入組標準由項目醫生掌握。
4. 報名方式
微信公眾號:ai幫幫