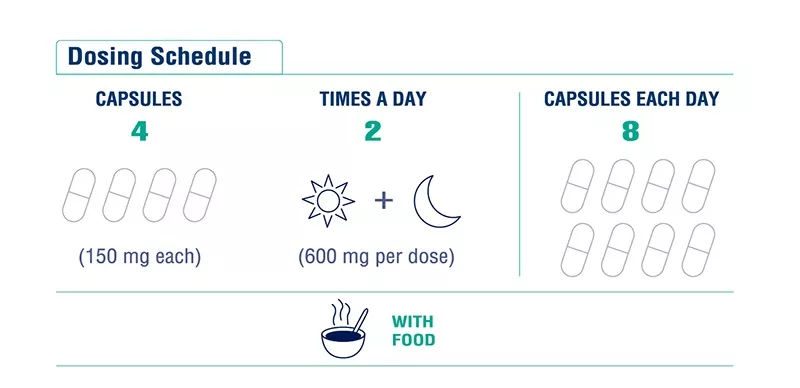
最近新葯獲批不斷,這不,小易才接到吡咯替尼獲批的好消息,就又雙叒叕接到了另一個好消息!
今天,國家藥品監督管理局正式批準了新一代 ALK 抑製劑安聖莎?(化學通用名,阿來替尼)進口註冊申請,用於治療間變性淋巴瘤激酶(Anaplastic Lymphoma Kinase,簡稱 ALK)陽性的局部晚期或轉移性非小細胞肺癌。
作為新一代 ALK 抑製劑,安聖莎將為 ALK 陽性非小細胞肺癌患者帶來全新的治療選擇。
全新一代 ALK 抑製劑
有效延長肺癌患者生存期
肺癌是我國最常見的惡性腫瘤,發病率、死亡率均居惡性腫瘤的首位,是我國的「第一癌症殺手」。
肺癌患者中 80%~85% 屬於非小細胞肺癌,其中 ALK 陽性非小細胞肺癌是一種比較罕見但非常兇險獨特的肺癌亞型,患者平均年齡比較低,大多數患者對化療藥物響應不理想,並伴有複發風險高、腦轉移發生率高、預後差等問題。
根據國際臨床研究 ALEX 結果,與現有標準治療方案相比,安聖莎用於一線治療 ALK 陽性晚期非小細胞肺癌,可以:
將中位無進展生存期(PFS)時間延長到34.8 個月,是現有治療方案近 3 倍。
將患者腦轉移的風險降低 84%,將疾病進展或死亡風險降低一半以上。
正是因為給患者帶來的切實臨床獲益,無論在臨床試驗還是新葯審批過程中,安聖莎都得到了國家藥品監督管理局以及眾多中國肺癌領域臨床專家的大力支持,並基本實現了與歐美同步上市。
新政縮短中外「時差」
創新葯基本實現歐美同步上市
2017年11月:安聖莎在美國獲批一線治療 ALK 陽性非小細胞肺癌。
2017年12月:安聖莎在歐盟獲批一線治療 ALK 陽性非小細胞肺癌。
2018年3月:安聖莎進入中國國家藥品監督管理局藥品審評中心優先審評程式。
2018年8月:安聖莎正式獲批,基本實現了與歐美同步上市。
以往進口抗癌藥在國內獲批上市,一般要比歐美的上市時間延後 5 到 6 年。安聖莎從進入優先審評程式到正式獲批,僅用不到 5 個月的時間。羅氏製藥中國總經理周虹女士表示:
感謝國家藥品監督管理局和中國肺癌領域臨床專家在安聖莎臨床試驗和新葯審批過程中所給予的大力支持,讓中國的肺癌患者與歐美患者基本可以同步獲得最新的治療選擇。
肺癌領域全覆蓋
全面的個體化治療選擇
安聖莎獲批後,羅氏在中國已經有三款治療肺癌的產品:
治療 EGFR 基因突變非小細胞肺癌藥物特羅凱?(化學通用名,鹽酸厄洛替尼)
抗血管生成藥物安維汀?(化學通用名,貝伐珠單抗)
治療 ALK 陽性的局部晚期或轉移性非小細胞肺癌藥物安聖莎? (化學通用名,阿來替尼)
再配合:
羅氏診斷的免疫組化檢測產品
今年登陸中國的新一代基因測序產品
以及即將進入中國的腫瘤免疫治療新葯
羅氏在中國的肺癌治療領域將實現全覆蓋,為廣大患者提供全面的肺癌個體化治療選擇。
本文內容來源:羅氏製藥中國