目前正在開展一項「AK105聯合卡鉑加培美曲塞對比安慰劑聯合卡鉑加培美曲塞一線治療轉移性非鱗非小細胞肺癌的隨機、雙盲、多中心III期臨床研究」。本研究在全國多家研究中心開展,共招募約360例患者。AK105注射液是康方天成(廣東)製藥有限公司研發一種重組抗PD-1人源化單克隆抗體。本研究已獲得國家食品藥品監督管理總局的批準。
主要入選標準
1.簽署書面知情同意書;
2.年齡 ≥ 18歲且≤75歲,男女均可;
3.ECOG體能狀況評分為0 或 1;
4.預期生存期 ≥ 3個月;
5.具有組織學或細胞學證實的不能手術治療且不能接受根治性同步放化療的轉移性(IV期)非鱗、非小細胞肺癌;
6.既往未接受過針對晚期/轉移性NSCLC的全身系統性化療。對於既往對非轉移性疾病以治癒為目的曾接受過輔助化療、新輔助化療或針對進展期疾病接受過根治性放化療的患者,如果疾病進展發生在最後一次治療結束之後>6個月,則有資格參加本研究;
7.必須至少有一個可測量病灶;
8.必須提供診斷為晚期或轉移性腫瘤時或之後的腫瘤組織樣本;
9.必須能提供通過基於組織的檢測證實EGFR和ALK均為野生型的報告;
10.通過如血液學、腎功能、肝功能、凝血功能檢查且確定符合試驗要求;
11.需目前無生育計劃,且在試驗期間能有效避孕;
12.其他的經研究醫生判斷及評估認為不符合本試驗排除標準者;
註:以上為主要參加標準,最終入組標準由項目研究者依照具體項目標準來定。
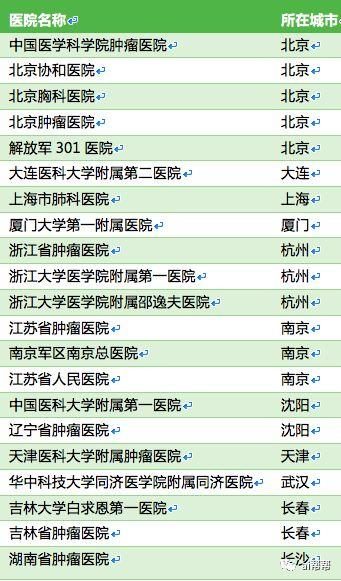
開展醫院
北京大學腫瘤醫院
中國人民解放軍總醫院
首都醫科大學附屬北京胸科醫院
哈爾濱醫科大學附屬腫瘤醫院
常州市腫瘤醫院
上海市胸科醫院
浙江大學醫學院附屬第一醫院