編者按:
2019年8月29-31日,第十屆亞太原發性肝癌專家會議(Asia-Pacific Primary Liver Cancer Expert,簡稱APPLE)在日本劄幌隆重舉行。大會重點聚焦了近年來肝癌藥物治療進展和最新研究成果。會上,有關肝癌免疫聯合治療的臨床研究首當其衝成為與會專家、學者們關注的熱點話題。本刊特邀北京協和醫院肝臟外科趙海濤教授在大會現場與我們分享免疫聯合治療領域最新、最熱的臨床研究成果,帶我們揭秘肝癌免疫聯合治療背後的作用機制。
?敬請觀看趙海濤教授訪談
《國際肝病》:您認為肝癌治療領域,近年來哪種治療手段進展最快、療效最為顯著?趙海濤教授:20多年來,肝癌的基礎和臨床研究均取得了巨大的突破,肝癌患者的治療有效率亦有了顯著提升。自2018年以來,靶向治療、免疫治療在肝癌的治療中取得了顯著進展。
從2007年索拉非尼作為唯一的肝細胞癌(HCC)治療一線藥物開始,肝癌靶向治療藥物崛起。到目前為止,多種治療方法被證明有效並逐漸得到應用。多種新葯已獲得FDA的批準,包括小分子靶向治療藥物,如二線藥物瑞戈非尼(regorafenib)和卡博替尼(cabozantinib),以及一線藥物侖伐替尼(lenvatinib);美國FDA也批準了免疫檢查點抑製劑納武利尤單抗(Nivolumab)和帕博利珠單抗(Pembrolizumab)作為HCC治療的二線藥物。此外雷莫蘆單抗(ramucirumab)用於高AFP水準的HCC患者也被證實是有效的。
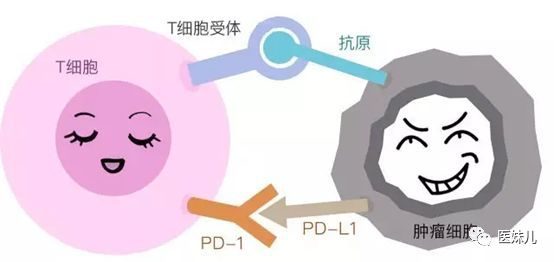
另外,免疫治療已成為目前腫瘤治療的主要方法之一。其作用機制是通過激活自身免疫細胞來對腫瘤細胞進行靶向殺傷。免疫檢查點抑製劑是目前最主流的免疫治療藥物,其治療的靶點較多,其中有關PD-1、PD-L1及CTLA-4的免疫檢查點抑製劑在腫瘤治療中應用較為廣泛。在肝癌治療方面,上述免疫檢查點抑製代表性藥物納武利尤單抗、帕博利珠單抗均已獲得FDA的批準治療晚期肝癌。
以上這些藥物在肝癌的一線或二線治療中獲得了顯著進展,然而更加值得我們期待的是靶向藥物與免疫治療藥物的聯合治療。在前期小樣本量的臨床數據中,我們可以看到靶向藥物與免疫藥物的聯合治療,可使得HCC患者的ORR率達到40%,DCR達到90%。因此,這也是未來肝癌治療非常值得期待的研究方向。
《國際肝病》:我們關注到,有關納武利尤單抗單葯一線治療和帕博利珠單抗單葯二線治療的兩項III期臨床試驗相繼失敗,都未能體現免疫治療對比現有療法的優勢。您認為癥結在哪,提高療效的策略是什麼?趙海濤教授:早期的臨床研究表明,關於納武利尤單抗、帕博利珠單抗在晚期HCC患者中的ORR均在17%左右。兩葯的III期臨床試驗相繼失敗可能與試驗設計有一定的關係,但最終的問題可能還是出在單葯的免疫治療在HCC中的有效率偏低,ORR一般為17%~21%。因此,在臨床實踐中我們更傾向於免疫治療藥物與其他治療手段的聯合,常常會獲得「1+1>2」的效果。
《國際肝病》:在本屆APPLE大會上,有學者報告了新型免疫治療藥物PD-L1抑製劑Atezolizumab+抗血管生成藥聯合治療的Ib期臨床研究的最終結果,讓我們又充滿了驚喜和期待。請您為我們點評一下此項研究的結果和意義?趙海濤教授:這是一項基於國際、多中心的1b臨床研究,觀察了Atezolizumab+貝伐珠單抗(以下簡稱「T+A」)聯合治療不可切除肝癌、晚期肝癌患者的安全性和有效性。早在2018年的ASCO、ESMO大會,有較早的小樣本數據公布,當時的有效率達到60%以上,這讓我們這些肝癌領域的研究者非常期待。
這次APPLE大會上公布的最終數據,將樣本量擴大到了104人,中位隨訪時間達到了12.4個月。結果顯示,主要研究終點:中央評估機構(IRF)基於RECIST 1.1評估的ORR為36%。關鍵次要研究終點:IRF基於HCC mRECIST評估的ORR達到了39%,OS達到了17.1個月(隨訪中,數據尚不成熟),PFS均為7.3個月,DOR雖尚未達到,但截至2019年6月14日,IRF基於RECIST 1.1和HCC mRECIST評估的疾病控制率(DCR)均達到了71%,分別有76%和68%的患者處於持續緩解中。這個數據在肝癌治療領域是非常優異的。
本人所在部門有幸參與了該聯合免疫治療方案的全球註冊III期研究,值得一提的是,該項研究的入組標準包含了具有血管侵犯和/或肝外播散(EHS)的患者,其比例達到88%,可以說患者腫瘤的惡性程度非常高,在這種情況下,「T+A」方案依然能夠取得這樣的有效率值得驚嘆,也非常讓我們充滿期待。
《國際肝病》:請您從抗腫瘤治療的機制上,解釋一下為何「T+A」的聯合能夠發揮出出人意料的作用?
趙海濤教授:近年來,採用免疫檢查點抑製劑聯合抗血管生成藥在多種腫瘤的治療中取得了一定的效果。目前,對於聯合治療的機制尚未明確。眾所周知,腫瘤的新生血管普遍存在異常,異常的新生血管不僅會直接影響免疫細胞對腫瘤部位的浸潤能力,還會導致腫瘤微環境呈現乏氧和酸性狀態,營造出對免疫細胞不利的「大環境」。抗血管生成藥物不僅可以改善腫瘤血管的生成,讓血管正常化的同時改善免疫微環境,還可以促進腫瘤中T細胞的浸潤,從而進一步加強免疫檢查點抑製劑的療效。我們知道,PD-L1抑製劑的作用是解除腫瘤細胞對於T淋巴細胞作用的抑製,然而只有在T淋巴細胞能夠充分進入到腫瘤微環境中,PD-L1抑製劑的作用才能得到充分發揮。因此,PD-1/L1抑製劑聯合抗血管生成藥的使用,從理論上有著「1+1>2」的增效基礎。這也正是二者聯合在多種實體腫瘤的治療中獲得節節勝利的主要原因。
《國際肝病》:隨著此項研究的結果公布,「T+A」的聯合將有望作為不可切除性肝癌、晚期肝癌的一線治療方案。相比較其他免疫治療的聯合,「T+A」方案具有哪些優勢?趙海濤教授:首先,由於Ib期研究入組的患者相比較其他藥物的研究,腫瘤惡性程度更高,因此,「T+A」方案可能在晚期肝癌患者中具有更高的療效。其次,目前關於免疫檢查點抑製劑(CICs)的給葯,主要都是通過靜脈注射,「T+A」治療完全通過靜脈輸注進行,每3周進行一次給葯。而其他的免疫+小分子TKI抗血管生成聯合方案,都是靜脈輸注+每日口服給葯的模式,「T+A」方案操作更加簡便。

專家簡介
趙海濤,北京協和醫院肝臟外科
教授,主任醫師,博士生導師
2017年國家萬人計劃專家(領軍人才)
2016年國家青年科技創新領軍人才
2011年教育部新世紀優秀人才
919腫瘤精準免疫治療公益基金創始人
北京大學校友會理事
歐美同學會醫師協會副秘書長,青委會主委,肝膽分會秘書長,副主委科技部重大項目評審專家HBSN(SCI收錄3.45)雜誌副主編,WJG(IF:3.3)雜誌編委以通訊作者發表SCI論文超過60篇,總影響因子超過300分
●
●
在看點這裡