來源丨醫學界腫瘤頻道
2018年,中國內地正式進入免疫腫瘤治療時代。
6月15日,納武利尤單抗注射液(nivolumab,商品名「歐狄沃?」)獲批上市,成為中國大陸地區首個且唯一獲批用於肺癌治療的PD-1抑製劑,開啟了我國腫瘤治療的新篇章。如今,靶向治療方興未艾,而免疫治療已從夢想照進現實。
在新時代的交叉路口,有人樂觀欣喜,有人冷靜保守。探路者們都在思考:未來的腫瘤治療,將會是怎樣一番圖景?免疫治療又將扮演何種角色,是核心,是主流,還是輔助?顯然,我們需要聽到更多智者的聲音。
9月19日~23日,2018年中國臨床腫瘤學會年會(CSCO)在廈門召開,「腫瘤免疫治療」成為了當之無愧的熱門詞。醫學界腫瘤頻道有幸採訪到「EGFR之父」、現任百時美施貴寶(BMS)首席科學官、美國馬薩諸塞州總醫院(MGH)前董事長兼首席執行官、耶魯醫學院教授Tom Lynch博士,講述他心目中腫瘤治療的過去、現在和未來。

圖:BMS首席科學官,Tom Lynch 博士
一
過去:EGFR 14年傳奇再續,免疫治療曲折探索
Tom Lynch博士之所以被稱為「EGFR之父」,起因於2004年他與其他MGH研究者在《新英格蘭醫學雜誌》上發表的「劃時代」發現:在非小細胞肺癌(NSCLC)患者中,酪氨酸酶抑製劑(TKI)吉非替尼的療效與表皮生長因子受體(EGFR)突變密切相關。
從此,肺癌治療進入了EGFR-TKI為代表的靶向治療時代。與此同時,變化正在不知不覺中發生著:越來越多的肺癌基因突變靶點被發現,目前已超過10種類型;基因測序技術飛速發展,準確、耗時少、費用低的技術正在迅速可及;EGFR-TKI已研發至第三代,出現了針對獲得性耐葯的有效藥物。
相比於靶向治療,免疫治療的路線似乎更加艱難曲折。
人們對免疫治療的探索,最早起源於300多年「人痘接種」的成功試驗。半個多世紀前,諾貝爾生理學或醫學獎得主Frank Burnet教授提出了癌症免疫監視的理論。但是,要能在極其紛繁複雜的免疫系統裡面找出可以對抗腫瘤的有效靶標談何容易。
在漫長的等待和研發過後,時間來到了2011年。這一年,全球第一個獲批的免疫腫瘤治療藥物——抗CTLA-4抑製劑ipilimumab獲美國FDA批準用於晚期轉移性黑色素瘤的治療。隨後,以PD-1/PD-L1為代表的免疫檢查點抑製劑藥物相繼湧現。
2013年,免疫腫瘤治療被《紐約時報》和《科學》雜誌評為現代醫學的「重大突破」。2016年和2017年,免疫治療連續兩年問鼎美國臨床腫瘤學會(ASCO)臨床腫瘤年度進展。人們驚呼:免疫腫瘤治療的「春天」真的來了!
二
現在:免疫治療登陸中國,奠定腫瘤治療裡程碑
談起「O葯」 納武利尤單抗,Tom Lynch博士也不得不讚歎道,這是一個令全球腫瘤醫生和患者「無比振奮」的藥物。

圖:Tom Lynch博士接受媒體採訪
在免疫治療領域,納武利尤單抗有多個「第一」的頭銜:它是第一個在全球範圍內獲批上市的PD-1抑製劑,第一個在全球獲批用於免疫腫瘤聯合治療的藥物,第一個在我國獲批進行腫瘤免疫治療臨床試驗的PD-1抑製劑,第一個在中國提交上市申請並第一個獲批的PD-1抑製劑,也是第一個和唯一一個證明能夠為晚期肺癌患者帶來顯著生存獲益的PD-1抑製劑。
截至目前,納武利尤單抗已在全球近70個國家及地區批準上市,獲得了17項適應證,覆蓋9大癌種,包括肺癌(非小細胞肺癌和小細胞肺癌)、肝癌、結直腸癌、腎癌、頭頸部鱗狀細胞癌、霍奇金淋巴瘤、黑色素瘤、膀胱癌、胃癌。
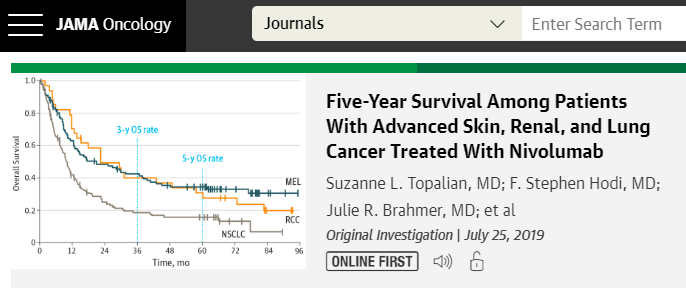
目前,納武利尤單抗的全球使用患者已超27萬。全球研究數據顯示,納武利尤單抗是目前在NSCLC免疫治療研究中隨訪時間最長的PD-1抑製劑,晚期患者五年生存率由過去的不到5%提高到了16%。也就是說,平均6個使用該葯的晚期NSCLC患者中,有1個有望生存期超過5年,達到長期疾病緩解。
在我國大陸地區啟動的首個PD-1抑製劑關鍵III期臨床試驗CheckMate 078顯示,最短隨訪8.8個月時,納武利尤單抗組的中位生存期(OS)為12.0個月,化療組為9.6個月,且死亡風險降低32%。該結果與之前的國際大型臨床研究一致。
此外值得注意的是,在該試驗的亞組分析中,納武利尤單抗在鱗癌和非鱗癌患者中均觀察到生存獲益(死亡風險分別降低39%和24%),不同PD-L1表達水準的患者均能獲益(PD-L1表達≥1% 和<1%,死亡風險分別降低38%和25%)。
納武利尤單抗憑藉其超越標準化療的穩定療效及長期生存數據,目前已經成為CSCO原發性肺癌診療指南唯一推薦用於肺癌治療的PD-1抑製劑,是EGFR/ALK陰性非小細胞肺癌的二線標準治療。
據悉,納武利尤單抗在今年6月的獲批,距BMS在2017年11月為其遞交上市申請,僅過了半年多的時間。這其中除了得益於卓越的循證醫學研究數據,也得益於我國在創新藥物審批方面的激勵性新政。2017年12月,《關於鼓勵藥品創新實行優先審評審批的意見》出爐,在惡性腫瘤等疾病領域能取得明顯臨床優勢的創新藥品有望獲得優先審評審批,這無疑加速了創新藥物來到患者身邊的速度。
三
未來:創新研發永不止步,聯合治療大勢所趨
現如今,作為全球領先的生物製藥公司,腫瘤免疫治療領域的長官者,BMS在研發領域的步伐從未停歇。「 我們的使命非常清晰,那就是發現、開發並提供創新藥物,幫助患者戰勝嚴重疾病。」Tom Lynch博士表示,「創新是做研發最核心的基礎,百時美施貴寶擁有一支以科學為驅動、充滿熱情的研發團隊,我們遵循科學,以患者需求以及科學發現為驅動力,致力於研發真正能夠改善患者現狀的革命性藥物,在需求尚未被滿足的醫療領域建立全新標準。」
目前百時美施貴寶在全球研發的重點包括腫瘤、免疫科學、心血管疾病、纖維化等未被滿足的迫切的重大疾病需求。「百時美施貴寶的在研產品線非常豐富,同時我們也在探尋不同的靶點對於癌症及其他疾病的治療作用。相信包括NLRP-3、新型CTLA-4、STING, NKTR-214等在內的極具前景的分子及創新藥物將有機會改變某些疾病的治療方式。」
談到中國,Tom Lynch博士無比自豪的介紹道,目前在中國已經和正在進行的免疫腫瘤臨床研究達26項之多,其中大部分為III期臨床研究,覆蓋肺癌、肝癌、胃癌等諸多中國高發的瘤種。這使得是百時美施貴寶成為免疫腫瘤治療在中國投入最大的公司。接下來,BMS要做的事情是和中國的監管機構密切溝通及合作,討論哪些適應證可以更快的推向中國市場,讓患者儘快獲益。

圖:Tom Lynch博士採訪現場
對於免疫治療未來的發展,Tom Lynch博士表示,聯合治療將會受到越來越多的關注,同時研究者也需要不斷深化對疾病生物學的理解,通過生物標誌物來幫助預測患者的治療效果。
目前,百時美施貴寶正在積極探尋多種免疫治療組合,包括免疫聯合免疫、免疫聯合靶向、免疫聯合化療、免疫聯合放療等。
「我認為,聯合治療無疑是未來肺癌治療的趨勢之一。」Tom Lynch博士肯定了聯合治療的價值,也指出了研發過程中需要警惕的3個方面的問題:「第一個問題是劑量,我們需要確保療效好且安全的劑量,這個劑量可能和單葯治療不盡相同。第二個問題是二者是否會產生拮抗,造成適得其反的效果。最後是藥物的副作用,患者是否可以耐受聯合治療帶來的藥物毒性。」
談到生物標誌物,Tom Lynch博士表示,包括TMB、LAG-3等潛在生物標誌物已展現出了良好的應用前景,有望在未來能夠更準確預測免疫腫瘤治療的應答效果。
創新研發是抗擊癌症的必經之路。除免疫檢查點抑製劑外,BMS正在研發許多其他潛在有效的靶點。除此之外,我國也有不少本土葯企進行腫瘤免疫治療創新藥物的研發。「中國是人口大國,創新能力不可小覷,同時,中國在健康及醫療領域已經取得了很多進展。我非常看好中國的藥物研發實力。」Tom Lynch博士如此評價。說不定在不久的將來,這些在研藥物將會把免疫治療帶入「2.0」時代。
總結作為全球及我國發病率第一的腫瘤,肺癌的治療進展總是非常吸引關注。縱觀肺癌治療史,從最初的化療、放療,到如今靶向、免疫治療,肺癌的長期生存已經從曾經的夢想變成了可以企及的現實。我們相信,隨著免疫腫瘤的「大幕」在我國開啟,包括肺癌在內的更多腫瘤患者將從中獲益,獲得更長的生存期和更好的生活品質!
專家簡介

BMS首席科學官,Tom Lynch博士
Tom Lynch博士於2017年3月加入百時美施貴寶擔任首席科學官,長官研發部門。他曾在2013-2017年期間擔任百時美施貴寶的董事。他擁有30多年在醫療、管理和長官方面的豐富經驗,並且在美國馬薩諸塞州總醫院(MGH)任職超過23年。他從2015年到2017年擔任MGH普通內科醫師組織主席和首席執行官,並擔任MGH的董事會成員。
在擔任MGH董事長兼首席執行官之前,他曾擔任耶魯癌症中心主任,並於2009年至2015年擔任耶魯醫學院理查德和喬納森·薩克勒內科教授。2009至2015年間,他還擔任位於耶魯紐黑文的斯邁洛癌症醫院(Smilow Cancer Hospital)的主治醫師。2009年之前,他曾任哈佛醫學院醫學教授和麻省總醫院血液學/腫瘤學主任。2004年,在他任職於MGH之時,他與團隊發布了醫學界一個極為重要的發現:有些藥物僅在某些具有基因突變的肺癌患者中有效。
Tom Lynch博士是美國癌症研究協會(AACR)、美國臨床腫瘤學會(ASCO)以及國際肺癌研究協會(IASLC)的成員。