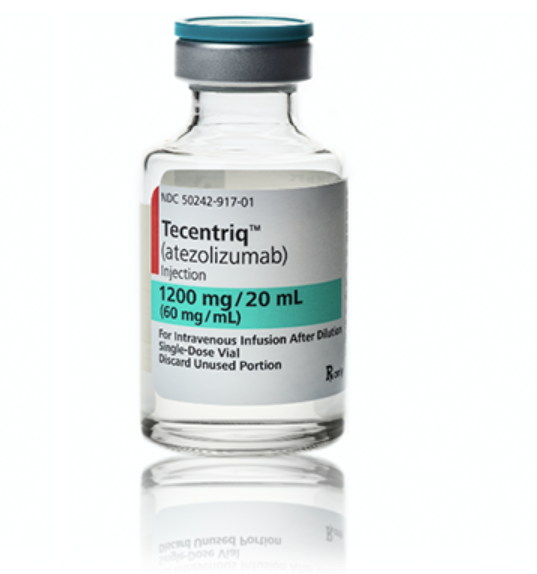
繼剛剛獲批三陰性乳腺癌沒多久,Tecentriq適應症再擴大!
3月19日,羅氏宣布,FDA已批準Tecentriq聯合化療,用於成人廣泛期小細胞肺癌(ES-SCLC)的初始(一線)治療。
據悉,這是20多年來首個被FDA批準用於ES-SCLC患者初始治療的新方案,是首個也是目前唯一一個被批準用於ES-SCLC初始治療的癌症免疫療法。
「Tecentriq是首個被批準用於ES-SCLC初始治療的癌症免疫療法,ES-SCLC是一種極為難治的惡性腫瘤。」羅氏首席醫學官兼全球產品開發負責人桑德拉·霍寧博士說,「截至目前,這種疾病的治療進展有限,我們很高興能為患者帶來一種新的治療標準。與化療相比,這種治療已被證明能夠改善患者的生存期。」


這一批準是基於一項名為IMpower133的III期研究,該研究是一項多中心、雙盲、隨機、安慰劑對照的研究,旨在評估Tecentriq聯合化療與單純化療相比,在ES-SCLC初次化療患者中的有效性和安全性。
研究結果顯示,在意向性治療人群中,Tecentriq聯合化療與單純化療相比,可以顯著延長生存期。
此外,Tecentriq聯合化療與單純化療相比,還顯著降低了疾病惡化或死亡風險。
另外,Tecentriq聯合化療方案的安全性與Tecentriq已知的安全性特徵一致。
該研究結果已發表在《新英格蘭醫學雜誌》上。
Tecentriq是一種靶向結合PD-L1的單克隆抗體,通過抑製PD-L1可以重新活化T細胞。
此前,Tecentriq已有多種適應症在美獲批,包括用於治療尿路上皮癌、非小細胞肺癌、以及三陰性乳腺癌等。
據了解,羅氏已在我國就Tencentriq開展了多項臨床研究,治療領域涵蓋非小細胞肺癌、肌層浸潤性尿路上皮癌、三陰性乳腺癌、肝細胞癌等。
肺癌是全球發病率和死亡率最高的惡性腫瘤。據估計,2018年肺癌將造成180萬人死亡,佔預計癌症死亡總人數的18.4%。
在我國,肺癌發病率、死亡率同樣高居首位。每年新發病例約78.1萬,死亡病例約62.6萬。
依據病理學,肺癌通常分為非小細胞肺癌和小細胞肺癌。其中,非小細胞肺癌約佔所有肺癌病例類型的85%,小細胞肺癌約佔所有肺癌類型的15%。
與非小細胞肺癌相比,小細胞肺癌的腫瘤細胞生長、分裂和擴散速度更快。其中,約70%被診斷為ES-SCLC,具有高度侵襲性,廣泛擴散到肺部、淋巴結或身體其他部位,在過去20年裡治療進展有限。
此次,Tecentriq聯合化療獲批用於治療ES-SCLC,對ES-SCLC患者來說無疑是一個好消息。
這一療法何時能在我國獲批,值得業界密切關注!