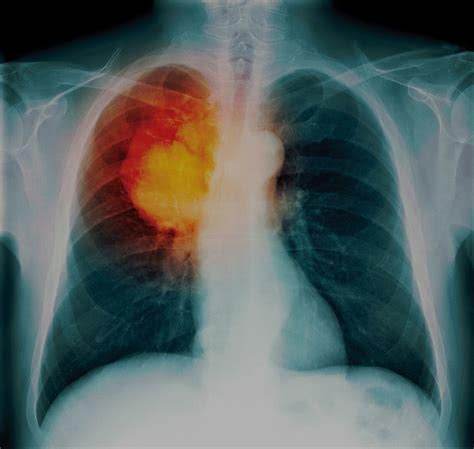
7月24日,百濟神州公司宣布,其在研的腫瘤免疫治療藥物PD-1抗體tislelizumab聯合化療作為潛在一線療法,治療中國IIIb期或IV期非鱗狀非小細胞肺癌(NSCLC)患者的臨床3期試驗實現首例患者給葯。
Tislelizumab (BGB-A317)是百濟神州開發的一種在研人源性單克隆抗體,它屬於一類被稱為免疫檢查點抑製劑的腫瘤免疫藥物。2017年7月,百濟神州與新基公司達成全球戰略合作關係,在亞洲(除日本)以外開發tislelizumab治療實體瘤。
據百濟神州腫瘤免疫學首席醫學官 Amy Peterson醫學博士評介紹,該3期臨床主要用以評估在目前針對晚期非鱗狀NSCLC患者的全球標準治療方案「鉑加培美曲塞化療」中加入在研免疫腫瘤藥物tislelizumab的潛在影響。
據介紹,這項3期、開放、多中心臨床試驗預計在中國大陸招募約320位IIIb期或IV期未經化療治療的非鱗狀NSCLC患者。該試驗旨在對比由獨立評審委員會(IRC)評估的根據RECIST v1.1定義的無進展生存期(PFS)。關鍵次要終點包括總生存期、總體緩解率、研究者評估的PFS、安全性和耐受性。
除了本次啟動的在中國肺癌患者中的3期臨床外,百濟神州也在開展tislelizumab用於治療肝細胞癌、食管鱗狀細胞癌的全球3期臨床,針對先晚期肝細胞癌患者及淋巴瘤患者的兩項全球2期臨床,以及治療複發/難治性經典霍奇金淋巴瘤和尿路上皮癌的兩項中國關鍵性2期臨床。
關注【葯務音訊】,讓新葯好葯不再杳無音訊~