責編丨迦漵

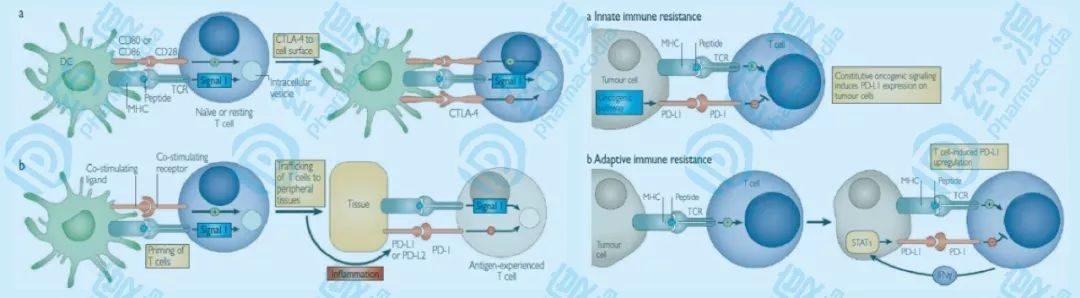
腫瘤免疫是機體對腫瘤細胞產生的特異性免疫反應。免疫系統通過識別腫瘤特異性抗原並遞呈給T細胞,從而特異地清除這些「非正常」細胞,抵禦腫瘤的發生髮展。大量的臨床數據表明,腫瘤免疫治療能夠在患者中產生持久抗腫瘤免疫記憶。這種現象表明腫瘤免疫治療較其他腫瘤治療有鮮明的特點:即便治療停止,仍然能在病人中產生長期的保護作用。
近年來,腫瘤免疫治療取得了重大的突破,2011年針對淋巴細胞CTLA4的伊匹木單抗(Ipilimumab)成為近30年來第一個被證明能延長晚期黑色素瘤生存的藥物;2012年起不斷有報導證實,針對PD-1/PD-L1通路的單抗在治療黑色素瘤、肺癌、膀胱癌等惡性腫瘤中取得了明顯療效;而以CAR-T細胞過繼治療為代表的越來越多的的免疫治療方法獲得了FDA突破性療法資格。這表明腫瘤免疫治療與其他傳統的腫瘤治療手段相比,具有鮮明的特點和優勢。腫瘤免疫治療於2013、2017兩次被Science雜誌評為年度十大科學突破;2016,2018兩次被美國臨床腫瘤協會(ASCO)評為最具影響力的年度進展,我國也將發展腫瘤免疫治療技術已正式寫入「十三五」國家科技創新規劃,顯示免疫治療已經成為目前國際免疫和腫瘤研究領域的前沿熱點,具有巨大的社會和經濟價值。
目前,免疫治療的效果受限於腫瘤免疫逃逸。腫瘤免疫逃逸是指腫瘤細胞通過自身或微環境的改變逃避免疫系統識別和攻擊。例如,中山大學孫逸仙紀念醫院宋爾衛、蘇士成團隊前期研究發現,高轉移的乳腺癌細胞分泌GM-CSF使單核細胞分化為腫瘤相關巨噬細胞並分泌CCL18,CCL18不但促進腫瘤轉移(Su et al., Cancer Cell, 2014)、纖維化(Su et al., Nature Communications, 2015;Su et al., Cell,2018)、還可募集外周血的幼稚T細胞至腫瘤局部,轉變Treg細胞抑製腫瘤特異性免疫(Su et al., Cell Research, 2017)。腫瘤微環境的複雜網路顯著地削弱了免疫治療的功效,使免疫治療在實體瘤中的開展仍有很大困難。
9月17日,中山大學孫逸仙紀念醫院宋爾衛、蘇士成團隊在Nature Immunology雜誌在線發表了題為NKILA LncRNA promotes tumor immune evasion by sensitizing T cells to activation-induced cell death的研究論文,首次發現lncRNA通過調控T細胞亞群的凋亡敏感性,從而改變腫瘤微環境中免疫激活及免疫抑製的T細胞亞群的平衡,造成腫瘤的免疫逃逸,揭示了不同亞群T細胞凋亡敏感性不同的調控機制。

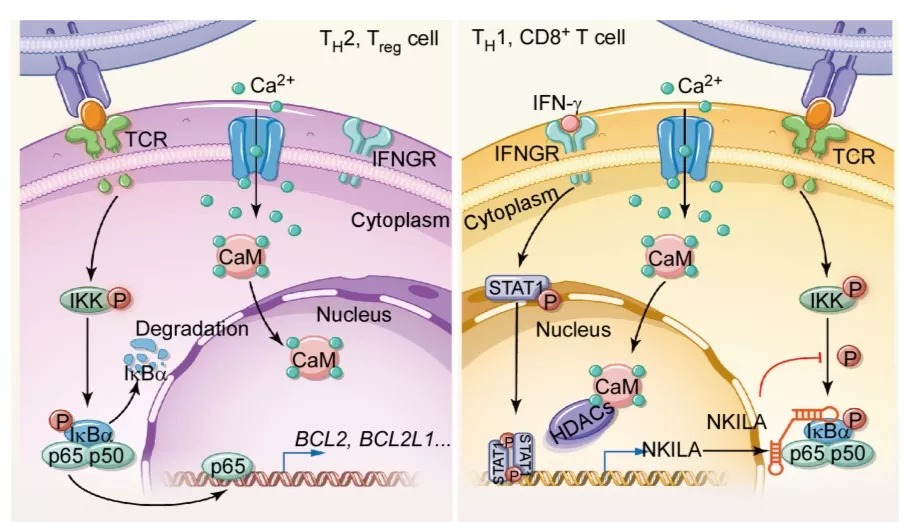
長非編碼RNA NKILA調控不同亞群T細胞凋亡敏感性的機制
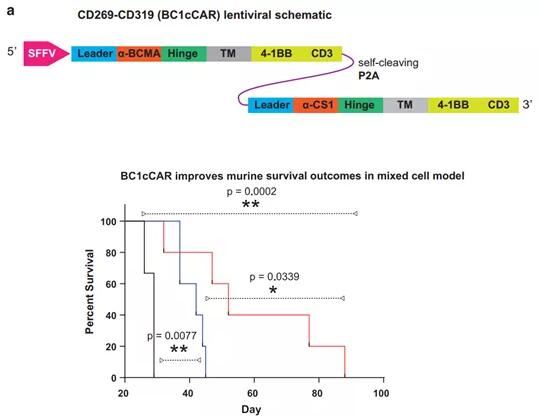
為了最大程度的模擬病人的腫瘤微環境以及避免同種異體反應,該研究選用了人源腫瘤異種移植(Patient-derived xenograft, PDX)模型,模擬人的過繼性免疫治療的過程,將修飾後的同源T細胞及樹突狀細胞回輸至荷瘤小鼠體內(下圖)。發現沉默NKILA的T細胞在荷瘤小鼠中的凋亡明顯減少,可更多地浸潤到腫瘤局部行使殺傷功能,使腫瘤明顯縮小。目前TCR-T或者CAR-T細胞治療的主要策略是促進T細胞對腫瘤的識別和殺傷,但在實體瘤中療效不佳,除了不能夠有效地浸潤到腫瘤組織內部等原因外,該研究提示,一個重要的原因可能就是這類細胞在接觸腫瘤之前,就已經死於微環境中FasL等凋亡信號的調控。

過繼性回輸沉默NKILA的T細胞在臨床前PDX模型中顯示療效
該研究首次發現lncRNA通過調控T細胞亞群的凋亡敏感性,從而改變腫瘤微環境中免疫激活及免疫抑製的T細胞亞群的平衡,造成腫瘤的免疫逃逸,揭示了不同亞群T細胞凋亡敏感性不同的調控機制。同時提出,通過靶向lncRNA NKILA,能夠保護T細胞順利識別腫瘤細胞,從而為過繼細胞免疫治療提供了新的思路。

論文通訊作者宋爾衛教授(左)和蘇士成副教授(右)
據悉,黃迪博士為本文第一作者,宋爾衛教授、蘇士成副教授是共同通訊作者。
附宋爾衛/蘇士成團隊近年來的代表論文:
Su, S., Chen, J., Yao, H., Liu, J., Yu, S., Lao, L., ... & Song, E. (2018). CD10+ GPR77+ cancer-associated fibroblasts promote cancer formation and chemoresistance by sustaining cancer stemness. Cell, 172(4), 841-856.
Su, S., Liao, J., Liu, J., Huang, D., He, C., Chen, F., ... & Song, E. (2017). Blocking the recruitment of naive CD4+ T cells reverses immunosuppression in breast cancer. Cell research, 27(4), 461.
Su, S., Zhao, Q., He, C., Huang, D., Liu, J., Chen, F., ... & Song, E. (2015). miR-142-5p and miR-130a-3p are regulated by IL-4 and IL-13 and control profibrogenic macrophage program. Nature communications, 6, 8523.
Su, S., Liu, Q., Chen, J., Chen, J., Chen, F., He, C., ... & Song, E. (2014). A positive feedback loop between mesenchymal-like cancer cells and macrophages is essential to breast cancer metastasis. Cancer cell, 25(5), 605-620.
論文鏈接(點擊文末「閱讀原文」)
BioArt,一心關注生命科學,只為分享更多有種、有趣、有料的資訊。關注投稿、合作、轉載授權事宜請聯繫微信ID:fullbellies 或郵箱:[email protected]