摘要
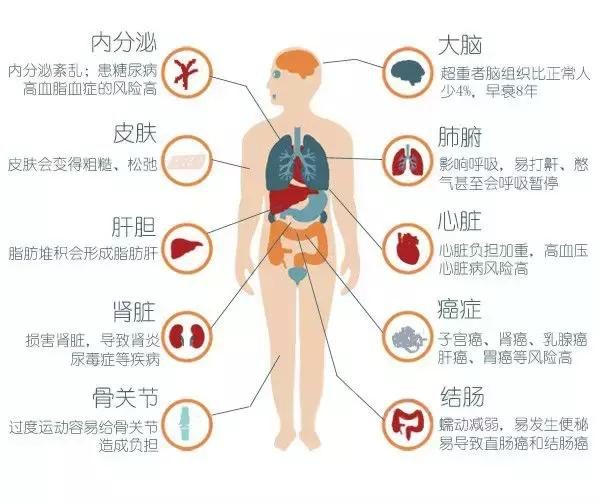
通過使用小鼠和採集的人體臨床標本,研究人員發現,caspase-2(一種蛋白質裂解酶),它是非酒精性脂肪性肝炎(non-alcoholic steatohepatitis,NASH)的一個關鍵驅動因素。而NASH是一種慢性和侵襲性的肝臟疾病。通過確定caspase-2的關鍵作用,他們認為這種酶的抑製劑可能會創造一種有效的方法來阻止NASH的病情發展——甚至可能可以逆轉早期癥狀。

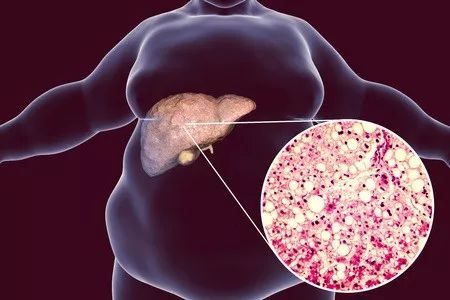
(這是肝臟切片,切片顯示了患了像人類NASH的小鼠體內的肝臟纖維化)
1

通過使用小鼠和採集的人體臨床標本,研究人員發現,caspase-2(一種蛋白質裂解酶),它是非酒精性脂肪性肝炎(non-alcoholic steatohepatitis,NASH)的一個關鍵驅動因素。而NASH是一種慢性和侵襲性的肝臟疾病。通過確定caspase-2的關鍵作用,他們認為這種酶的抑製劑可能會創造一種有效的方法來阻止NASH的病情發展——甚至可能可以逆轉早期癥狀。
該研究結果發表在9月13日的《細胞》(Cell)的在線期刊上。
2

研究結果顯示,caspase-2是NASH發病機制的關鍵介質,不僅在小鼠中是這樣,而且在人類中也是如此。當解釋NASH如何開始時,該研究結果也可能為治療或預防這種可怕的疾病提供了一種簡單而有效的方法。
NASH是最具侵襲性的非酒精性脂肪性肝病(non-alcoholic fatty liver disease,NAFLD),包括一系列慢性肝病,並已成為肝臟移植的主要原因。但是,NAFLD和NASH的原因仍然是一個謎。
研究人員認為,促使良性NAFLD發展為侵襲性NASH的一個因素是肝內蛋白質錯誤摺疊引起的內質網(endoplasmic reticulum,ER)應激水準升高,這就會導致肝臟組織中膽固醇和甘油三酯的過度累積。
在小鼠中應用這一觀點時,研究人員首先通過同時運用肝臟特有的ER應激和高脂肪飲食來引發NASH樣疾病,來複製人類NASH的主要特徵(包括肝臟細胞中脂肪堆積,肝臟損傷,炎症和疤痕),從而確定參與NASH發病機制的分子。 研究人員利用該模型發現,NASH的發病與caspase-2的表達增加有關。
之後一個階段中,研究團隊檢視了從良性NAFLD或侵襲性NASH患者收集的人體肝臟標本,以確認人類身體中caspase-2的表達也會升高。通過敲除採用肝臟ER應激和高脂肪飲食小鼠中的caspase-2基因或用特異性caspase-2抑製劑治療小鼠,他們發現caspase-2負責NASH發生過程的各個方面,包括脂滴積聚,肝臟損傷,炎症和疤痕。
通過阻止caspase-2表達或抑製其活性,NASH的生物標誌物會得到緩解。這一研究結果令人非常興奮,因為現在,不僅對caspase-2在疾病中的作用有了了解,而且還發現了一條研發潛在治療藥物的新途徑。
通過這項研究,該研究團隊還發現,caspase-2在激活SREBP1和2中具有關鍵作用,SREBP1和2是脂肪生成過程中的主要調節因子。脂肪生成是一種發生在肝臟中的過程,其中像碳水化合物之類的營養成分會轉化為脂肪酸,甘油三酯和膽固醇。發現Caspase-2通過切割另一種被稱為site-1蛋白酶的蛋白質來控制SREBP1和2的活化。
在未患有NASH的個體中,SREBP1和SREBP2的活性會受到控制,這對於防止肝臟中產生過多的脂質積聚至關重要。然而,在NASH患者中,就出了一點問題,肝臟會持續產生過量的甘油三酯和膽固醇。這與升高的SREBP1和SREBP2活性以及增加的caspase-2表達相關。
展望未來,該研究團隊希望開發更有效的藥物如caspase-2抑製劑用於預防NASH,並最終使該藥物成為治療該疾病的一種選擇。
這項研究向前邁出了一大步,能夠了解相關疾病原因,並為NASH和NAFLD患者探索可能的新療法。該研究團隊也希望進一步擴大試驗規模來驗證這些研究結果和實現研究成果的轉化。
原始論文:
Ju Youn Kim, Ricard Garcia-Carbonell,Shinichiro Yamachika, Peng Zhao, Debanjan Dhar, Rohit Loomba, Randal J.Kaufman, Alan R. Saltiel, Michael Karin. ER Stress Drives Lipogenesis andSteatohepatitis via Caspase-2 Activation of S1P. Cell, 2018; DOI: 10.1016/j.cell.2018.08.020