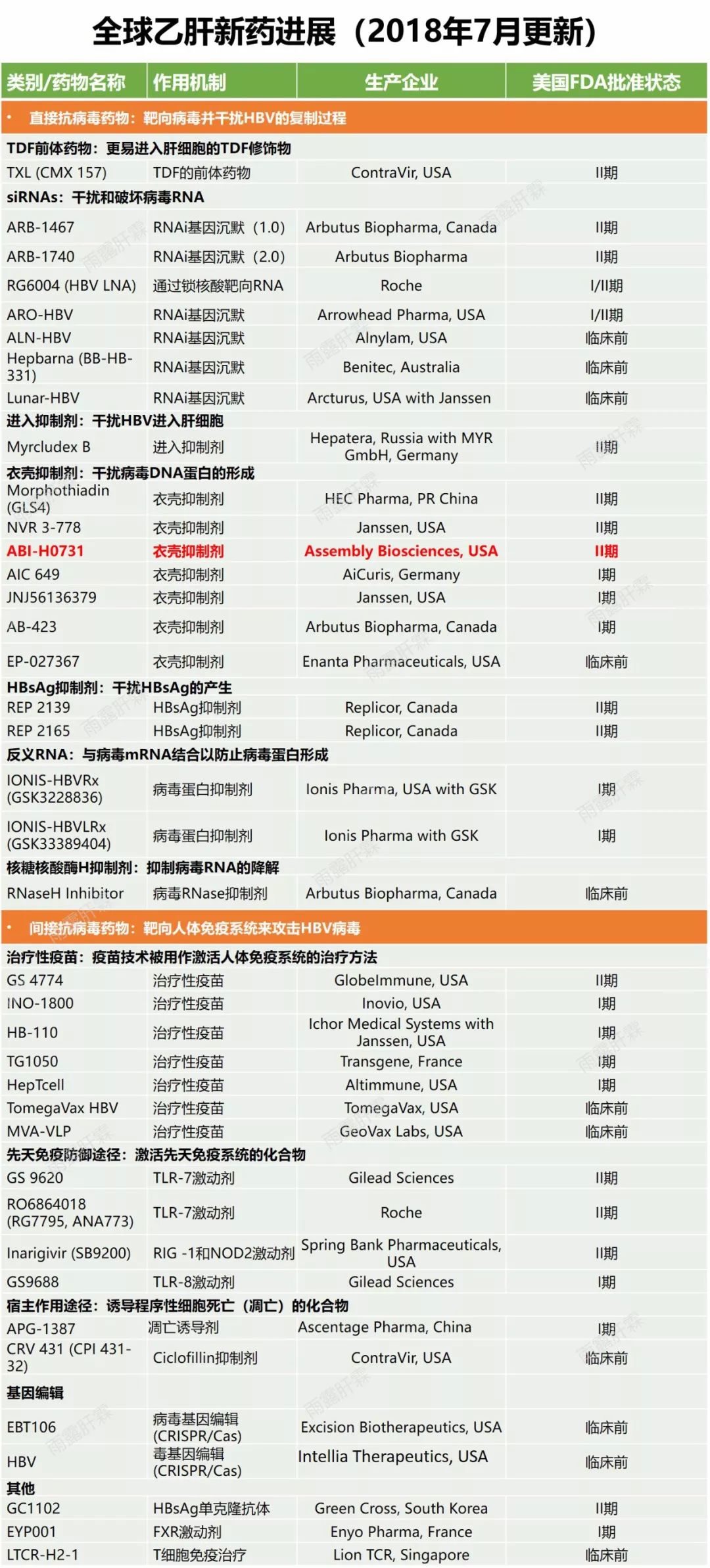
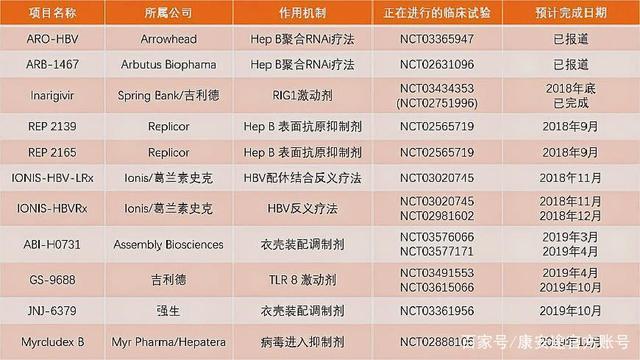
生物醫藥公司百濟神州有限公司(BeiGene, Ltd)與Assembly Biosciences公司達成合作協議,根據協議,Assembly公司授予百濟神州 VBR(ABI-H0731)、ABI-H2158(去年已停止)以及ABI-H3733在中國(包括港澳台地區)的獨家開發和商業化權利。
來自AssemblyB肝新藥研發管道,可見百濟神州已獲得兩款候選藥物中國獨家開發

在研B肝新藥VBR/H3733,Assembly授予百濟神州,在我國獨家開發
百濟神州是一家全球性商業化生物醫藥公司,致力於成為分子靶向藥物和免疫腫瘤藥物研發。根據這項協議,百濟神州負責針對以上候選藥物在中國的開發、藥政注冊以及商業化活動。Assembly公司保留在除上述地區以外的全球範圍內對其B肝研發管線的全部權利。
這三款研究藥物,我們不會陌生,它們是 Assembly Bio公司B肝新藥研發管道中核心組合,用於治療慢性B肝感染的臨床階段核心抑製劑。

ABI-H0731,現已更名為VBR,去年2月末,Assembly公司宣布放棄ABI-H0731作為一種慢B肝抑製療法3期注冊性研究(不進入第3期研究,目前主要以組合臨床試驗為主)。2021年美肝會上,研究人員繼續帶來了VBR更多臨床試驗數據,它也是Assembly公司第一代核心抑製劑,在第2期研究中,儘管B肝e抗原陽性受試者繼續接受 NRTI療法,但在停用VBR後,受試者的pgRNA以及HBVDNA均立即反彈。
研究結果重在說明,B肝受試者停用研究藥物VBR,繼續使用核苷類逆轉錄酶抑製劑,受試者的各項病毒標誌物隨即反彈!這說明,在 VBR+Nrtl組合療法中,VBR扮演著強效抑製HBV複製作用,一旦停用VBR就容易導致反彈。
ABI-H2158,它是Assembly公司第二代核心抑製劑。去年9月初,研究人員基於其第2期臨床試驗中受試者的丙氨酸轉氨酶 (ALT) 水準升高,因而決定停止ABI-H2158後續開發(因關注到 ALT水準與藥物誘導的肝毒性反應一致,決定停止,未滿足安全性標準)。
這項2期研究主要是對B肝e抗原陽性或陰性受試者,共有88名入組,他們隨機接受 ABI-H2158+ETV或 安慰劑+ETV,結果有2名接受ABI-H2158發生4級ALT升高而停藥。
ABI-H3733,它是Assembly公司開發的新型核心抑製劑,和前兩代核心抑製劑的主要不同點是,它是一款泛基因型抗病毒活性藥物,在與其他核心抑製劑發生耐藥情況下,ABI-H3733依然繼續能夠保持活性,目前正在第1期臨床試驗中。
來自百濟神州最新公告:有關B肝新藥在中國獨家授權開發

小番健康結語:百濟神州與Assembly Biosciences公司合作協議是於2020年7月達成,由於ABI-H2158已經停止,並從B肝新藥管道中撤下,Assembly授予百濟神州在中國獨家開發的目前是兩款,分別為VBR(ABI-H0731)和ABI-H3733。本研究進展,已發布在百濟神州最新公告中,Assembly公司授予百濟神州在研B肝新藥在中國獨家開發。返回搜狐,查看更多
責任編輯: