▎醫藥觀瀾/報導
繼幾日前恆瑞醫藥的PD-1單抗藥卡瑞利珠單抗在中國獲批上市,用於複發/難治性經典型霍奇金淋巴瘤患者的治療後,近日該葯又迎來新進展。
6月3日,恆瑞醫藥發布公告稱,公司向國家葯監局提交的注射用卡瑞利珠單抗的肝細胞癌2期臨床試驗報告,申請有條件批準上市,已獲審評中心承辦並納入擬優先審評品種公示名單。這意味著,恆瑞醫藥自主研發的這款PD-I單抗新葯的第二個適應症肝細胞癌,有望在優先審評政策下加速獲批上市。同時,恆瑞醫藥還宣布公司已向國家葯監局遞交了卡瑞利珠單抗的食管癌3期主要臨床試驗結果。
注射用卡瑞利珠單抗是一款人源化抗PD-1單克隆抗體,可與人PD-1受體結合併阻斷PD-1/PD-L1通路,恢復機體的抗腫瘤免疫力,從而形成癌症免疫治療基礎。根據公開資料,卡瑞利珠單抗目前正在開展29項臨床研究,涉及適應症有肝癌、晚期非小細胞肺癌、縱膈原發瀰漫大B細胞淋巴瘤、胃食管癌等,探索的治療方案包括了單葯治療和卡瑞利珠單抗聯合阿帕替尼、卡瑞利珠單抗聯合化療、地西他濱等聯合用藥方案。在今年ASCO年會上,卡瑞利珠單抗的10項臨床研究結果將先後亮相,包括多項與阿帕替尼聯合療法的探索。
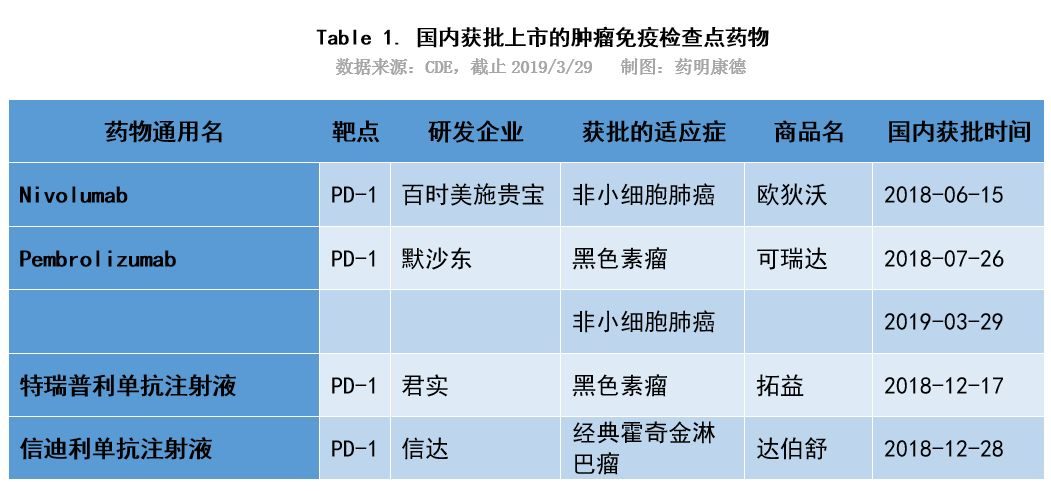
其中,在肝細胞癌領域,nivolumab和pembrolizumab兩款葯分別於2017年9月和2018年11月獲美國FDA加速批準,用於既往接受過索拉非尼治療的肝細胞癌。而在國內,目前尚未有同類PD-1/L1單抗獲批肝細胞癌適應症。
恆瑞醫藥公告還表示,截至目前,該產品項目已投入研發費用約為5.04億元人民幣。
歡迎掃碼關注「醫藥觀瀾」微信公眾號,了解更多中國醫藥創新動態。
參考資料:
[1]恆瑞醫藥關於公司產品擬納入優先審評程序的公告Retrieved June 3,2019 from 恆瑞醫藥公告