第三屆中國醫師協會體外生命支持年會(CSECLS 2019)於2019年6月20日-23日在四川成都隆重召開。會議期間,解放軍總醫院心內科田峰教授就「急性冠脈綜合征(ACS)臨床乾預時機與再血管化」進行了講解。
醫脈通整理報導,未經授權請勿轉載。
ACS是以冠狀動脈不穩定斑塊破裂,繼發完全或不完全閉塞性血栓為病理基礎的一組臨床綜合征,可分為ST段抬高型心肌梗死(STEMI)和非ST段抬高型ACS(NSTE-ACS)。對於STEMI患者,應儘快、充分、持續開通「罪犯」血管,時間就是心肌,時間就是生命;對於NSTE-ACS患者,抗栓不溶栓,根據癥狀、胸痛發作時心電圖、TnT水準進行危險分層,高危患者早期乾預,低危患者保守治療。
STEMI
1. 直接PCI
I類推薦
?發病12h內(包括正後壁心肌梗死)或伴有新出現左束支傳導阻滯的患者(證據水準A)
?伴心源性休克或心力衰竭時,即使發病超過12h者(證據水準B)
IIa類推薦
?發病12~24h內具有臨床和(或)心電圖進行性缺血證據(證據水準B)
?除心源性休克或梗死相關動脈PCI後仍有持續性缺血外,應僅對梗死相關動脈病變行直接PCI(證據水準B)
III類推薦
?無血流動力學障礙患者,不應對非梗死相關血管進行急診PCI(證據水準C)
?發病超過24 h、無心肌缺血、血液動力學和心電穩定的患者不宜行直接PCI(證據水準C)
?不推薦常規使用主動脈內氣囊反搏泵(IABP)(證據水準A)
2. 溶栓後PCI
?溶栓後儘早將患者轉運到有PCI條件的醫院,溶栓成功者於3~24 h進行冠狀動脈造影和血運重建治療(IIa,B);溶栓失敗者儘早實施挽救性PCI(IIa,B)
?溶栓治療後無心肌缺血癥狀或血液動力學穩定者不推薦緊急PCI(III,C)
3. 轉運PCI
?若STEMI患者首診於無直接PCI條件的醫院,當預計首次醫療接觸(FMC)至PCI的時間延遲<120 min時,應儘可能地將患者轉運至有直接PCI條件的醫院(I,B)
?如預計FMC至PCI的時間延遲>120 min,則應於30 min內溶栓治療
?根據我國國情,也可以請有資質的醫生到有PCI設備的醫院行直接PCI(時間<120 min)(IIb,B)
4. 未接受早期再灌注治療STEMI患者的PCI(癥狀發病>24 h)
?病變適宜PCI且有再發心肌梗死、自發或誘發心肌缺血或心原性休克或血液動力學不穩定的患者建議行PCI治療(I,B)
?左心室射血分數(LVEF)<40%、有心力衰竭、嚴重室性心律失常者應常規行PCI(IIa,C)
?STEMI急性發作時有臨床心力衰竭的證據,但發作後左心室功能尚可(LVEF>40%)的患者也應考慮行PCI(IIa,C)
?對無自發或誘發心肌缺血證據,但梗死相關動脈有嚴重狹窄者可於發病24 h後行PCI(IIb,C)
?對梗死相關動脈完全閉塞、無癥狀的1~2支血管病變,無心肌缺血表現,血液動力學和心電穩定患者,不推薦發病24 h後常規行PCI(III,B)
NSTE-ACS
指南建議,根據患者的病史、癥狀、體征、心電圖和肌鈣蛋白作為風險分層的工具(I,A)。採用GRACE評分進行缺血危險分層,分為緊急(2h以內)、早期(24h以內)和延遲(72h以內),以及再評價/藥物治療的血運重建策略。
存在至少下列一項表現的極高危患者,推薦立即侵入治療(<2 h):
?血流動力學不穩定或心源性休克
?藥物治療無效的反覆發作或持續性胸痛
?致命性心律失常或心跳驟停
?心肌梗死合併機械性併發症
?急性心力衰竭
?反覆ST-T波動態改變,尤其是伴間歇性ST段抬高
存在至少下列一項表現的高危患者,推薦早期侵入治療(<24 h):
?肌鈣蛋白水準升高
?ST段或T波動態演變(有或無癥狀)
?GRACE評分>140分
存在至少下列一項表現的中危患者,推薦侵入治療(<72 h):
?糖尿病腎功能不全,eGFR<60 ml/min/1.73 m2
?左心室功能下降(LVEF<40%)或充血性心力衰竭
?早期心肌梗死後心絞痛
?近期PCI治療
?既往CABG史
?GRACE評分>109但<140分
?無創檢查時反覆出現缺血癥狀
無上述風險表現,且無再發癥狀的患者,推薦在決定侵入性檢查前行非侵入性檢查(首選心臟超聲等影像方法),尋找缺血證據,再決定是否採用侵入策略。
血流動力學支持
高危/極高危ACS患者常合併各種併發症,如心衰、肺水腫、心源性休克、再灌注損傷及機械併發症,有效的血流動力學支持可提高手術成功率,降低患者死亡率。血流動力學支持的方法包括使用血管活性藥物(如多巴胺、腎上腺素、去甲腎上腺素、多巴酚丁胺等)和器械輔助(如IABP、Impella、ECMO)。
1. IABP——降低左室後負荷
若血管活性藥物不能改善臨床情況:心率快、肢端濕冷、心衰發作、少尿,尤其是多巴胺> 10~15 μg/kg/min,應使用IABP,降低左室後負荷。當出現機械併發症時更依賴IABP,如乳頭肌斷裂、室間隔穿孔、心臟破裂。
2014年ESC/EACTS《心肌血運重建指南》建議:STEMI合併機械併發症導致血流動力學不穩定/心源性休克的患者,應考慮接受IABP治療(IIa,C);不推薦心源性休克患者常規使用IABP(III,A)。
2015年《中國STEMI診斷和治療指南》建議:血運重建治療術前置入IABP有助於穩定血流動力學狀態,但對遠期死亡率的作用仍有爭議(IIb,B)。
2017年ESC《急性ST段抬高型STEMI》指南指出:不推薦所有心源性休克患者常規使用IABP (III類)。對於機械併發症導致的心源性休克患者,應考慮使用IABP(IIa,C)。
2. IABP or ECMO:時機與輔助循環方法選擇
IABP僅適用於AMI後發生心源性休克的早期,器官功能尤其是心肌尚未發生不可逆缺血損傷,血壓尚能維持在50 mmHg以上的水準。
ECMO不論是休克早期還是在血壓更低的水準均能提供更有效的循環和呼吸支持。
休克晚期組織損傷進入到不可逆的階段後,兩者均不能發揮有效作用。
如心電穩定、自身心臟有一定功能,則先採取IABP輔助,如效果不佳,考慮聯合ECMO治療。對於心功能嚴重受損的患者宜先行ECMO輔助,如血壓仍然較低者,及時地聯合應用IABP。
對於急性心肌梗死合併心臟驟停,需進行CPR的的患者,使用ECMO 輔助心肺復甦,心肺復甦成功後在ECMO輔助下進行急診介入治療。
3. ECMO的應用時機
無客觀指標,但有證據長時間持續的低心排量、低灌注和氧化,將會導致較差的預後。儘管ECMO有相應的風險,但儘早啟用ECMO可以減少併發症和改善預後。
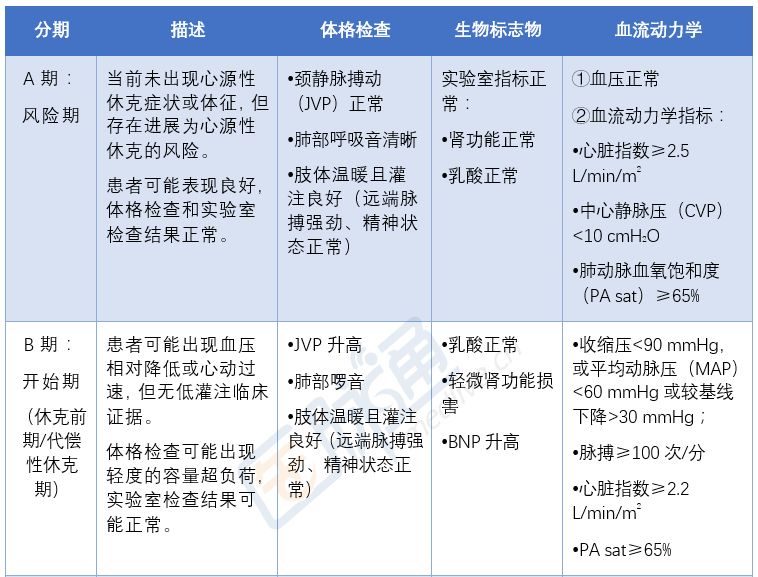
此外,對於心源性休克新的分期C期和D期,以及使用20 μg/kg·min劑量的多巴胺或0.19 μg/kg·min劑量的去甲腎上素仍不能維持患者的血壓時,也應啟用ECMO。