中國證券網訊 5月25日,三生製藥宣布,胰高血糖素樣肽-1受體激動劑(GLP-1RA)周製劑「百達揚」(注射用艾塞那肽微球)正式上市。這是國內目前唯一獲批上市的一周一次用降糖葯。GLP-1RA現成為全球降糖葯增長的最大動力,目前國內多家企業已經布局,行業觀點認為,降糖葯市場更新在即。
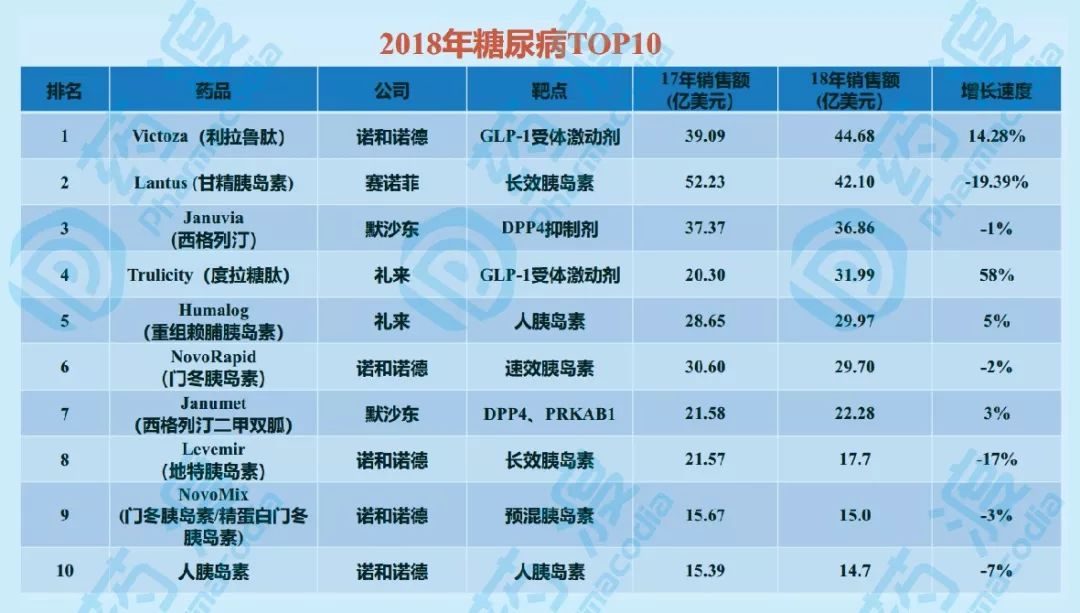
我國的糖尿病發病率迅猛攀升,患病人群已達到1.14億,降糖葯市場受到更廣泛關注。GLP-1RA有多種機制促進血糖降低,但不易引發低血糖風險。同時,部分GLP-1RA已被證實有降低心血管事件發生和減重的增益,可有效降低併發症風險。
2018年1月發布的《中國2型糖尿病防治指南》中提到,GLP-1RA的治療地位將從三線治療手段提升為二聯治療方案之一。2018年初,三生製藥的注射用艾塞那肽微球獲批上市,成為國內首個長效GLP-1RA。同時,多家葯企也在申報GLP-1RA相關臨床試驗,或重金購買GLP-1相關的新葯技術或商業權利。
三生製藥向阿斯利康共支付6.7億元購買艾塞那肽(注射液、緩釋劑)在內的四款糖尿病產品在中國的商業化獨家權利;江蘇豪森研發的首個國產暢銷GLP-1RA洛塞那肽上市申請已於2017年12月獲國家藥品評審中心受理,目前已納入優先審評名單,預計2018年下半年即可獲批;通化東寶的利拉魯肽於2017年11月臨床申請獲原國家食品藥品監督管理總局(CFDA)受理,成為繼翰宇葯業和華東醫藥後的第三家申報臨床企業;昆葯集團的蘇帕魯肽於2017年12月獲CFDA受理;華東醫藥的TTP273於2017年12月在美國完成IIb期臨床,成為首創的小分子非肽類口服劑型。
據諾和諾德的報告,使用GLP-1RA的患者一般是由於服用口服降糖葯但血糖控制效果不佳,轉而使用GLP-1RA。國際糖尿病聯盟西太平洋地區主席、艾塞那肽微球亞洲III期臨床研究的首席研究者、北京大學人民醫院內分泌科主任紀立農教授指出,「對於中國的2型糖尿病患者,一周一次的艾塞那肽微球治療26周後可有效改善患者血糖,同時降低體重;此外,與短效艾塞那肽製劑治療組相比,艾塞那肽微球治療組胃腸道不良反應更少,低血糖風險更低,血糖控制得更好。在歐美糖尿病藥物市場,GLP-1受體激動劑周製劑在2型糖尿病藥物中是處方量增長最快的藥物」。
IMS的統計顯示,目前全球範圍內GLP-1RA佔到降糖藥物市場的12%,而中國的GLP-1RA佔比排名最後,僅為1%。現在,中國糖尿病患者人數佔全球1/4,到2040年,中國的患病人數將達到1.51億,而根據目前以胰島素治療為主的治療路徑,僅有不到一半的患者血糖得到了控制,未來有望提高對GLP-1RA的使用。同時,GLP-1RA的心血管增益、減肥等效果也將在臨床上得以重視,減少糖尿病併發症的出現。
隨著進口GLP-1RA快速進入國內市場,3至5年後競爭將趨於白熱化。根據中國產業資訊網數據,2015年中國糖尿病市場規模總體達到413億元。國信證券預測認為,估算到2020年,中國降糖葯銷售額可達500億元,GLP-1RA的市場規模可達25億元。(張雪)