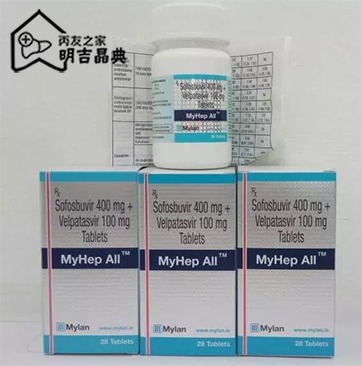
吉利德針對慢性丙型肝炎病毒的泛基因型治療藥物--丙通沙?(索磷布韋/維帕他韋)通過了國家藥品監督管理局的審批。
丙通沙?是中國首個獲批的泛基因型、每日一次、針對慢性丙型肝炎病毒的單一片劑

2018年5月30日,上海——吉利德科學公司(NASDAQ:GILD)今日宣布,國家藥品監督管理局批準丙通沙?(索磷布韋400 mg /維帕他韋100 mg)可用於治療基因1-6型慢性丙型肝炎病毒(HCV)的成人感染患者。國家藥品監督管理局同時批準丙通沙?聯合利巴韋林(RBV)可用於C肝合併失代償期肝硬化的成年患者。丙通沙?是中國首個通過審批的泛基因型HCV單一片劑方案(STR)。
丙通沙?能夠在中國獲得批準,主要基於五項國際多中心3期臨床研究,即ASTRAL-1、ASTRAL-2、ASTRAL-3、ASTRAL-4和ASTRAL-5。在很難治癒的患者群體(包括經治患者,以及代償期或失代償期肝硬化患者)中,SVR12(定義為完成治療後的第12周,檢測不出HCV RNA)的總體實現率較高,為92%-100%。
「丙通沙?的安全性和有效性已被大量的臨床試驗和真實世界的數據證實,」北京大學人民醫院肝病研究所魏來教授說,「由於丙通沙?對所有基因型的C肝患者都有高治癒率,我們在治療時有望免除基因分型的檢測,這對擴大C肝治療有積極意義。」
在中國,HCV是第四大常見傳染病,約有1000萬人受到感染。其中,HCV 基因1、2、3和6型佔全部病例的96%以上。[1]
在ASTRAL-1、ASTRAL-2和ASTRAL-3研究中,1,035名不伴肝硬化/伴代償期肝硬化的基因1-6型HCV感染的初治患者和經治患者接受了12周的丙通沙?治療。98%(1,015/1,035)的患者實現了SVR12。在ASTRAL-5 的研究中,106名不伴肝硬化/伴代償期肝硬化的基因1-6型HCV感染的初治患者和經治患者接受了12周的丙通沙?治療,他們還同時感染了HIV, 正在接受平穩的抗逆轉錄病毒治療。其中,95%(101/106)的患者實現了SVR12。
ASTRAL-4研究評估了267名失代償期肝硬化(Child-Pugh B級)的基因1-4型和基因6 型 HCV感染患者接受12周丙通沙?聯合/不聯合利巴韋林(RBV)治療或者24周的丙通沙?治療的安全性和有效性。其中,接受了12周的丙通沙?聯合RBV治療的失代償期肝硬化的患者,實現了94%(82/87)的SVR12。
在ASTRAL-1、ASTRAL-2、ASTRAL-3和ASTRAL-5中,接受丙通沙?治療的患者最常見的不良反應(≥10%)包括頭痛和疲乏。在ASTRAL-1研究中,安慰劑組的患者出現頭痛和疲乏的頻率與之相似。在ASTRAL-4中,伴有失代償期肝硬化的HCV感染患者接受丙通沙?和利巴韋林(RBV)治療後最常見不良反應(≥10%)包括疲乏、貧血、噁心、頭痛、失眠和腹瀉。四名服用丙通沙?聯合RBV的患者由於不良反應而停止治療。
「作為首個無需考慮HCV患者基因型和肝纖維化程度、每日一次的單片劑治療方案,丙通沙?在很大程度上簡化了中國醫生對C肝患者的治療,同時有望在公共衛生層面減輕HCV帶來的巨大負擔,」吉利德科學公司總裁兼首席執行官John F. Milligan博士表示,「吉利德已經在中國推出了兩種直接抗病毒治療方案,而且我們始終致力於為患者的篩查和治療工作提供相應的支持,以助力解決中國的HCV流行問題。」
2016年,丙通沙?獲得了美國食品藥品監督管理局(FDA)和歐盟委員會的上市許可,成為了首個用於HCV感染的泛基因型單一片劑方案。此外,丙通沙?也已在54個國家獲批。
索華迪?(Sofosbuvir)作為單片製劑,在2017年獲得中國食品藥品監督管理總局的批準,是聯合抗病毒治療方案的重要組成部分,用於治療基因1,2,3,4,5 或者6 型的成人和青少年( 12-18 歲,基因2和3型)HCV感染患者。
###
丙通沙?、索華迪?是吉利德科學公司或其相關公司的註冊商標。
吉利德科學在中國
在中國,吉利德承諾用創新產品解決尚未滿足的醫療需求。2007年進入中國以來,吉利德從藥物生產起步,並逐步轉型,於2016年在上海正式設立中國總部進行商業運營。
關於吉利德科學
吉利德科學是一家生物製藥公司,在未滿足的醫療需求領域發現、研發創新療法並使之商業化。公司的使命是改善和簡化全球重疾患者的治療方案。吉利德在全世界超過35個國家進行運營,總部位於加利福尼亞州福斯特市。
前瞻性聲明
本新聞稿包含1995年私人證券訴訟改革法案所界定的前瞻性聲明,這些聲明受到風險、不確定性和其他因素的影響,包括醫生在處方丙通沙?可能無法預見到的風險。由於諸多風險和不確定因素,實際結果可能與目前預期的結果存在重大差異。謹請讀者注意,不要依賴這些前瞻性聲明。這些和其他的風險在吉利德截止於2017年12月31日的10-k 年報中有詳述,並在美國證券交易委員會登記備案。所有前瞻性聲明均基於Gilead目前可獲知的資訊, Gilead不承擔任何義務並且不承諾更新任何此類前瞻性聲明。
關於吉利德科學的更多資訊,請訪問公司官網www.gileadchina.com,或關注公司官方微信號「吉利德科學」。
[1]China HCV Guidelines 2015.