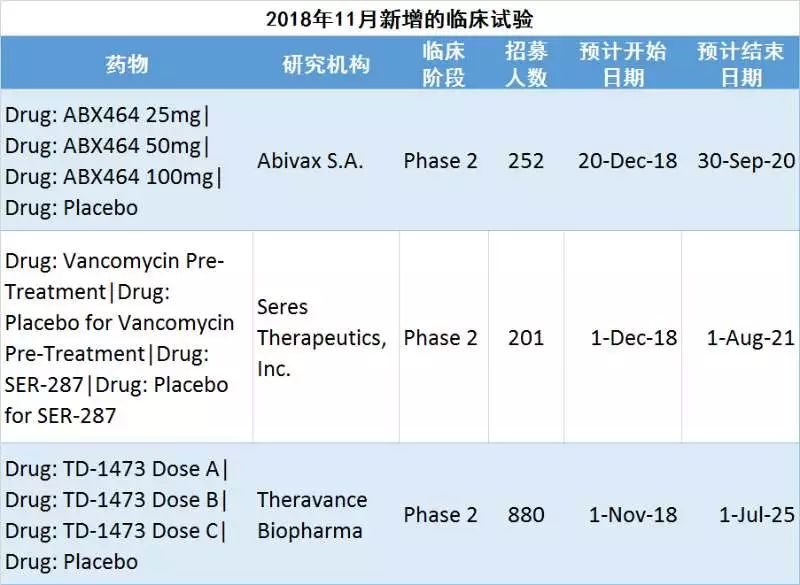
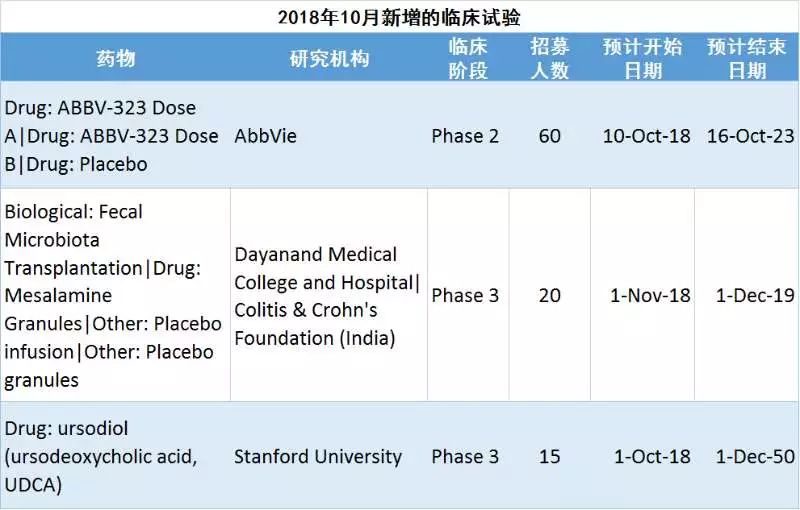
研究背景
現在,由北京協和醫院,中山大學附屬第一醫院等全國三十多家大型醫院開展一項CBP-307 針對中重度潰瘍性結腸炎/克羅恩病治療的臨床項目,該項目已獲得國家藥品食品督管理總局(CFDA)批準,批件號2017L00503
研究概要
①研究課題:多中心、隨機、雙盲、安慰劑對照、評價CBP-307在中重度潰瘍性結腸炎/克羅恩受試者中的有效性和安全性的II期臨床試驗
②試驗藥物:CBP-307膠囊
③面向受試者:中重度UC/CD
④招募例數:195/192人
試驗藥物
CBP-307是一個口服的新型的鞘氨醇-1-磷酸鹽受體亞型1(S1P1)調節物,根據已完成的CBP-307臨床前藥理毒理學研究、臨床I期研究以及已報導的第二代S1P1藥物治療中重度UC/CD患者的臨床研究結果,預測CBP-307可能對該疾病會有較好的療效和耐受性。
主要入選標準
潰瘍性結腸炎:
①受試者年齡為18-75歲(含)的男性或女性
②受試者在篩選前確診UC至少3個月,UC的診斷有臨床表現和內鏡檢查的證據,並且有組織病理學報告支持。
③中重度活動性UC,且目前正在口服5-ASA類藥物(美沙拉嗪/柳氮磺吡啶等)或口服或靜脈注射皮質類固醇(激素)
克羅恩:
①受試者年齡為18-75歲(含)的男性或女性
②受試者在篩選前確診CD至少3個月,CD的診斷有臨床表現和內鏡檢查的證據,並且有組織病理學報告支持。
③中重度活動性CD,且目前正在口服5-ASA類藥物(美沙拉嗪/柳氮磺吡啶等)或口服或靜脈注射皮質類固醇(激素)
聯繫方式
如您願意參加該研究,或想了解本研究更多的信息,請聯繫醫脈通CBP-307研究招募組。參與研究的受試者,本研究藥物、研究相關程序和檢查以及研究的訪視均免費,且為您每次訪視提供一定的交通補助。
電話:010-64405225 轉 889(周一至周五)
手機:17190442160(可加微信,隨時和我們溝通)
研究中心表
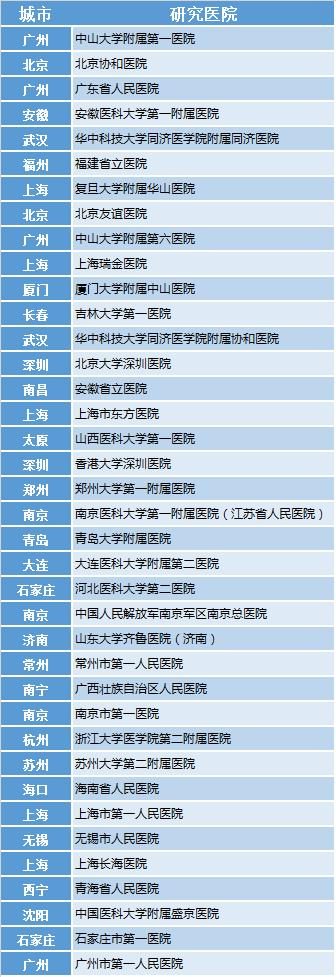
註:「研究概要」等部分信息來源自「藥物臨床試驗登記與信息公示平台」(CDE)