歡迎個人在朋友圈轉發分享
如需平台轉載,請後台聯繫授權
大多數抗癌藥物並不能區分癌細胞和正常細胞,會同時殺死這兩種細胞。近日《自然通訊》刊發一項研究成果,證實了一種特殊的核酸納米結構可避開正常細胞,直接靶向作用於癌細胞。
早在100多年前,德國諾貝爾獎得主保羅·埃爾利希就為業界帶來靶向治療「靈丹妙藥」的早期概念:未來某一天,醫生可採用這種藥物靶向治療感染人體的微生物,同時避免對身體其他部位造成傷害。
傳統化療藥物副作用大▲▲▲儘管化療靶向治療癌症的療效顯著,但伴隨的副作用仍對病人帶來損害。
密蘇裡大學的David Porciani博士和他的團隊證實了一種特殊的核酸納米結構可避開正常細胞的同時,精準靶向作用於癌細胞。該項研究成果近日發表在《自然通訊》雜誌上。

研究項目負責人David Porciani博士
研究人員稱:大多數癌症治療藥物並不能區分癌細胞和正常細胞,因此會同時殺死這兩種細胞。在短期內,這種抗癌療法帶來的副作用對身體的損害比癌症本身更嚴重。
「智能」分子可與癌細胞特異性結合▲▲▲研究人員正在研發一種「智能」分子,可與癌細胞表面的受體特異性結合,這些受體是癌症所特有的,利用這些智能分子作為載體對癌症進行診斷或精準治療。
Porciani和他的團隊通過一種模仿高度加速模式的自然進化分子過程,找到了核酸配體或適配體。由於其三維結構特性,適配體可演變成具有高親和力和選擇性的分子與特定目標結合。當結合靶點是癌症相關受體時,這些適配體可作為識別特定癌變細胞的分子工具。
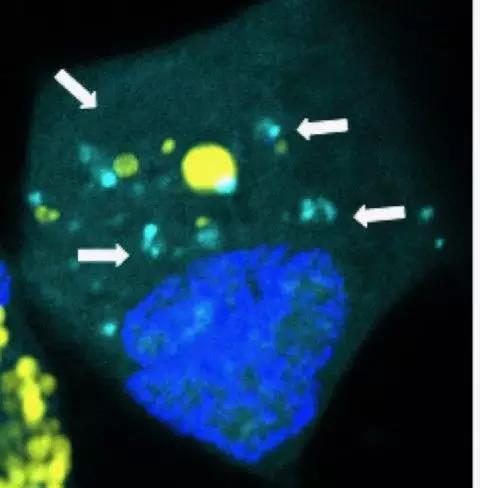
研究人員用熒遊標記的大分子RNA適配體,生成核酸納米結構。在與靶向治療癌細胞和非靶向細胞一起孵育時,只有惡變的細胞被核酸納米結構識別產生熒光信號,表明核酸納米結構可正確地與目標細胞結合。
Porciani博士指出:研究的下一步是證實這些適配子可裝載治療分子,靶向治療癌細胞,而不影響正常組織。
過去,適配體已被證明可裝載小分子藥物的載體,而這項研究為來發更具潛力的RNA配體藥物鋪平路線,這些藥物將有望成為埃利希在上個世紀提出的「靈丹妙藥」!


報名免費參會等詳情,請查看【閱讀原文】
學術亮點
探討兒童腦瘤、神經系統腫瘤手術方案、精準化療以及質子放療前沿進展,包括案例演示和討論。宣布成立中美首個國際專科疾病(兒童神經系統腫瘤)「醫聯體」和國際遠程醫療協作網平台。